
【题目】设NA为阿伏加德罗常数的数值,下列说法正确的是( )
A.在密闭容器中,使1molN2和3molH2充分反应后生成NH3的分子数为2NA
B.标准状况下,0.56L丙烷中含有共价键的数目为0.2NA
C.2gH218O和D2O的混合物中,含有的中子数为NA
D.标准状况下1.12LNO2通入足量NaOH溶液中被完全吸收,转移电子数为NA
【答案】C
【解析】
A.N2与H2化合成NH3的反应为可逆反应,在密闭容器中1molN2和3molH2充分反应后生成NH3分子物质的量小于2mol,生成的NH3分子数小于2NA,A项错误;
B.n(C3H8)=![]() =0.025mol,1个丙烷分子中含2个C-C键和8个C-H键,标准状况下0.56L丙烷中含有的共价键物质的量为0.025mol×10=0.25mol,B项错误;
=0.025mol,1个丙烷分子中含2个C-C键和8个C-H键,标准状况下0.56L丙烷中含有的共价键物质的量为0.025mol×10=0.25mol,B项错误;
C.H218O和D2O的摩尔质量都是20g/mol,2gH218O和D2O混合物中分子物质的量为![]() =0.1mol,1个H218O分子和1个D2O分子中都含有10个中子,2gH218O和D2O混合物中含有中子物质的量为0.1mol×10=1mol,含有的中子数为NA,C项正确;
=0.1mol,1个H218O分子和1个D2O分子中都含有10个中子,2gH218O和D2O混合物中含有中子物质的量为0.1mol×10=1mol,含有的中子数为NA,C项正确;
D.二氧化氮与氢氧化钠反应的方程式为2NO2+2NaOH=NaNO3+NaNO2+H2O,标准状况下1.12LNO2的物质的量是0.05mol,通入足量NaOH溶液中被完全吸收,转移电子数为0.025NA,D项错误;
答案选C。


科目:高中化学 来源: 题型:
【题目】某兴趣小组研究亚硝酸钠,查阅下列资料,试根据信息回答下列问题。
药品 | NaNO2 (亚硝酸钠) |
性质 | 1.在酸性溶液中有较强氧化性,能将Fe2+ 氧化成Fe3+ ; 2.AgNO2是一种难溶于水、易溶于酸的盐。 |
(1)已知NaNO2能发生如下反应:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。请用双线桥表示电子转移的方向和数目:___。
(2)误食NaNO2会导致血红蛋白中的Fe2+转化为Fe3+ 而中毒,可服用维生素C 解毒。下列分析错误的是__(填序号)。
A.NaNO2被还原 B.维生素C具有还原性
C.还原性:维生素C>Fe2+ D.NaNO2是还原剂
(3)下列方法中,可用来区分NaNO2和NaCl的是___(填序号)。
A.焰色反应 B.分别滴加酸化FeSO4溶液和KSCN溶液
C.在酸性条件下加入KI 淀粉溶液 D.分别滴加AgNO3溶液
(4)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
①晶体中分子间作用力越大,分子越稳定 ②原子晶体中共价键越强,熔点越高 ③干冰是CO2分子通过氢键和分子间作用力有规则排列成的分子晶体 ④在Na2O和Na2O2晶体中,阴、阳离子数之比相等 ⑤正四面体构型的分子,键角都是109°28′,其晶体类型可能是原子晶体或分子晶体 ⑥分子晶体中都含有化学键 ⑦含4.8 g碳元素的金刚石晶体中的共价键的物质的量为0.8 mol
A. ①②③④⑤ B. ②④⑦ C. ⑤⑥⑦ D. ③④⑤⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在由Cu片、Zn片和200 mL稀H2SO4组成的原电池中,当Cu片上放出2.24 L(标准状况下)H2时,H2SO4恰好用完。问:
(1)此时在导线上有________摩尔电子通过?
(2)Zn片溶解的质量是________?
(3)原稀H2SO4的物质的量浓度是________?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将等物质的量的A、B 混合于 2L 的密闭容器中,发生下列反应:3A(g)+B(g) xC(g) +2D(g),经2min 后测得D 的浓度为 0.5mol·L-1,c(A)∶c(B)=3∶5,以 C 表示的平均速率 v(C)=0.25mol·L-1·min-1,下列说法正确的是( )
A.该反应方程式中,x=2B.2 min 时,A 的转化率为 50%
C.2 min 时,A 的物质的量为 0.75molD.反应速率 v(B)=0.25 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(题文)亚氯酸钠(NaClO2)是重要漂白剂。探究小组开展如下实验,回答下列问题:
实验Ⅰ:制取NaClO2晶体按右图装置进行制取。
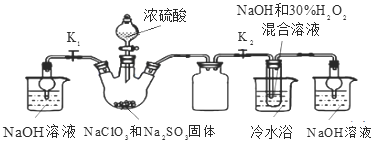
A B C D E
已知:NaClO2饱和溶液在低于38℃时析出NaClO23H2O,38-60℃时析出NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。
(1)用50%双氧水配制30%的H2O2溶液,需要的玻璃仪器除玻璃棒、胶头滴管、烧杯外,还需要_____(填仪器名称);装置C的作用是_____________________。
(2)B中产生ClO2的化学方程式______________________________________。
(3)装置D中反应生成NaClO2的化学方程式为____________________________ 。反应后的溶液中阴离子除了ClO2-、ClO3-、Cl-、ClO-、OH—外还可能含有的一种阴离子是_________,检验该离子的方法是___________________________。
(4)请补充从装置D反应后的溶液中获得NaClO2晶体的操作步骤。
①减压,55℃蒸发结晶;②______________;③______________;④______________;得到成品。
(5)如果撤去D中的冷水浴,可能导致产品中混有的杂质是______________;
实验Ⅱ:样品杂质分析与纯度测定
(6)测定样品中NaClO2的纯度。测定时进行如下实验:
准确称一定质量的样品,加入适量蒸馏水和过量的KI晶体,在酸性条件下发生如下反应:ClO2-+ 4I-+4H+ =2H2O+2I2+Cl-,将所得混合液稀释成100mL待测溶液。
取25.00mL待测溶液,加入淀粉溶液做指示剂,用c mol·L-1 Na2S2O3标准液滴定至终点,测得消耗标准溶液体积的平均值为V mL(已知:I2 +2S2O32-=2I-+S4O62-)。
①确认滴定终点的现象是__________________________________________________。
②所称取的样品中NaClO2的物质的量为______________mol(用含c、V的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用燃烧法测定某种氨基酸(CxHyOzNm)的分子组成。取Wg该种氨基酸放在纯氧中充分燃烧,生成二氧化碳、水和氮气。按下图所示装置进行实验。

回答下列问题:
(1)实验开始时,首先通入一段时间的氧气,其理由是__________________。
(2)以上装置中需要加热的仪器有_______ (填写字母),操作时应先点燃_____处的酒精灯。
(3)A装置中发生反应的化学方程式是____________________________。
(4)D装置的作用是____________________________。
(5)读取氮气的体积时,应注意①_________________;②_________________。
(6)实验中测得氮气的体积为VmL(标准状况),为确定此氨基酸的分子式,还需要的有关数据有____________________。
A.生成二氧化碳气体的质量
B.生成水的质量
C.通人氧气的体积
D.氨基酸的相对分子质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将有机物完全燃烧,生成CO2和H2O,将12 g该有机物完全燃烧产物通过浓硫酸,浓硫酸增重14.4 g,再通过碱石灰,又增重26.4 g。则该有机物的分子式为( )
A. C4H10 B. C2H6O
C. C3H8O D. C2H4O2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com