
【题目】在一密闭容器中,发生可逆反应:3A(g)![]() 3B+C(正反应为吸热反应),平衡时,升高温度,气体的平均相对分子质量有变小的趋势,则下列判断中正确的是
3B+C(正反应为吸热反应),平衡时,升高温度,气体的平均相对分子质量有变小的趋势,则下列判断中正确的是
A.B和C可能都是固体B.B和C一定都是气体
C.若C为固体,则B一定是气体D.B和C不可能都是气体
【答案】C
【解析】
正反应吸热,随着温度的升高,则平衡向正反应方向移动,气体平均相对分子质量变小,如气体的质量不变,则说明气体的物质的量增多,如气体的质量减小,则气体的物质的量不变也符合。
A、若B和C都是固体,气体只有A,气体的平均相对分子质量不变,故A错误;
B、若B和C都是气体,升高温度平衡向正反应方向移动,混合气体总质量不变,总的物质的量增大,平均相对分子质量减小。若C为非气态,升高温度平衡向正反应方向移动,混合气体总质量减小,总的物质的量不变,平均相对分子质量也减小,故B错误;
C、若B和C都是固体,气体只有A,气体的平均相对分子质量不变,故若C为固体,则B一定是气体,高温度平衡向正反应方向移动,混合气体总质量减小,总的物质的量不变,平均相对分子质量也减小,故C正确;
④若B和C都是气体,升高温度平衡向正反应方向移动,混合气体总质量不变,总的物质的量增大,平均相对分子质量减小,故D错误,
故选C。


 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:高中化学 来源: 题型:
【题目】一定温度下的恒容密闭容器中,可逆反应2NO2(g)![]() 2NO(g)+ O2(g)达到平衡状态的标志是
2NO(g)+ O2(g)达到平衡状态的标志是
①2V(O2)=V(NO2)
②单位时间内生成n molO2的同时生成2n molNO2
③NO2、NO、O2的浓度之比为2∶2∶1
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的平均相对分子质量不再改变
A.②④⑥ B.①④⑥ C.②④⑤ D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向50 mL稀H2SO4与稀HNO3的混合溶液中逐渐加入铁粉,假设加入铁粉的质量与产生气体的体积(标准状况)之间的关系如图所示,且每一段只对应一个反应。下列说法正确的是( )

A. 开始时产生的气体为H2
B. AB段发生的反应为置换反应
C. 参加反应铁粉的总质量m2=5.6 g
D. 所用混合溶液中c(HNO3)=0.5 molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在C(s)+CO2(g)![]() 2CO(g)反应中,可使反应速率增大的措施是
2CO(g)反应中,可使反应速率增大的措施是
①压缩容器体积 ②增加炭的量 ③恒容下通入CO2 ④恒压下充入N2 ⑤恒容下充入N2 ⑥升高温度
A.①③⑥B.②④⑥C.①③④D.③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在12g某二价金属的硫酸盐中,含有0 4mol氧原子,此硫酸盐的摩尔质量为_________g/mol。
(2)质量分数为49%的硫酸溶液,密度为1.8g/cm3,则物质的量浓度为__________mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钙晶体(CaO2·8H2O)常温下为白色,能溶于酸,难溶于水、乙醇,是一种温和的氧化剂,常用于鱼类长途运输的增氧剂等。
(1)过氧化钙晶体可用下列方法制备:CaCl2+H2O2+2NH3+8H2O=CaO2·8H2O↓+2NH4Cl。
用如下制取装置制备过氧化钙晶体。
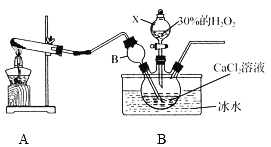
①装置A中发生反应的化学方程式为____________。
②装置C采用冰水浴控制温度在0 ℃左右,可能的原因主要有:
Ⅰ. 该反应是放热反应,温度低有利于提高CaO2·8H2O产率;
Ⅱ.__________________________________。
③反应结束后,经过滤、洗涤、低温烘干可获得CaO2·8H2O。检验晶体已洗涤干净的操作为:______。
(2)测定产品中CaO2·8H2O含量的实验步骤如下:
步骤一:准确称取a g产品于有塞锥形瓶中,加入适量蒸馏水和过量的b g KI晶体,再滴入2 mol·L-1的硫酸溶液,充分反应(I-被氧化I2)。
步骤二:向上述锥形瓶中加入几滴淀粉溶液以指示反应的终点。
步骤三:逐滴加入浓度为c mol·L-1的Na2S2O3溶液至反应完全,滴定至终点,记录数据,再重复上述操作2次,得出3次平均消耗Na2S2O3溶液体积为V mL。发生的反应为:I2+2S2O32-=2I-+S4O62-,产品中CaO2·8H2O的质量分数为____(用含字母的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是实验室制取纯净氯气的装置图,下列说法正确的是( )
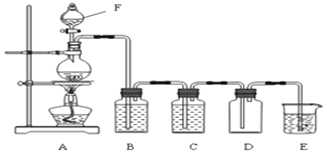
A.分液漏斗中盛装的是浓硫酸
B.B的目的是为了除去氯气中的水分
C.E的目的是为了处理过量的氯气,E中盛装的是Ca(OH)2溶液
D.D广口瓶除了可以用于收集气体外,还可以用做安全瓶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知亚磷酸(H3PO3)的结构如图![]() ,具有强还原性的二元弱酸,可以被银离子氧化为磷酸。
,具有强还原性的二元弱酸,可以被银离子氧化为磷酸。
(1)已知亚磷酸可由PCl3水解而成,请写出相应的方程式___;
(2)Na2HPO3是________(填“正盐”或“酸式盐”);
(3)亚磷酸与银离子反应时氧化剂与还原剂的物质的量之比为______________;
(4)某温度下,0.10molL-1的H3PO3溶液的pH为1.6,即c(H+)=2.5×10-2molL-1,该温度下H3PO3的一级电离平衡常数Ka1=______;(H3PO3第二步电离忽略不计,结果保留两位有效数字)
(5)向H3PO3溶液中滴加NaOH溶液至中性,所得溶液中:c(Na+)_____c(H2PO3-)+2c(HPO32-)(填“>”、“<”或“=”);
(6)向某浓度的亚磷酸中滴加NaOH溶液,其pH与溶液中的H3PO3、H2PO3—、HPO32—的物质的量分数a(X)(平衡时某物种的浓度与整个物种浓度之和的比值)的关系如图所示。
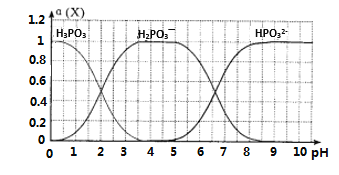
以酚酞为指示剂,当溶液由无色变为浅红色时,发生主要反应的离子方程式是____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com