
【题目】某化学实验室以一种工业上的废渣(废渣主要含有MgCO3、MgSiO3和少量Fe、Al的氧化物)为原料,制备MgCO3·3H2O。实验流程如下图所示:

(1)为了加快废渣的酸溶速率,可采取的办法有_________(任写一点),酸溶时废渣中主要成分发生反应的离子方程式为___________________________________。
(2)加入30%H2O2的目的是__________________________________。
(3)用萃取分液的方法除去溶液中的Fe3+
①加入30%H2O2后,检验溶液中是否含有Fe2+的最佳试剂是__________________________。
②萃取分液完成后,检验水相中是否含有Fe3+的最佳试剂是______________________________。
(4)室温下,除去MgSO4溶液中的A13+(使Al3+浓度小于1×10-6mol/L)而不引入其它杂质,应加入的试剂X为__________,应调节pH的范围为_________________。
已知:①Ksp[Al(OH)3]=1.0×10-33 ②pH=8.5时,Mg(OH)2开始沉淀
(5)向滤液中加入Na2CO3溶液生成MgCO3沉淀并用蒸馏水洗涤,确认沉淀洗净的操作及现象是____________________________。
(6)下图为不同反应温度下所得水合碳酸镁的X射线衍射谱图。由图可知,干燥时需控制温度范围为___________________,温度较高时MgCO3·3H2O发生转化的化学方程式为_______________________________。

【答案】 升高温度、搅拌、提高硫酸浓度等 MgCO3+2H+=Mg2++H2O+CO2↑ MgSiO3+2H+=Mg2++H2SiO3 将Fe2+氧化为Fe3+ ,便于除去 K3[Fe(CN)6]溶液 KSCN 溶液 MgO、Mg(OH)2、MgCO3或Mg2(OH)2 CO3 5.0 取少量最后一次的洗涤过滤液于试管中,向其中滴加盐酸酸化的氯化钡溶液,若不产生白色沉淀,则表明已洗涤干净 293K~313K(313K以下也可) 5MgCO3·3H2O![]() Mg5(OH)2 (CO3)4·4H2O+CO2↑+10H2O
Mg5(OH)2 (CO3)4·4H2O+CO2↑+10H2O
【解析】(1)为了加快废渣的酸溶速率,可采取的办法有升高温度、搅拌、提高硫酸浓度等,酸溶时废渣中主要成分是碳酸镁和硅酸镁,发生反应的离子方程式为MgCO3+2H+=Mg2++H2O+CO2↑、MgSiO3+2H+=Mg2++H2SiO3。(2)溶液中含有亚铁离子,双氧水具有强氧化性,能把亚铁离子氧化为铁离子,便于除去。(3)①检验溶液中是否含有Fe2+的最佳试剂是K3[Fe(CN)6]溶液。②萃取分液完成后,检验水相中是否含有Fe3+的最佳试剂是KSCN溶液。(4)室温下,除去MgSO4溶液中的A13+(使Al3+浓度小于1×10-6mol/L)而不引入其它杂质,应加入的试剂X为MgO、Mg(OH)2、MgCO3或Mg2(OH)2·CO3。根据氢氧化铝的溶度积常数可知当铝离子浓度是1×10-6mol/L时,氢氧根的浓度是![]() ,又因为pH=8.5时,Mg(OH)2开始沉淀,所以应调节pH的范围为5.0<pH<8.5。(5)沉淀表面含有硫酸根离子,可以通过检验硫酸根离子判断沉淀是否洗涤干净,则确认沉淀洗净的操作及现象是:取少量最后一次的洗涤过滤液于试管中,向其中滴加盐酸酸化的氯化钡溶液,若不产生白色沉淀,则表明已洗涤干净。(6)根据图像可知超过313K时碳酸镁晶体会发生化学变化,所以干燥时需控制温度范围为293K~313K,温度较高时MgCO3·3H2O发生转化生成Mg5(OH)2(CO3)4·4H2O,反应的化学方程式为5MgCO3·3H2O
,又因为pH=8.5时,Mg(OH)2开始沉淀,所以应调节pH的范围为5.0<pH<8.5。(5)沉淀表面含有硫酸根离子,可以通过检验硫酸根离子判断沉淀是否洗涤干净,则确认沉淀洗净的操作及现象是:取少量最后一次的洗涤过滤液于试管中,向其中滴加盐酸酸化的氯化钡溶液,若不产生白色沉淀,则表明已洗涤干净。(6)根据图像可知超过313K时碳酸镁晶体会发生化学变化,所以干燥时需控制温度范围为293K~313K,温度较高时MgCO3·3H2O发生转化生成Mg5(OH)2(CO3)4·4H2O,反应的化学方程式为5MgCO3·3H2O![]() Mg5(OH)2(CO3)4·4H2O+CO2↑+10H2O。
Mg5(OH)2(CO3)4·4H2O+CO2↑+10H2O。


科目:高中化学 来源: 题型:
【题目】已知A—L所代表的物质(溶液中的溶质),除F外其余均是中学化学里常见的物质,它们的转化关系如图所示(反应中部分产物及水已略去)。
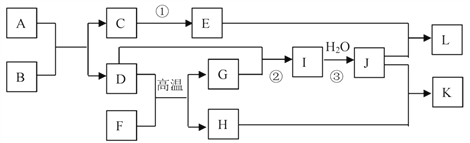
已知:a.通常状况下,A是淡黄色固体,B 是无色无味气体,D 是气体单质,H 是红棕色固体,L是白色胶状沉淀;b.反应①是工业生产普通玻璃的反应之一,反应②③是工业生产J的部分反应;c. F是由两种元素组成的化合物,其质量比为7:8;请填写下列空白:
(1)A的电子式__________。
(2)K的化学式_____________。
(3)完成下列反应方程式:
①D+G→I的化学方程式:_____________。
②E+J→L的离子方程式:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某容积一定的密闭容器中,可逆反应:A(g)+B(g)![]() xC(g),符合下列图象(Ⅰ)所示关系。由此推断对图(Ⅱ)的正确说法是( )
xC(g),符合下列图象(Ⅰ)所示关系。由此推断对图(Ⅱ)的正确说法是( )
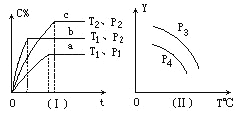
A. P3>P4,Y轴表示A的质量
B. P3<P4,Y轴表示B的百分含量
C. P3>P4,Y轴表示混合气体密度
D. P3>P4,Y轴表示混合气体平均摩尔质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中能用来区别SO2和CO2气体的是( ) ①澄清的石灰水
②氯水
③酸性高锰酸钾溶液
④氯化钡溶液
⑤品红溶液.
A.①④⑤
B.②③⑤
C.①②③
D.②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于燃料电池的说法正确的是
A.燃料电池是通过燃烧方式将化学能转换为电能
B.氢氧燃料电池中,通入氢气的一极为正极
C.氢氧燃料电池是一种环境友好电池
D.燃料电池的能量转化率可达100%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钠、氯及其化合物有如下转化关系,请按要求填空:

(1)Na、Na2O、Na2O2、NaOH久置空气中最终都是变为____________(填化学式);
(2)Na放在石棉网上加热反应的化学方程式为______________________________
(3)Na2O2与水反应的化学方程式为__________________________________
(4)一小块金属钠投入CuCl2溶液中,发生反应的方程式有:___________,和_________________________________________________________________.
(5)在点燃的条件下Fe 与Cl2发生反应的现象为_____________________________________________,反应的化学方程式为______________________________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜元素位于元素周期表中第ⅠB族,在化合物中其化合价可以呈现+1、+2 价。铜的单质及其化合物在很多领域有重要的应用。
Ⅰ.CuSO4和Cu(NO3)2是常见的+2价铜的化合物,有较为广泛的应用。
(1)向CuSO4溶液中滴加氨水,最后可以得到深蓝色的[Cu(NH3)4]SO4溶液。
①N、O、S三种元素的第一电离能由大到小的顺序为______________________________。
②比较NH3 和[Cu(NH3)4]2+中H-N-H键角的大小:NH3___________[Cu(NH3)4]2+(填“>”或“<”),并说明理由________________________。
(2)制备Cu(NO3)2的一种方法是在N2O4的乙酸乙酯溶液中加入铜,反应一段时间后,加热即可得到Cu(NO3)2。
①NO3- 的立体构型的名称为_______________,N原子的杂化方式为________________。NO3- 的一种等电子体为________________________。
②N2O4会发生类似于水的自偶电离N2O4![]() NO++NO3- ,制备无水Cu(NO3)2的化学方程式为__________________________________________。
NO++NO3- ,制备无水Cu(NO3)2的化学方程式为__________________________________________。
Ⅱ.CuCl是较为常见的+1价铜的化合物。
(3)基态Cu+ 的价层电子排布式为________________________。
(4)CuCl的晶胞结构如图所示,C1原子位于立方体的顶点和面心,Cu原子位于Cl原子构成的四面体体心。
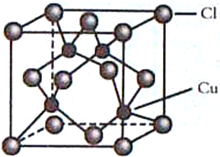
①每个Cl原子周围距Cl原子最近且等距离的Cu原子数目为________________。
②设NA为阿伏加德罗常数的值,晶体的密度为ρg/cm3,CuCl的摩尔质量为M g/mol,计算晶胞中距离最近的两个Cu原子间的距离为___________pm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纳米级碳酸钙广泛应用于橡胶、塑料、造纸、化学建材、油墨、涂料、密封胶等行业。在CaCl2溶液中通入NH3和CO2可以制得纳米级碳酸钙。某化学兴趣小组设计如图所示装置制取该产品。D中装有蘸有稀硫酸的脱脂棉,图中夹持装置已略去。
可选用的药品有:a.石灰石 b.饱和氯化钙溶液 c.6mol/L盐酸 d.氯化铵e.氢氧化钙

(1)A中制备气体时,所需药品是______(选填字母序号)。
(2)B中盛有_____________溶液,其作用是___________________________。
(3)写出该实验中制取氨气的化学方程式________________________________。
(4)在实验中,向C中通入气体是有先后顺序的,应先通入的气体是_____(填化学式)。
(5)检验D出口处有氨气逸出的方法是_____________________________。
(6)写出制纳米级碳酸钙的化学方程式____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图1是细胞中化合物含量的扇形图,图2是有活性的细胞中元素含量的柱形图,下列说法不正确的是( )

A. 若图1表示细胞鲜重,则A、B化合物依次是H2O、蛋白质
B. 若图2表示组成人体细胞的元素含量,则a、b、c依次是O、C、H
C. 地壳与活细胞中含量最多的元素都是a,因此说明生物界与非生物界具有统一性
D. 若图1表示细胞完全脱水后化合物的含量,则A化合物具有多样性,其中含的元素为C、H、O、N
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com