
【题目】下图是部分短周期元素的常见化合价与原子序数的关系图:
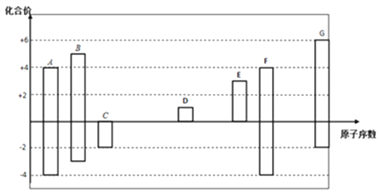
(1)元素A在周期表中的位置_________。
(2)用电子式表示D2G的形成过程_________________。
(3)C、D、G对应的简单离子半径大小顺序是__________(用离子符号回答)。
(4)某同学设计实验装置如图所示,证明A、B、F的非金属性强弱关系:
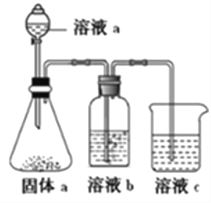
①溶液a和溶液b分别为__________,__________。
②溶液c中的离子反应方程式为___________。
【答案】 第二周期ⅣA族 ![]() S2->O2->Na+ 硝酸(或HNO3) 饱和NaHCO3溶液 SiO32-+CO2+H2O=H2SiO3↓+CO32-
S2->O2->Na+ 硝酸(或HNO3) 饱和NaHCO3溶液 SiO32-+CO2+H2O=H2SiO3↓+CO32-
【解析】A与F均有+4价和-4价,原子序数A小于F,则A是C,F是Si;B有+5价和-3价,则B是N;C只有-2价,C是O;D只有+1价,D是Na;E只有+3价,则E是Al;G有+6价和-2价,G是S。则
(1)碳元素在周期表中的位置为第二周期ⅣA族;(2)D2G是离子化合物硫化钠,用电子式表示的形成过程为![]() ;(3)离子的核外电子层数越多,离子半径越大,核外电子排布相同时离子半径随原子序数的增大而减小,则C、D、G对应的简单离子半径大小顺序是S2->O2->Na+;(4)①要证明C、N、Si的非金属性强弱关系,需要根据较强酸制备较弱酸的原理设计,又因为硝酸易挥发,生成的二氧化碳中含有硝酸,需要除去,因此溶液a和溶液b分别为硝酸、饱和NaHCO3溶液;②根据以上分析可知溶液c中的离子反应方程式为SiO32-+CO2+H2O=H2SiO3↓+CO32-。
;(3)离子的核外电子层数越多,离子半径越大,核外电子排布相同时离子半径随原子序数的增大而减小,则C、D、G对应的简单离子半径大小顺序是S2->O2->Na+;(4)①要证明C、N、Si的非金属性强弱关系,需要根据较强酸制备较弱酸的原理设计,又因为硝酸易挥发,生成的二氧化碳中含有硝酸,需要除去,因此溶液a和溶液b分别为硝酸、饱和NaHCO3溶液;②根据以上分析可知溶液c中的离子反应方程式为SiO32-+CO2+H2O=H2SiO3↓+CO32-。


 黄冈创优卷系列答案
黄冈创优卷系列答案科目:高中化学 来源: 题型:
【题目】乙烯是石油化学工业最重要的基础原料,用乙烯可以制得许多工业材料和日用品,乙烯能发生下列转化关系: 
(1)反应①的化学方程式为:该反应属于反应.
(2)B中所含官能团的电子式为 , D中官能团的名称为 .
(3)已知氯乙烯不溶于水.沸点为﹣13.9℃,则反应②产物A分离的方法为;聚氯乙烯(PVC)曾是世界上产量最大的通用塑料,应用非常广泛.关于聚氯乙烯的说法正确的是 . A.属于纯净物 B.可以燃烧 C.能使溴水褪色 D.可用作食品保鲜膜.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于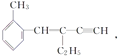 ,下列结论正确的是( )
,下列结论正确的是( )
A. 该有机物分子式为C13H16 B. 该有机物属于苯的同系物
C. 该有机物分子至少有4个碳原子共直线 D. 该有机物分子最多有13个碳原子共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图所示,下列表述正确的是 ( )
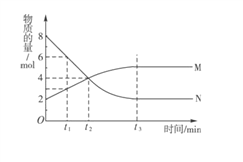
A. 化学方程式为2MN B. t2时,正逆反应速率相等,达到平衡
C. t2时,正反应速率大于逆反应速率 D. t1时,M的浓度是N浓度的2倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A.化学反应除了生成新的物质外,还伴随着能量的变化
B.放热反应不需要从外界吸收任何能量就能发生
C.在一个确定的化学反应中,反应物总能量总是高于生成物总能量
D.物质燃烧不一定是放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知: 2SO2(g)+O2(g)![]() 2SO3(g) △H=-XkJ/mol;
2SO3(g) △H=-XkJ/mol;
2NO(g)+O2(g)![]() 2NO2(g) △H=-YkJ/mol。
2NO2(g) △H=-YkJ/mol。
则反应NO(g)+SO2(g)![]() SO3(g)+NO(g) 的△H=______ kJ/mol。
SO3(g)+NO(g) 的△H=______ kJ/mol。
(2)甲烷是一种高效清洁的新能源,0.25mol甲烷完全燃烧生成液态水时放出热量222.5kJ,则甲烷燃烧的热化学方程式为____________。
(3)以KOH溶液为电解质溶液,依据(2)中反应设计一个原电池,其负极反应式为_______;以H2SO4溶液为电解质溶液,将甲烷燃料电池中的甲烷改为C2H5OH,其负极反应式为_________。
(4)以上述甲烷燃料电池为电源,用铂电极电解1LCu(NO3)2和KNO3混合溶液,通电一段时间,两极均产生11.2L(标准状况)气体。则电解后溶液的pH为______(电解过程中溶液体积不变),原混合溶液中Cu2+的物质的量浓度为___________,假设电解过程中能量利用率为80%,在甲烷燃料电池中消耗的甲烷在标准状况下的体积为________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机物检验方法正确的是( )
A.取少量卤代烃加NaOH水溶液共热,冷却,再加AgNO3溶液检验卤原子存在
B.苯和乙烯都能使溴水褪色,但褪色的原理是不同的
C.用溴水可以鉴别乙烯与乙炔
D.苯和苯的同系物都可以用酸性高锰酸钾溶液鉴别
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,浓度均为0.10mol·L-1、体积均为V0的MOH和ROH溶液,分别加水稀释至体积V,pH随lg![]() 的变化如图所示。下列叙述正确的是
的变化如图所示。下列叙述正确的是

A. MOH的电离程度:c点大于d点
B. ROH溶液由a点到b点时,  变大
变大
C. pH=10时,MOH和ROH溶液中,c(M+)>c(R+)
D. lg![]() =2时,MOH和ROH两种溶液中,水电离的c(OH-)的比值是1:10
=2时,MOH和ROH两种溶液中,水电离的c(OH-)的比值是1:10
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁分别为A、B、C、D四种短周期元素的最高价氧化物对应的水化物,已知0.1mol·L-1甲、丙、丁溶液的pH与A、C、D的原子序数关系如图所示(lg2=0.3),且常温下甲、丙、丁均可与乙反应。下列说法正确的是

A. 原子半径:A<B<C<D
B. A、B分别与D形成的化合物均为离子化合物
C. B、C的简单离子都会影响水的电离平衡
D. 乙在浓氨水中能溶解
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com