
【题目】以铬铁矿(含FeO·Cr2O3、Al2O3、SiO2等)为原料制备二草酸铬钾的实验步骤如下:
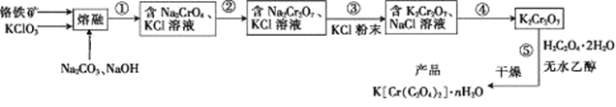
回答下列问题:
(1)若“熔融”在坩埚中进行,其材质可以是____(填“铁”、“陶瓷”或“SiO2”)。
(2) FeO·Cr2O3与KClO3及Na2CO3发生反应,生成Fe2O3、KCl、Na2CrO4和CO2的化学方程式为____________________________。
(3)熔融后的固体中含Na2CrO4、Fe2O3、Na2SiO3、NaAlO2、KCl等, 步骤①包含两次过滤操作:一是水浸后过滤;二是调节所得滤液pH为7~8,加热煮沸半小时,趁热过滤。第一次过滤滤渣中的主要成分为______,第二次过滤滤渣的主要成分为_________。
(4)步骤②需加入酸,则加入稀硫酸时发生反应的离子方程式为___________。
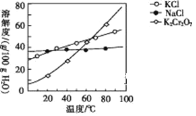
(5)步骤④包含的具体操作有_____、_____,过滤、洗涤,再经干燥得到K2Cr2O7晶体。(有关物质的溶解度曲线如图所示)
(6)已知K[Cr(C2O4)2]的相对分子质量为267。采用热重分析法测定K[Cr(C2O4)2]·nH2O样品所含结晶水数目,将样品加热到80 ℃时,失掉全部结晶水,失重16.8%。K[Cr(C2O4)2]·nH2O晶体中n=____。
【答案】铁 6FeO·Cr2O3+12Na2CO3+7KClO3![]() 12Na2CrO4+3Fe2O3+7KCl+12CO2↑ Fe2O3 Al(OH)3和H2SiO3 2CrO42-+2H+= Cr2O72-+H2O 蒸发浓缩 冷却结晶 3
12Na2CrO4+3Fe2O3+7KCl+12CO2↑ Fe2O3 Al(OH)3和H2SiO3 2CrO42-+2H+= Cr2O72-+H2O 蒸发浓缩 冷却结晶 3
【解析】
铬铁矿(含FeO·Cr2O3、Al2O3、SiO2等)为原料,加入氯酸钾、碳酸钠和氢氧化钠在坩埚中熔融发生氧化还原反应,熔融后的固体中含Na2CrO4、Fe2O3、Na2SiO3、NaAlO2、KCl等, 步骤①包含两次过滤操作:一是水浸后过滤,氧化铁不溶于水,其他物质都为钾盐和钠盐,都可溶于水,则第一次过滤滤渣中的主要成分为Fe2O3;根据步骤①最后得到的为氯化钾和铬酸钠,二是调节所得滤液pH为7~8,加热煮沸半小时,使Na2SiO3、NaAlO2转化为硅酸和氢氧化铝沉淀,趁热过滤。则第二次过滤滤渣的主要成分为Al(OH)3和H2SiO3;过滤后获得含有氯化钾和铬酸钠溶液,调节溶液pH值,加入适量的酸,使溶液中的铬酸钠转化为重铬酸钠,向溶液中氯化钾粉末,转化为重铬酸钾和氯化钠的混合溶液,利用重铬酸钾和氯化钠的溶解度不同,经过蒸发浓缩、冷却结晶、过滤、用无水乙醇对晶体洗涤,再经干燥得到K2Cr2O7晶体。
(1)熔融操作一般在坩埚中进行,由于熔融过程加入氢氧化钠和碳酸钠,高温下可与二氧化硅反应,故不能选用瓷坩埚或SiO2坩埚,应选用铁坩埚。
答案为:铁;
(2) 利用氧化还原反应得失电子守恒,化学方程式为6FeO·Cr2O3+12Na2CO3+7KClO3![]() 12Na2CrO4+3Fe2O3+7KCl+12CO2↑,
12Na2CrO4+3Fe2O3+7KCl+12CO2↑,
答案为:6FeO·Cr2O3+12Na2CO3+7KClO3![]() 12Na2CrO4+3Fe2O3+7KCl+12CO2↑;
12Na2CrO4+3Fe2O3+7KCl+12CO2↑;
(3)步骤①包含两次过滤操作:一是水浸后过滤,氧化铁不溶于水,其他物质都为钾盐和钠盐,都可溶于水,则第一次过滤滤渣中的主要成分为Fe2O3;根据步骤①最后得到的为氯化钾和铬酸钠,二是调节所得滤液pH为7~8,加热煮沸半小时,使Na2SiO3、NaAlO2转化为硅酸和氢氧化铝沉淀,趁热过滤。则第二次过滤滤渣的主要成分为Al(OH)3和H2SiO3;
答案为: Fe2O3;Al(OH)3和H2SiO3;
(4)根据分析,步骤②需加入酸,目的是在酸性条件下,使溶液中的铬酸钠转化为重铬酸钠,则加入稀硫酸时发生反应的离子方程式为2CrO42-+2H+= Cr2O72-+H2O ,
答案为:2CrO42-+2H+= Cr2O72-+H2O;
(5)如图所示,重铬酸钾和氯化钠在一定温度下的溶解度差别较大,经过蒸发浓缩、冷却结晶、过滤,可将重铬酸钾和氯化钠分离,再用无水乙醇对晶体洗涤,再经干燥得到K2Cr2O7晶体。
答案为:蒸发浓缩,冷却结晶;
(6) 已知K[Cr(C2O4)2]的相对分子质量为267。采用热重分析法测定K[Cr(C2O4)2]·nH2O样品所含结晶水数目,将样品加热到80 ℃时,失掉全部结晶水,失重16.8%,,相对分子质量在数值上等于摩尔质量,则失去的结晶水的摩尔质量分数=![]() =16.8%,解得n=3。
=16.8%,解得n=3。
答案为:3。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某同学利用如图装置进行喷泉实验,已知圆底烧瓶内充满X气体,胶头滴管内装有少量Y液体,烧杯内装有足量Z液体,下列组合能进行喷泉实验且最终液体一定能充满整个烧瓶的是( )
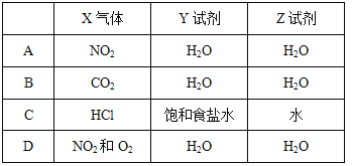
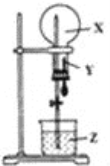
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z和W代表原子序数依次增大的四种短周期元素,它们满足以下条件:
①元素周期表中,Z与Y相邻,Z与W也相邻;②Y、Z和W三种元素的原子最外层电子数之和为17。
请填空:
(1)Y、Z和W是否位于同一周期(填“是”或“否”):__________,理由是________________。
(2)Y是_______,Z是_______,W是_______。
(3)X、Y、Z和W可组成一种化合物,其原子个数比为8∶2∶4∶1,写出该化合物的名称及化学式: _______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白黎芦醇具有抗氧化和预防心血管疾病的作用,下列有关白黎芦醇的说法正确的是( )

A.白黎芦醇能与NaHCO3溶液反应
B.分子中共含有7种化学环境不同的氢原子
C.1mol白黎芦醇最多能与7mol氢气加成
D.1mol白黎芦醇最多能反应溴水中的3.5mol Br2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国化学家首次实现了膦催化的(3+2)环加成反应,并依据该反应,发展了一条合成中草药活性成分茅苍术醇的有效路线。已知(3+2)环加成反应:![]()
![]() (
(![]() 、
、![]() 可以是
可以是![]() 或
或![]() )
)
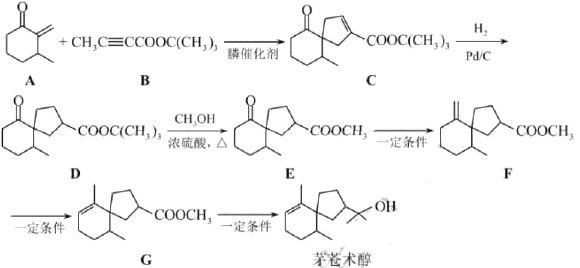
回答下列问题:
(1)茅苍术醇的分子式为____________,所含官能团名称为____________,分子中手性碳原子(连有四个不同的原子或原子团)的数目为____________。
(2)化合物B的核磁共振氢谱中有______个吸收峰;其满足以下条件的同分异构体(不考虑手性异构)数目为______。
①分子中含有碳碳叁键和乙酯基![]()
②分子中有连续四个碳原子在一条直线上
写出其中碳碳叁键和乙酯基直接相连的同分异构体的结构简式____________。
(3)![]() 的反应类型为____________。
的反应类型为____________。
(4)![]() 的化学方程式为________,除外该反应另一产物的系统命名为______
的化学方程式为________,除外该反应另一产物的系统命名为______
(5)下列试剂分别与和反应,可生成相同环状产物的是______(填序号)。
a.Br2 b.HBr c.NaOH溶液
(6)参考以上合成路线及条件,选择两种链状不饱和酯,通过两步反应合成化合物M,在方框中写出路线流程图(其他试剂任选)。_______
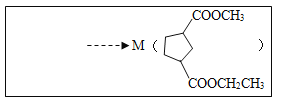
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】国际计量大会第26届会议修订了阿伏加德罗常数(NA=6.02214076×1023mol-1),于2019年5月2日正式生效。设NA是阿伏加德罗常数的值,下列说法正确的是
A.40g正丁烷和18 g异丁烷的混合物中共价键数目为13NA
B.常温常压下,124 g P4中所含P—P键数目为4NA
C.电解精炼铜时,阳极质量减小3.2g时,转移的电子数为0.1NA
D.0.1mol FeCl3完全水解转化为氢氧化铁胶体,生成胶粒数目为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】GaAs晶体的熔点很高, 硬度很大, 密度为ρ g·cm-3,Ga 和As 的摩尔质量分别为MGag·mol-1和MAs g·mol-1, 原子半径分别为rGa pm 和rAs pm, 阿伏加德罗常数值为NA, 其晶胞结构如下图所示, 下列说法错误的是
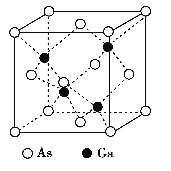
A. 该晶体为原子晶体
B. 在该晶体中,Ga和As均无孤对电子,Ga和As的配位数均为4
C. 原子的体积占晶胞体积的百分率为![]()
D. 所有原子均满足8电子稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知SO2通入BaCl2溶液无明显现象。某同学利用如图装置探究SO2与BaCl2溶液反应生成白色沉淀的条件。下列判断正确的是
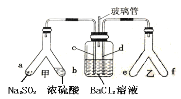
A.e、f两管中的试剂可以分别是浓氨水和NaOH固体
B.乙中产生的一定为氧化性气体,将BaSO3氧化为BaSO4沉淀
C.玻璃管的作用是连通大气,使空气中的氧气进入广口瓶,参与反应
D.c、d两根导管都必须插入BaCl2溶液中,保证气体与Ba2+充分接触
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Z、Q、R、T、U分别代表原子序数依次增大的短周期元素,在周期表的短周期主族元素中,X的原子半径最小,X与R的最外层电子数相等;Z的内层电子数是最外层电子数的一半;U的最高化合价和最低化合价的代数和为6;R和Q可形成原子个数之比为1:1和2:1的两种化合物;T与Z同主族。请回答下列问题:
(1)T元素在周期表中的位置是________________________。
(2)X、Z、Q三种元素的原子半径由小到大的顺序为___________(填元素符号)。
(3)R、T两元素最高价氧化物对应的水化物反应的化学方程式为____________。
(4)某同学用X、R两元素的单质反应生成固体物质RX,RX属于离子化合物,且能与化合物X2Q反应生成X的单质。
①RX的电子式为_____________;RX与X2Q反应的化学方程式为___________。
②该同学认为取X、R两元素的单质反应后的固体物质与X2Q反应,若能产生![]() 的单质,即可证明得到的固体物质一定是纯净的RX。请判断该方法是否合理并说明理由:_____________。
的单质,即可证明得到的固体物质一定是纯净的RX。请判断该方法是否合理并说明理由:_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com