
| ||
| △ |
| A、氧化剂 |
| B、还原剂 |
| C、既是氧化剂又是还原剂 |
| D、既不是氧化剂又不是还原剂 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、n=m+1 |
| B、n=m+8 |
| C、n=m+11 |
| D、n=m+25 |
查看答案和解析>>
科目:高中化学 来源: 题型:
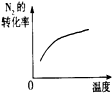
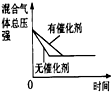
| A | B | C | D | |
| 研究目的 | 压强对反应的影响(P1>P2) | 温度对反应的影响 | 平衡体系增加N2对反应的影响 | 催化剂对反应的影响 |
| 图示 |  |
 |
 |
 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图是以石墨为电极电解CuCl2溶液的装置示意图.
如图是以石墨为电极电解CuCl2溶液的装置示意图.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、②③ | C、①③ | D、②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
7 14 |
4 2 |
17 8 |
1 1 |
A、
 | ||
| B、氦气分子为双原子分子 | ||
C、一个H2
| ||
D、C
 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(Na+)>c (H+)>c (CH3COO-)>c (OH-) |
| B、c (Na+)>c (CH3COO-)>c (OH-)>c (H+) |
| C、c (Na+)+c (H+)=c (OH-)+c (CH3COO-) |
| D、c (Na+)=c (OH-)>c (CH3COO-)=c (H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HCHO |
| B、CO |
| C、SO2 |
| D、CH3CH2CH3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com