
【题目】下面有关晶体的叙述中,不正确的是
A. 氯化铯晶体中,每个Cs+周围紧邻8个Cl-
B. SiO2晶体为空间网状结构,由共价键形成的原子环中,最小的环上有12个原子
C. 干冰晶体中,每个CO2分子周围紧邻12个CO2分子
D. 金属铜属于六方最密堆积结构,金属镁属于面心立方最密堆积结构
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】“绿色化学实验”已走进课堂,下列做法符合“绿色化学”的是( )
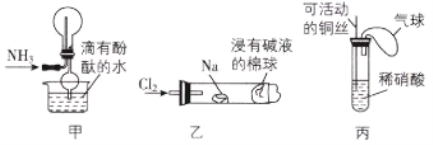
①实验室收集氨气采用图甲所示装置
②实验室中做氯气与钠反应的实验时采用图乙所示装置
③实验室中用玻璃棒分别蘸取浓盐酸和浓氨水做氨气与酸生成铵盐的实验
④实验室中采用图丙所示装置进行铜与稀硝酸的反应
A.②③④B.①②③C.①②④D.①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化亚铜(CuCl)广泛应用于冶金工业,也用作催化剂和杀菌剂。以硫化铜精矿为原料生产CuCl的工艺如下:
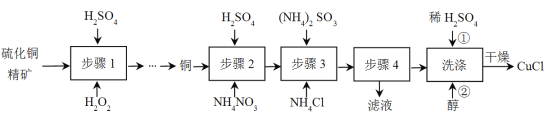
已知CuCl难溶于醇和水,溶于c(Cl-)较大的体系[CuCl(s)+Cl-![]() CuCl2-],潮湿空气中易水解氧化。
CuCl2-],潮湿空气中易水解氧化。
(1)步骤1开始前需要对硫化铜精矿进行粉碎,目的是______;
(2)步骤1是“氧化酸浸”的过程,该过程生成蓝色溶液和浅黄色沉淀,化学方程式是__________________________________;
(3)步骤2是溶解过程,溶解时反应的离子方程式______;
(4)步骤3为主反应,Cu+的沉淀率与加入的NH4Cl的量关系如图所示。
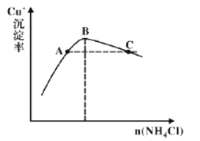
①反应的氧化产物是______;
②比较c(Cu+)相对大小:A点______C点(填“>”、“<”或“=”);
③提高C点状态混合物中Cu+沉淀率的措施是______;
(5)步骤4进行的实验操作是______;
(6)洗涤过程中不能用硝酸代替硫酸进行“酸洗”,理由是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年为“国际化学元素周期表年”。如图所示是元素周期表的一部分,W、X、Y、Z为短周期主族元素,W与X的最高化合价之和为8。下列说法不正确的是
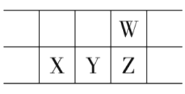
A.原子半径:W<X
B.气态氢化物热稳定性:Z<W
C.Y单质可用做半导体材料
D.X的最高价氧化物的水化物是强碱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Li4Ti5O12和LiFePO4都是锂离子电池的电极材料,可利用钛铁矿(主要成分为FeTiO3,还含有少量MgO、SiO2等杂质)来制备,工艺流程如下:
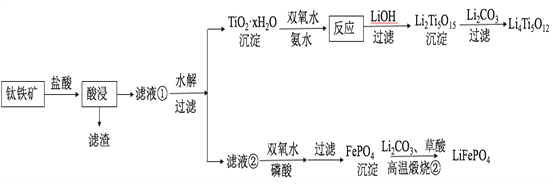
回答下列问题:
(1)“酸浸”实验中,铁的浸出率结果如下图所示。由图可知,当铁的净出率为70%时,所采用的实验条件为___________________。
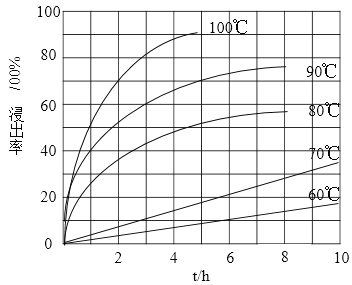
(2)“酸浸”后,钛主要以TiOCl42-形式存在,写出相应反应的离子方程式__________________。
(3)TiO2·xH2O沉淀与双氧水、氨水反应40 min所得实验结果如下表所示:
温度/℃ | 30 | 35 | 40 | 45 | 50 |
TiO2·xH2O转化率% | 92 | 95 | 97 | 93 | 88 |
分析40℃时TiO2·xH2O转化率最高的原因__________________。
(4)Li2Ti5O15中Ti的化合价为+4,其中过氧键的数目为__________________。
(5)若“滤液②”中c(Mg2+)=0.02 mol/L,加入双氧水和磷酸(设溶液体积增加1倍),使Fe3+恰好沉淀完全即溶液中c(Fe3+)=1×10-5 mol/L,此时是否有Mg3(PO4)2沉淀生成?___________(列式计算)。
FePO4、Mg3(PO4)2的Ksp分别为1.3×10-22、1.0×10-24。
(6)写出“高温煅烧②”中由FePO4制备LiFePO4的化学方程式______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下列填空。
(1) 原子序数为24的元素基态原子核外有________个未成对电子,电子占据的最高能层符号为______,该能层具有的原子轨道数为________;
(2)B元素基态原子中能量最高的电子其电子云在空间有___个伸展方向,原子核外有___个运动状态不同的电子。
(3)在下列物质中:①NH3 ②I2 ③CH4 ④Na2O2 ⑤H2O2 ⑥CO2 ⑦NaOH ⑧CH3COONH4,既存在非极性键又存在极性键的极性分子是__________;既存在σ键又存在π键的非极性分子是________,既存在σ键又存在π键的离子晶体是________
(4)1mol NH4BF4含有___mol配位键, 1mol [Zn(CN)4]2-中含有σ键的数目为___.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种生产高氯酸(HClO4)的工艺流程如图所示,该流程同时产出重要含氯消毒剂(ClO2)和漂白剂亚氯酸钠(NaClO2):
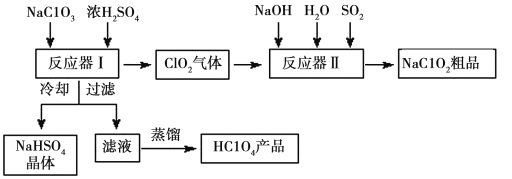
已知:①NaHSO4溶解度随温度的升高而增大,适当条件下可结晶析出。
②高氯酸是一种强酸,沸点130℃左右。.
请回答下列问题:
(1)完成反应器1中生成高氯酸的化学方程式:NaClO3+H2SO4=HClO4+__ClO2↑+NaHSO4+![]() ___。冷却的目的是__,能用蒸馏法分离出高氯酸的原因是___。
___。冷却的目的是__,能用蒸馏法分离出高氯酸的原因是___。
(2)反应器II中发生反应的离子方程式为___。
(3)通入反应器II中的SO2用H2O2代替同样能生成NaClO2,请简要说明H2O2能代替SO2的原因是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化白藜芦醇W具有抗病毒等作用。下面是利用Heck反应合成W的一种方法:
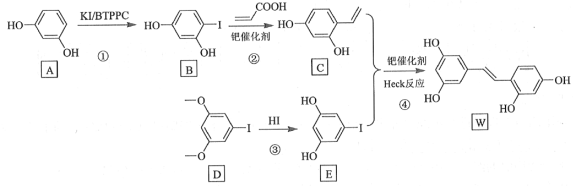
回答下列问题:
(1)A的化学名称为___________。
(2)![]() 中的官能团名称是___________。
中的官能团名称是___________。
(3)反应③的类型为___________,W的分子式为___________。
(4)不同条件对反应④产率的影响见下表:
实验 | 碱 | 溶剂 | 催化剂 | 产率/% |
1 | KOH | DMF | Pd(OAc)2 | 22.3 |
2 | K2CO3 | DMF | Pd(OAc)2 | 10.5 |
3 | Et3N | DMF | Pd(OAc)2 | 12.4 |
4 | 六氢吡啶 | DMF | Pd(OAc)2 | 31.2 |
5 | 六氢吡啶 | DMA | Pd(OAc)2 | 38.6 |
6 | 六氢吡啶 | NMP | Pd(OAc)2 | 24.5 |
上述实验探究了________和________对反应产率的影响。此外,还可以进一步探究________等对反应产率的影响。
(5)X为D的同分异构体,写出满足如下条件的X的结构简式________________。
①含有苯环;②有三种不同化学环境的氢,个数比为6∶2∶1;③1 mol的X与足量金属Na反应可生成2 g H2。
(6)利用Heck反应,由苯和溴乙烷为原料制备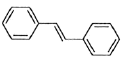 ,写出合成路线________________。(无机试剂任选)
,写出合成路线________________。(无机试剂任选)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com