
【题目】称取14.2 g 无水硫酸钠固体(摩尔质量为142 g/mol)溶于适量水中,再稀释至100 mL。回答下列问题:
(1)从配制所得的溶液中取出50 mL,该50 mL的溶液中硫酸钠的物质的量浓度为:___________
(2)写出硫酸钠在水溶液中的电离方程式:________。
(3)14.2 g该固体中含有钠离子的数目是:__________。
【答案】1 mol/L Na2SO4=2Na++SO42- 1.204×1023(或0.2NA)
【解析】
(1)先根据n=![]() 计算硫酸钠的物质的量,再根据物质的量浓度公式c=
计算硫酸钠的物质的量,再根据物质的量浓度公式c=![]() 计算溶液的物质的量浓度,利用溶液浓度的均一性,所取溶液浓度与原溶液浓度一样,与所取溶液的体积大小无关;
计算溶液的物质的量浓度,利用溶液浓度的均一性,所取溶液浓度与原溶液浓度一样,与所取溶液的体积大小无关;
(2)硫酸钠是强电解质,能完全电离出钠离子和硫酸根离子,据此书写电离方程式;
(3)然后根据溶质的分子式与其电离产生离子的关系结合N=n·NA计算离子的数目。
(1)硫酸钠的物质的量n(Na2SO4)=![]() =0.1 mol,则该溶液的物质的量浓度c=
=0.1 mol,则该溶液的物质的量浓度c=![]() =1 mol/L,从配制所得的溶液中取出50 mL,由于溶液具有均一性,即溶液的各处浓度相同,与溶液的体积无关,所以该50 mL的溶液中硫酸钠的物质的量浓度为1 mol/L;
=1 mol/L,从配制所得的溶液中取出50 mL,由于溶液具有均一性,即溶液的各处浓度相同,与溶液的体积无关,所以该50 mL的溶液中硫酸钠的物质的量浓度为1 mol/L;
(2)Na2SO4是盐,属于强电解质,完全电离产生Na+、SO42-,所以其电离方程式为:Na2SO4=2Na++SO42-;
(3)硫酸钠的物质的量n(Na2SO4)=![]() =0.1 mol,1个Na2SO4电离产生2个Na+、1个SO42-,所以14.2 g该固体中含有钠离子的数目N(Na+)=0.1 mol×2×6.02×1023/mol=1.204×1023。
=0.1 mol,1个Na2SO4电离产生2个Na+、1个SO42-,所以14.2 g该固体中含有钠离子的数目N(Na+)=0.1 mol×2×6.02×1023/mol=1.204×1023。


科目:高中化学 来源: 题型:
【题目】汉黄芩素是传统中草药黄芩的有效成分之一,对肿瘤细胞的杀伤有独特作用。下列有 关汉黄芩素的叙述正确的是
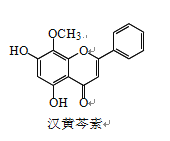
A. 汉黄芩素的分子式为 C16H13O5
B. 该物质遇 FeCl3 溶液显色
C. 1 mol 该物质与溴水反应,最多消耗 1 mol Br2
D. 与足量 H2 发生加成反应后,该分子中官能团的种类减少 1 种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,下列溶液的离子浓度关系式正确的是
A. pH=5的H2S溶液中,c(H+)= c(HS-)=1×10—5mol·L—1
B. pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1
C. pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合:c(Na+)+ c(H+)= c(OH-)+c( HC2O4-)
D. pH相同的①CH3COO Na②NaHCO3③NaClO三种溶液的c(Na+):①>②>③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在化学课上围绕浓硫酸的化学性质进行了如下实验探究,将适量的蔗糖放入烧杯中,加入少量水,搅拌均匀,然后加入浓硫酸,快速搅拌,生成疏松多孔的黑色物质。
(1)  (2)
(2)  (3)
(3)  (4)
(4)  (5)
(5) 
请回答下列问题:
①根据上述实验步骤(1)-(5)中,蔗糖与浓硫酸反应的实验现象,浓硫酸表现出的化学性质有____________ (填字母)。
A.酸性 B.吸水性 C.脱水性 D.强氧化性
②反应中生成的黑色物质继续与浓硫酸作用,产生两种气体,其中一种气体 X 有刺激性气味,另一种气体 Y 无色无味,写出反应的化学方程式_____________。
③为了在混合气体中检验出 X、Y 这两种气体,提供下列试剂:(试剂可多次使用,不考虑尾气处理)
A.品红溶液 B.澄清石灰水 C.酸性高锰酸钾溶液 D.氢氧化钠溶液
气体通过的顺序依次是:____________→____________→____________→____________ (填字母)。证明有气体 Y 存在的实验现象为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】30 mL1 mol·L-1NaCl溶液和40 mL0.5 mol·L-1CaCl2溶液混合后,混合液中Cl-浓度为(假设溶液体积混合前后不变)( )
A.0.5 mol·L-1B.0.6 mol·L-1C.1.0 mol·L-1D.2 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验的说法正确的是( )
A.向![]() 溶液中滴入用硫酸酸化的
溶液中滴入用硫酸酸化的![]() 溶液,溶液变黄,说明发生氧化还原反应,且氧化性:
溶液,溶液变黄,说明发生氧化还原反应,且氧化性:![]()
B.为测定熔融氢氧化钠的导电性,可在瓷坩埚中熔化氢氧化钠固体后进行测量
C.制备氢氧化铁胶体通常是将饱和氯化铁溶液煮沸,直至呈红褐色,停止加热
D.在饱和![]() 溶液中加入一定量
溶液中加入一定量![]() ,充分反应后恢复到原温度,有晶体析出,溶液质量不变
,充分反应后恢复到原温度,有晶体析出,溶液质量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国科学技术大学的钱逸泰教授等以![]() 和金属钠为原料,在700℃时反应制造出纳米级金刚石粉末和另一种化合物,该成果发表在世界权威的《科学》杂志上,被科学家们高度评价为“稻草变黄金”。下列有关说法中,你认为错误的是( )
和金属钠为原料,在700℃时反应制造出纳米级金刚石粉末和另一种化合物,该成果发表在世界权威的《科学》杂志上,被科学家们高度评价为“稻草变黄金”。下列有关说法中,你认为错误的是( )
A.![]() 的还原性强于金刚石B.另一种化合物是
的还原性强于金刚石B.另一种化合物是![]()
C.纳米级金刚石粉末可以透过半透膜D.这个反应是氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,某一元弱酸HA的电离常数K=1.6×10-6。向20.00mL浓度约为0.1mol·L-1 HA溶液中逐滴加入0.1000mol·L-1的标准NaOH溶液,其pH变化曲线如图所示(忽略温度变化)。请回答下列有关问题:
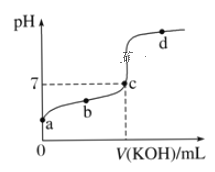
(1)a、b、c、d四点中水的电离程度最大的是_______点,滴定过程中宜选用__________作指示剂,滴定终点在__________(填“c点以上”或“c点以下”)。
(2)滴定过程中部分操作如下,下列各操作使测量结果偏高的是_____(填字母序号)。
A.滴定前碱式滴定管未用标准NaOH溶液润洗
B.用蒸馏水洗净锥形瓶后,立即装入HA溶液后进行滴定
C.滴定过程中,溶液出现变色后,立即停止滴定
D.滴定结束后,仰视液面,读取NaOH溶液体积
(3)若重复三次滴定实验的数据如下表所示,计算滴定所测HA溶液的物质的量浓度为_____mol/L。(保留4位有效数字)
实验序号 | NaOH溶液体积/mL | 待测HA溶液体积/mL |
1 | 21.01 | 20.00 |
2 | 20.99 | 20.00 |
3 | 21.60 | 20.00 |
(4)a点溶液中pH约为________,此时溶液中H2O电离出的c(H+)为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A.1 mol/L的BaCl2溶液中含Cl-的数目为2NA
B.常温常压下,28 g N2中所含电子数目为10NA
C.标准状况下,4.48 L CH4中所含原子数目为NA
D.2 mol Al与足量盐酸完全反应,转移电子数目为3NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com