
【题目】地震灾区的水需用杀菌消毒剂处理后才能确保饮水安全。救灾物资中的一瓶“84消毒液”的包装说明上有如下信息:含25%NaClO(次氯酸钠)、1000mL、密度1.19gcm-3,稀释100倍(体积比)后使用。
请回答下列问题:
(1)上述“84消毒液”的物质的量浓度为______molL-1。
(2)该同学取100mL上述“84消毒液”,稀释后用于消毒,稀释100倍后的溶液中c(Na+)=______molL-1(假设稀释后溶液密度为1.0gcm-3),该消毒液长时间放置在空气中能吸收标准状况下CO2的体积为______L。
(3)灾区志愿者根据上述“84消毒液”的包装说明,欲用NaClO固体(NaClO易吸收空气中的H2O、CO2)配制480mL含25%NaClO的消毒液。下列说法正确的是______。
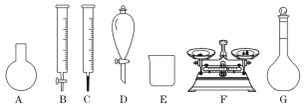
a.如图所示的仪器中,有四种是不需要的,还需一种玻璃仪器
b.容量瓶用蒸馏水洗净后,要烘干才能用于溶液的配制
c.利用购买的商品NaClO来配制可能会导致结果偏低
d.需要NaClO固体的质量为143g
【答案】4.0 0.04 8.96 c
【解析】
根据溶质的质量分数计算物质的量浓度;根据反应方程式及气体摩尔体积计算消耗气体的体积;根据一定物质的浓度溶液的配置原理分析配置所需仪器、误差分析等。
(1)则c(NaClO)=![]() ,故答案为 :4.0;
,故答案为 :4.0;
(2)根据稀释前后溶质的物质的量不变,则100mL×4.0molL-1=10000mL×c(NaClO),
解得稀释后c(NaClO)≈0.04molL-1,c(Na+)=c(NaClO)≈0.04molL-1;根据NaClO+CO2+H2O=NaHCO3+HClO,可知,n(CO2)=n(NaClO)=0.4mol ,标准状况下二氧化碳的体积的体积为0.4mol×22.4L/mol= 8.96L,故答案为:0.04;8.96;
(3)a.需用托盘天平称量NaClO固体,需用烧杯来溶解NaClO,需用玻璃棒进行搅拌和引流,需用容量瓶和胶头滴管来定容,图示的a、b、c、d不需要,但还需玻璃棒和胶头滴管,故a错误;
b.配制过程中需要加入水,所以经洗涤干净的容量瓶不必烘干后再使用,故b错误;
c.由于NaClO易吸收空气中的H2O、CO2而变质,所以商品NaClO可能部分变质导致NaClO减少,配制的溶液中溶质的物质的量减小,结果偏低,故c正确;
d.应选取500mL的容量瓶进行配制,然后取出480mL即可,所以需要NaClO的质量:0.5L×4.0molL-1×74.5gmol-1=149g,故d错误;故答案为:c。


 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:高中化学 来源: 题型:
【题目】下面a~f是中学化学实验中常见的几种仪器:
a 量筒 b 容量瓶 c 托盘天平 d 温度计 e 分液漏斗
(1)标出仪器使用温度的是________(填写编号)。
(2)使用前需要检查是否漏水的是________(填写编号)。
(3)称取10.5 g固体样品(1 g以下使用游码)若样品与砝码错放位置,则实际称取的样品质量为________ g。
(4)在某次实验中,要用500mL 0.52mol·L-1的NaOH溶液, 配制此浓度NaOH溶液时需用的主要仪器有托盘天平(附砝码、镊子)、药匙、量筒、烧杯、玻璃棒、_________和___________;
(5)下列操作使所配物质的量浓度偏大的有__________(填写字母)。
A 称量时用了生锈的砝码;
B 将NaOH放在托盘天平的右盘上称量(使用游码);
C NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中;
D 往容量瓶转移时,有少量液体溅出;
E 定容时俯视刻度线;
F 容量瓶未干燥即用来配制溶液;
G 定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线
(6) 实验室用密度为1.25g·mL-1,质量分数为36.5%的浓盐酸配制240mL0.1mol ·L-1的盐酸.
请回答下列问题:
(1)浓盐酸的物质的量浓度为________。
(2)配制240mL 0.1mol·L-1的盐酸应量取浓盐酸体积______mL,应选用容量瓶的规格是______mL.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以CO2和Na2O2为原料,制取纯净干燥的O2,实验装置如下( )

下列说法正确的是
A. 装置②中试剂为碱石灰
B. 装置③的作用是除去二氧化碳和水
C. .收集氧气应选择装置a
D. 装置②、③之间应增加盛澄清石灰水的洗气瓶,以确认氧气中二氧化碳已经除尽
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25°C向![]() 中滴加
中滴加![]() 过程中,
过程中,![]() 变化如图所示。
变化如图所示。

(1)A点溶液![]() ,用化学用语解释原因:_________________。
,用化学用语解释原因:_________________。
(2)下列有关B点溶液的说法正确的是_______________(填字母序号)。
a. 溶质为:![]()
b. 微粒浓度满足:![]()
c. 微粒浓度满足:![]()
(3)![]() 两点水的电离程度:
两点水的电离程度:![]() ______
______![]() (填“
(填“![]() ”、“
”、“ ![]() ”或“
”或“![]() ”)。
”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2Cu(IO3)2+24KI+12H2SO4=2CuI![]() (碘化亚铜)+13I2+12K2SO4+12H2O,下列说法正确的是 ( )
(碘化亚铜)+13I2+12K2SO4+12H2O,下列说法正确的是 ( )
A.Cu(IO3)2作氧化剂,Cu(IO3)2中只有碘元素被还原
B.CuI既是氧化产物又是还原产物
C.每生成1mol CuI,有11mol KI发生氧化反应
D.每转移1.1mol电子,有0.2mol IO3-被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式中,不正确的是( )
A. 侯氏制碱法:![]()
B. 向![]() 溶液中滴加
溶液中滴加![]() 溶液:
溶液:![]()
C. 氧化铁与足量的![]() 溶液反应:
溶液反应:![]()
D. 已知酸性的强弱:![]() ,则向
,则向![]() 溶液中通入少量的
溶液中通入少量的![]() 时:
时:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A(g)+B(g) ![]() C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
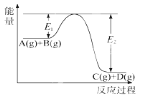
(1)该反应是________反应(填“吸热”、“放热”)。
(2)当反应达到平衡时,升高温度,A的转化率________(填“增大”、“减小”或“不变”),原因是________。
(3)反应体系中加入催化剂对反应热是否有影响_______(填“有”、“无”)。
(4)在反应体系中加入催化剂,反应速率增大,此时E1______,E2_______(填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、R、Q、M是六种原子序数依次增大的短周期主族元素,X是原子半径最小的元素,Y的气态氢化物能使湿润的红色石蕊试纸变蓝,Z的单质是空气的主要成分之一,R、Q、M三种元素的最高价氧化物对应的水化物相互之间均可反应,M的单质是黄绿色气体。请回答下列问题:
(1)Z和M的非金属性强弱Z_________M(填“<”“>”或“=”)。
(2)Z、Q、M简单离子半径由大到小的顺序为__________________(用离子符号表示)。
(3)X和Z两元素形成的原子个数比为1∶1的化合物电子式为___________。
(4)Y元素的气态氢化物与其最高价氧化物对应的水化物反应的化学方程式为______________,所生成的物质水溶液中离子浓度由大到小的顺序为_______________。
(5)![]() 是一种高效安全的杀菌消毒剂,它能将电镀废水中的
是一种高效安全的杀菌消毒剂,它能将电镀废水中的![]() 氧化为两种无毒的气体,自身还原成最低价的简单离子,写出该反应的离子方程式___________________________。
氧化为两种无毒的气体,自身还原成最低价的简单离子,写出该反应的离子方程式___________________________。
(6)用电解法可制备![]() ,电解总反应为
,电解总反应为![]() 。已知阳极产物为
。已知阳极产物为![]() ,该物质在水中水解生成
,该物质在水中水解生成![]() 和
和![]() ,则该电极生成
,则该电极生成![]() 的电极反应为________________。
的电极反应为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】维生素 C(又名抗坏血酸,分子式为 C6H8O6)具有较强的还原性,放置在空气中易被氧化,其质量分数可通过在弱酸性溶液中用已知物质的量浓度的 I2 溶液进行测定。该反应 的化学方程式如下:C6H8O6+ I2 = C6H6O6 +2HI。现欲测定某样品中维生素 C 的质量分 数,具体的步骤及测得的数据如下:取10mL6mol/LCH3COOH(提供酸性环境),加入100 mL 蒸馏水,将溶液加热煮沸后放置冷却。精确称取 0.2000g 样品,溶解于上述冷却的 溶液中,立即用物质的量浓度为 0.05000 mol/L 的 I2 溶液进行反应,刚好完全反应时共消耗21.00 mL I2 溶液。
(1)CH3COOH 稀溶液要先经煮沸、冷却后才能使用,煮沸的是为了赶走溶液在溶液中的_____(填物质的化学式)
(2)样品中维生素 C 的质量分数为______。计算过程
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com