
【题目】下列离子方程式中,不正确的是( )
A. 侯氏制碱法:![]()
B. 向![]() 溶液中滴加
溶液中滴加![]() 溶液:
溶液:![]()
C. 氧化铁与足量的![]() 溶液反应:
溶液反应:![]()
D. 已知酸性的强弱:![]() ,则向
,则向![]() 溶液中通入少量的
溶液中通入少量的![]() 时:
时:![]()
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】2008年9月,中国爆发三鹿婴幼儿奶粉受污染事件,导致食用了受污染奶粉的婴幼儿产生肾结石病症,其原因是奶粉中含有三聚氰胺.三聚氰胺的分子式为C3N3(NH2)3下列有关三聚氰胺的说法不正确的是( )
A.三聚氰胺的摩尔质量为126
B.三聚氰胺中C、N、H的原子个数比为1:2:2
C.三聚氰胺中C、N两种元素的质量比为3:7
D.三聚氰胺中氮元素的质量分数约为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于古籍中的记载说法不正确的是( )
A. 《吕氏春秋·别类编》中“金(即铜)柔锡柔,合两柔则刚”,体现了合金硬度方面的特征
B. 《天工开物》中有“至于矾现五金色之形,硫为群石之将,皆变化于烈火”,其中的矾指的是金属硫化物
C. 《本草纲目》中记载:“此即地霜也。所在山泽,冬月地上有霜,扫取以水淋汁,后乃煎炼而成。”文中对硝酸钾的提取涉及溶解、蒸发、结晶操作
D. 《清嘉录》中记载:“研雄黄末,屑蒲根,和酒饮之,谓之雄黄酒。”其中的雄黄是![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】地震灾区的水需用杀菌消毒剂处理后才能确保饮水安全。救灾物资中的一瓶“84消毒液”的包装说明上有如下信息:含25%NaClO(次氯酸钠)、1000mL、密度1.19gcm-3,稀释100倍(体积比)后使用。
请回答下列问题:
(1)上述“84消毒液”的物质的量浓度为______molL-1。
(2)该同学取100mL上述“84消毒液”,稀释后用于消毒,稀释100倍后的溶液中c(Na+)=______molL-1(假设稀释后溶液密度为1.0gcm-3),该消毒液长时间放置在空气中能吸收标准状况下CO2的体积为______L。
(3)灾区志愿者根据上述“84消毒液”的包装说明,欲用NaClO固体(NaClO易吸收空气中的H2O、CO2)配制480mL含25%NaClO的消毒液。下列说法正确的是______。
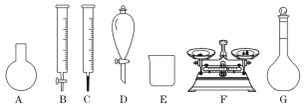
a.如图所示的仪器中,有四种是不需要的,还需一种玻璃仪器
b.容量瓶用蒸馏水洗净后,要烘干才能用于溶液的配制
c.利用购买的商品NaClO来配制可能会导致结果偏低
d.需要NaClO固体的质量为143g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语书写正确的是
A.镁离子的结构示意图: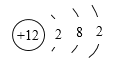
B.12C和13C互为同位素
C.H2SO4 电离:H2SO4=H2++SO42-
D.NaOH电离:NaOH=Na++O2-+H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将甘油![]() 转化为高附加值产品是当前的热点研究方向,如甘油和水蒸气、氧气经催化重整或部分催化氧化可制得
转化为高附加值产品是当前的热点研究方向,如甘油和水蒸气、氧气经催化重整或部分催化氧化可制得![]() ,反应过程如下:
,反应过程如下:
反应Ⅰ |
| 甘油水蒸气重整 |
反应Ⅱ |
| 甘油部分氧化 |
反应Ⅲ |
| 甘油氧化水蒸气重整 |
下列说法正确的是( )
A. ![]() B. 消耗等量的甘油,反应Ⅲ的放热效果最显著
B. 消耗等量的甘油,反应Ⅲ的放热效果最显著
C. 消耗等量的甘油,反应的产氢率最高D. 甘油不溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】FeSO4·7H2O在医学上常用作补血剂。某课外小组通过用KMnO4滴定已配好的FeSO4溶液来测定某补血剂中FeSO4的含量。实验室需配制0.01 mol/L 1000 mL的KMnO4溶液。
(1)需要的玻璃仪器有烧杯、_______ 、_______ 、_______。
(2)用托盘天平称取KMnO4固体的质量为_______g。
(3)下列操作使实验结果偏大的是 _______。
A.容量瓶未干燥 B.未洗涤烧杯和玻璃棒
C.定容时俯视容量瓶刻度线 D.在烧杯溶解时,有少量液体溅出
(4)现测定补血剂中FeSO4的含量,实验步骤如下:
a.取8片补血剂样品除去糖衣、研磨、溶解、过滤,将滤液配制成250 mL溶液
b.取上述溶液25 mL于锥形瓶中,加入少量硫酸酸化,逐渐滴加0.01 mol/L的KMnO4溶液,反应为10 FeSO4+2KMnO4+8H2SO4=5Fe2(SO4)3 +2MnSO4+K2SO4+8H2O。记录滴定终点时消耗KMnO4溶液的体积(假定药品中其他成分不与KMnO4反应)。
c.重复步骤b 2-3次,平均消耗KMnO4溶液20.00 mL。
该补血剂中FeSO4的含量为 _______ mg/片(写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】稀土元素是元素周期表中第IIIB族钪、钇和镧系元素的总称。第三代永磁体材料——钕铁硼(NdFeB)因其优异的综合磁性能,被广泛应用于计算机、通信信息等高新技术产业。回答下列问题:
(1)基态Fe原子的价电子排布式为____;铁、钴、镍元素性质非常相似,原子半径接近但依次减小,NiO、FeO的晶体结构类型与氯化钠相同,则晶格能NiO____(填“>”“<”或“=”)FeO。
(2)氨硼烷化合物(![]() )是一种新型化学储氢材料,与该化合物分子互为等电子体的有机物为___(填化学式);氨硼烷分子中N、B原子的杂化方式分别为___、___。
)是一种新型化学储氢材料,与该化合物分子互为等电子体的有机物为___(填化学式);氨硼烷分子中N、B原子的杂化方式分别为___、___。
(3)![]() 俗称摩尔盐,相对于
俗称摩尔盐,相对于![]() 而言,摩尔盐不易失水,不易被空气氧化,在化学分析实验中常用于配制Fe(II)的标准溶液,试分析硫酸亚铁铵晶体中亚铁离子稳定存在的原因。______
而言,摩尔盐不易失水,不易被空气氧化,在化学分析实验中常用于配制Fe(II)的标准溶液,试分析硫酸亚铁铵晶体中亚铁离子稳定存在的原因。______
(4)钕是最活泼的稀土金属之一,晶体为六方晶系,钕原子以六方最密堆积方式连接。晶胞参数:![]() 。每个晶胞含有___个钕原子,设阿伏加德罗常数为
。每个晶胞含有___个钕原子,设阿伏加德罗常数为![]() ,则金属钕的密度为___
,则金属钕的密度为___![]() (Nd的相对原子质量为M,列出计算表达式)
(Nd的相对原子质量为M,列出计算表达式)

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com