
【题目】短周期元素R、T、Q、W在元素周期表中的相对位置如下图所示,其中 T 所处的周期序数与族序数相等。下列判断不正确的是
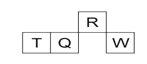
A. 最简单气态氢化物的热稳定性:R > Q
B. 含 T 的盐溶液一定显酸性
C. 原子半径:T > Q > R
D. 最高价氧化物对应水化物的酸性:Q < W
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】物质X的结构简式如图所示,它常被用于制香料或作为饮料的酸化剂,在医学上也有广泛用途.下列关于物质X的说法正确的是( )
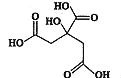
A.X的分子式为C6H7O7
B.1 mol物质x最多可以和3 mol氢气发生加成反应
C.X分子内所有原子均在同一平面内
D.足量的X分别与等物质的量的NaHCO3、Na2CO3反应得到的气体的物质的量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】药物贝诺酯可由乙酰水杨酸和对乙酰氨基酚在一定条件下反应制得:
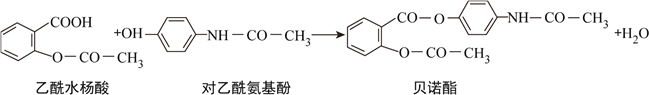
下列有关叙述正确的是( )
A. 贝诺酯分子中有三种含氧官能团
B. 可用FeCl3溶液区别乙酰水杨酸和对乙酰氨基酚
C. 乙酰水杨酸和对乙酰氨基酚均能与NaHCO3溶液反应
D. 贝诺酯与足量NaOH溶液共热,最终生成乙酰水杨酸钠和对乙酰氨基酚钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(6分)
(1)有机化学中取代反应范畴很广。下列6个反应中,属于取代反应范畴的是(填写相应的字母)
A.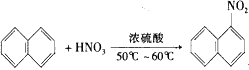 +H2O
+H2O
B.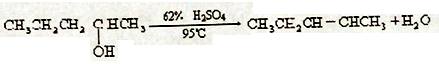
C.2CH3CH2OH ![]() CH3CH2OCH2CH3 + H2O
CH3CH2OCH2CH3 + H2O
D.(CH3)2CHCH=CH2 + 2HI![]()
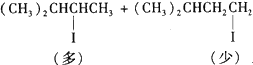
E.CH3COOH+CH3OH![]() CH3COOCH3+H2O
CH3COOCH3+H2O
F.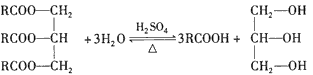 [式中R为正十七烷基CH3(CH2)15CH2-]
[式中R为正十七烷基CH3(CH2)15CH2-]
(2)Nomex纤维是一种新型阻燃性纤维。它可由间苯二甲酸和间苯二胺在一定条件下以等物质的量缩聚合成.请把Nomex纤维结构简式写在下面的方框中
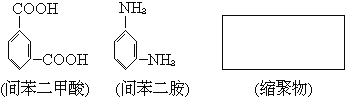
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷单质及其化合物有广泛应用。
(1)三聚磷酸可视为三个磷酸分子之间脱去两个水分子的产物,三聚磷酸钠(俗称“磷酸五钠”)是常用的水处理剂,其化学式为___________________。
(2)次磷酸钠(NaH2PO2)可用于化学镀镍。
①NaH2PO2中P元素的化合价为____________。
②化学镀镍的溶液中含有Ni2+和H2PO![]() ,在酸性条件下发生下述反应,请配平:
,在酸性条件下发生下述反应,请配平:
Ni2++_______H2PO![]() +_______
+_______![]() =_______Ni++_______H2PO
=_______Ni++_______H2PO![]() +_______
+_______![]()
(3)磷酸钙与焦炭、石英砂混合,在电炉中加热到1 500 ℃生成白磷,反应为
2Ca3(PO4)2+6SiO2![]() 6CaSiO3+P4O10
6CaSiO3+P4O10
10C+P4O10![]() P4+10CO
P4+10CO
若反应生成31 g P4,则反应过程中转移的电子数为____________(用NA表示阿伏加德罗常数的值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)把下列现象中硫酸所表现出来的性质填写在空白处.
①把锌粒放入稀硫酸中时,有气体放出.
②盛有浓硫酸的烧杯敞口放置一段时间后,质量增加.
③用玻璃棒蘸浓硫酸滴在纸上时,纸变黑.
④把木炭放入热的浓硫酸中时,有气体放出.
⑤在常温下可以用铁、铝制容器盛装冷的浓硫酸.
(2)实验室制取氨气的化学方程式: .
(3)铜与稀硝酸反应的离子方程式: .
(4)铜与浓硝酸反应的化学方程式:
(5)氢氧化钠溶液和铵盐溶液共热发生的离子方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A.沸水中滴入FeCl3饱和溶液:Fe3++3H2O![]() Fe(OH)3↓+3H+
Fe(OH)3↓+3H+
B.一小块钠投入水中:Na+2H2O===Na++2OH-+H2↑
C.用氢氧化钠溶液吸收过量二氧化碳:OH-+CO2===HCO![]()
D.Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-===2Fe2++I2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属钨用途广泛,主要用于制造硬质或耐高温的合金,以及灯泡的灯丝。高温下,在密闭容器中用H2还原WO3可得到金属钨,其总反应为:
WO3 (s) + 3H2 (g)![]() W (s) + 3H2O (g)。请回答下列问题:
W (s) + 3H2O (g)。请回答下列问题:
(1)上述反应的化学平衡常数表达式为____________________。
(2) 某温度下反应达平衡时,H2与水蒸气的体积比为2:3,则H2的平衡转化率为___________;随温度的升高,H2与水蒸气的体积比减小,则该反应为 反应(填“吸热”或“放热”)。
(3)用H2还原WO2也可得到金属钨。已知:
WO2 (s) + 2H2 (g)![]() W (s) + 2H2O (g) ΔH = +66.0 kJ·mol–1
W (s) + 2H2O (g) ΔH = +66.0 kJ·mol–1
WO2 (g) + 2H2 (g)![]() W (s) + 2H2O (g) ΔH =-137.9 kJ·mol–1
W (s) + 2H2O (g) ΔH =-137.9 kJ·mol–1
则WO2 (s)![]() WO2 (g) 的ΔH = ______________________。
WO2 (g) 的ΔH = ______________________。
(4)钨丝灯管中的W在使用过程中缓慢挥发,使灯丝变细,加入I2可延长灯管的使用寿命,其工作原理为:W (s) +2I2 (g)![]() WI4 (g)。下列说法正确的有________(填序号)。
WI4 (g)。下列说法正确的有________(填序号)。
a.灯管内的I2可循环使用 b.WI4在灯丝上分解,产生的W又沉积在灯丝上
c.WI4在灯管壁上分解,使灯管的寿命延长
d.温度升高时,WI4的分解速率加快,W和I2的化合速率减慢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2016届北京东城一模】下列叙述正确的是( )
A.NaOH可用于治疗胃酸过多
B.CaO可防止月饼等食品氧化变质
C.氢弹中用到的2H、3H互为同位素
D.向海水中加入净水剂明矾可以使海水淡化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com