
����Ŀ���黯�����������������������뵼�弤������̫���ܵ�غ��ټ��ɵ�·��
��1����̬Niԭ�ӵļ۵����Ų�ʽΪ ___����̬Asԭ�ӵ���ռ������ܼ��ĵ���������ͼΪ __ �Ρ�
��2����һ������As ___Se(����>����������) ��ԭ����____��As2O3(��˪)�����������As2O3������������AsCl3��AsCl3��LiAlH4��ԭ����AsH3��
��3����AlH4-������ԭ�ӵ��ӻ���ʽΪ___����ռ乹��Ϊ____��д��һ����AlH4-��Ϊ�ȵ�����ķ��ӵĻ�ѧʽ___��
��AsH3������H��As��H����__109.5�����>������=������)��AsH3�е����NH3����ԭ����____��
��4���л���![]() �����ƻ�˯������ȱ�ٵ�ҩ����л����д��ڵĻ�ѧ��������Ϊ____(����ĸ���)��
�����ƻ�˯������ȱ�ٵ�ҩ����л����д��ڵĻ�ѧ��������Ϊ____(����ĸ���)��
a�����Ӽ� b������ c������ d��̼̼˫��
��5���黯��������ҽѧ����������Ƥ����ճĤ����ĸ�Ⱦ������ȣ��黯��������ͼ��ʾ���þ����ܶ���Ϊ____g��cm-3(��ʽ���ɣ����ػ���)��

���𰸡�3d84s2 ���壨�Ĵ��� �� AsԪ��ԭ�ӵ�4p����ϵĵ��ӳʰ���״̬���Ƚ��ȶ� sp3 �������� SiH4��CH4 �� Һ̬NH3���Ӽ����γ������AsH3���Ӽ�ֻ�з��»��� abc ![]() ��
��![]() ��
��![]()
��������
��1��Niԭ������Ϊ28����̬Niԭ�ӵļ۵���Ϊ3d�ܼ��ϵ�8�����ӡ�4s�ܼ��ϵ�2�����ӣ���̬Asԭ�Ӻ�������Ų�ʽΪ[Ar]3d104s24p3���û�̬ԭ����ռ������ܼ��ĵ���Ϊ4p���ӣ�Ϊ�����Σ�
��2��ԭ�ӹ���е��Ӵ���ȫ����ȫ�ջ���ʱ���ȶ���
��3����AlH4��������ԭ��Al�ļ۲���ӶԸ���=4+(3+1-4��1)/2=4�Ҳ����µ��Ӷԣ����ݼ۲���ӶԻ��������ж�Alԭ���ӻ���ʽ����ռ乹�ͣ���AlH4����Ϊ�ȵ�����ķ����к���5��ԭ�ӡ��۵�������8��
��AsH3������Asԭ�Ӽ۲���ӶԸ���=3+(5-3��1)/2=4�Һ���1���µ��Ӷԣ��÷���Ϊ�����νṹ���µ��Ӷ���ɼ����Ӷ�֮����ų������ڳɼ����Ӷ�֮����ų�������������Ǽ�С��
�����Ӽ����γ�������⻯���۷е�ϸߣ�
��4���л���![]() �й��۵����д��ڦҼ��������д��ڴ�м��������Ӻ�������֮��������Ӽ���
�й��۵����д��ڦҼ��������д��ڴ�м��������Ӻ�������֮��������Ӽ���
��5���þ�����Niԭ�Ӹ���=4��1/12+4��1/6+2��1/3+2��1/6=2��Asԭ�Ӹ���Ϊ2��Ni��Asԭ�Ӹ���֮��Ϊ2��2=1��1���������=��a��10-10 cm��2��sin60���b��10-10cm=![]() �������ܶ�=
�������ܶ�=![]() ��������㡣
��������㡣
��1��Niԭ������Ϊ28����̬Niԭ�ӵļ۵���Ϊ3d�ܼ��ϵ�8�����ӡ�4s�ܼ��ϵ�2�����ӣ���̬Asԭ�Ӻ�������Ų�ʽΪ[Ar]3d104s24p3����۵����Ų�ʽΪ3d84s2���û�̬ԭ����ռ������ܼ��ĵ���Ϊ4p���ӣ�Ϊ�����Σ�
��2��ԭ�ӹ���е��Ӵ���ȫ����ȫ�ջ���ʱ���ȶ���AsԪ��ԭ�ӵ�4p����ϵĵ��ӳʰ���״̬���Ƚ��ȶ���
��3����AlH4��������ԭ��Al�ļ۲���ӶԸ���=4+(3+1-4��1)/2=4�������µ��Ӷԣ����ݼ۲���ӶԻ������ۣ�Alԭ���ӻ���ʽΪsp3���ռ乹��Ϊ��������ṹ����AlH4����Ϊ�ȵ�����ķ����к���5��ԭ�ӡ��۵�������8����ȵ������� SiH4��CH4��
��AsH3������Asԭ�Ӽ۲���ӶԸ���=3+(5-3��1)/2=4������1���µ��Ӷԣ��÷��ӹ���Ϊ�����Σ��µ��Ӷ���ɼ����Ӷ�֮����ų������ڳɼ����Ӷ�֮����ų������÷����к��йµ��Ӷԣ���������Ǽ�С��С��109.5�㣻
���Ӽ����γ�������⻯���۷е�ϸߣ�Һ̬NH3���Ӽ����γ������AsH3���Ӽ�ֻ�з��»����������۷е�ϸߣ�
��4���л���![]() ���۵����д��ڦҼ��������д��ڴ�м��������Ӻ�������֮��������Ӽ������Ժ������Ӽ����Ҽ����м���
���۵����д��ڦҼ��������д��ڴ�м��������Ӻ�������֮��������Ӽ������Ժ������Ӽ����Ҽ����м���
��ѡabc��
��5���þ�����Niԭ�Ӹ���=4��1/12+4��1/6+2��1/3+2��1/6=2��Asԭ�Ӹ���Ϊ2��Ni��Asԭ�Ӹ���֮��Ϊ2��2=1��1���������=��a��10-10 cm��2��sin60���b��10-10cm=![]() �������ܶ�=
�������ܶ�=![]() =
= g��cm��3��
g��cm��3��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼʵ����ijŨ�����Լ�ƿ��ǩ�ϵ��й����ݣ�����˵����ȷ����

A. ��Ũ������HCl�����ʵ���Ũ��Ϊ11.9mol��L��1
B. ��Һ��HCl�����ʵ���������ȡ����Ķ��ٶ��仯
C. ����500 mL0.400 mol��L��1��ϡ������Ҫ��ȡŨ����1.68mL
D. �кͺ�0.4 g NaOH��NaOH��Һ��ȡ0.400 mol��L��1��ϡ����2.5 mL
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NaOH��Na2CO3�����Һ�еμ�0.2mol��L-1ϡ���ᣬCO2�����������������������V���Ĺ�ϵ��ͼ��ʾ�������ж���ȷ���ǣ� ��
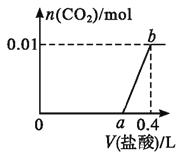
A.��0~a��Χ�ڣ�ֻ������ӦOH-+H+=H2O
B.a=0.35
C.ab�η�����Ӧ�����ӷ���ʽΪ��CO32-+2H+=H2O+CO2��
D.ԭ�����Һ��NaOH��Na2CO3�����ʵ���֮��Ϊ2:1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��1��4�����Ҷ�����ͨ������·�ߺϳɣ�ijЩ��Ӧ�ķ�Ӧ��ͷ�Ӧ����δ�г�����
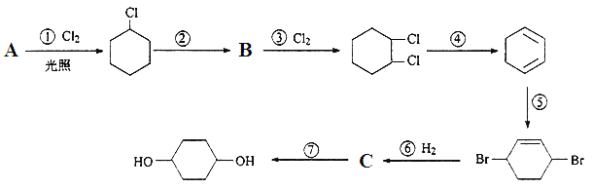
1��4�����Ҷ���
��1��A�Ľṹ��ʽ��___________________________��
��2����Ӧ��Ӧ������Լ���������_______________________________��
��3��д����Ӧ�������Ļ�ѧ����ʽ��
��____________________________________________��
��_________________________________________��
��4�����ķ�Ӧ������_________�����ķ�Ӧ������_________�������߸���Ӧ�����ڼӳɷ�Ӧ����_________���Ӧ��ţ���
��5����Ӧ���п��ܲ���һ�������л����������ܵĽṹ��ʽΪ________________________����д��һ�ּ��ɣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ�У���ȷ����
A. �ö��Ե缫���MgCl2��Һ��2Cl��+H2Oͨ�� 2OH��+Cl2��+H2��
B. SO2ͨ���ˮ�У���Ӧ�����ӷ���ʽΪSO2��I2��2H2O=SO42����2I����4H+
C. ����ͨ����ˮ�У�Cl2 ��H2O ![]() Cl�� ��ClO�� ��2H+
Cl�� ��ClO�� ��2H+
D. ̼��þ����Һ�мӴ��CO32����2CH3COOH �� 2CH3COO����CO2����H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͼa��1 mol NO2��1 mol CO��Ӧ����CO2��NO�����������仯ʾ��ͼ��ͼb�Ƿ�Ӧ�е�CO��NO��Ũ����ʱ��仯��ʾ��ͼ������ͼ��ش��������⣺
a 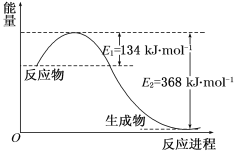 b
b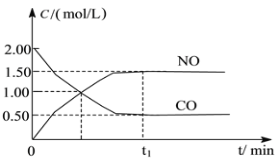
(1)д��NO2��CO��Ӧ���Ȼ�ѧ����ʽ_______________��
(2)�ӷ�Ӧ��ʼ��ƽ�⣬��NO2Ũ�ȱ仯��ʾƽ����Ӧ����v(NO2)��__________��
(3)���¶��¸÷�Ӧ��ƽ�ⳣ��K=_________���¶Ƚ��ͣ�K________����������С�����䡱��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����CH4�� H2OΪԭ���Ʊ������Ѻͼ״��Ĺ�ҵ�������£�
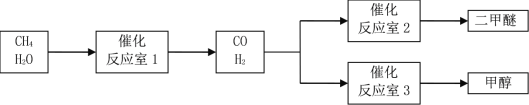
��֪��2CO(g)��O2(g)��2CO2(g)��H����566 kJ��mol-1��CH3OCH3 (g)��3O2(g)��2CO2(g)��3H2O (g) ��H����1323 kJ��mol-1��2H2(g)��O2(g)��2H2O(g)��H����484 kJ��mol-1��
��1����Ӧ��3�з�����Ӧ��CO(g)��2H2(g)��CH3OH(g)���÷�Ӧ��һ�����������Է����е�ԭ����_____��
��2����Ӧ��2�з�����Ӧ��2CO(g)��4H2(g)��CH3OCH3(g)��H2O (g) ��H��_____��
��3����Ӧ��1�з�����Ӧ��CH4(g)��H2O (g) ![]() CO(g)��3H2(g)���Դ˷�Ӧ���������о���T��ʱ�����ݻ�Ϊ2 L���ܱ������г���һ������CH4(g)��H2O (g)���з�Ӧ��ʵ���÷�Ӧ�����еIJ������ݼ��±�������t1��t2����
CO(g)��3H2(g)���Դ˷�Ӧ���������о���T��ʱ�����ݻ�Ϊ2 L���ܱ������г���һ������CH4(g)��H2O (g)���з�Ӧ��ʵ���÷�Ӧ�����еIJ������ݼ��±�������t1��t2����
��Ӧʱ��/min | n(CH4)/mol | n(H2O)/ mol |
0 | 1.20 | 0.60 |
t1 | 0.80 | |
t2 | 0.20 |
�ٷ�Ӧ�ӿ�ʼ��t1����ʱ��ƽ����Ӧ����Ϊv(H2)=_______mol��L-1��min-1��
�������������������䣬��ʼʱ�������г���0.60 mol CH4��1.20 mol H2O����Ӧһ��ʱ����������H2�����ʵ���Ϊ0.60 mol�����ʱv��______v�����>������<����=������
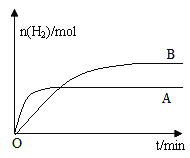
����������Ӧ�ı�ijһ���������H2�����ʵ�����ʱ��仯��ͼ������B��AΪԭ��Ӧ�����ߣ�����ı������������_________��
��4���Է�Ӧ��1������CO��H2Ϊȼ�ϣ�һ������Li2CO3��Na2CO3���ۻ����Ϊ����ʹ��ɵ�һ��̼����ȼ�ϵ��������ͼ��ʾ��
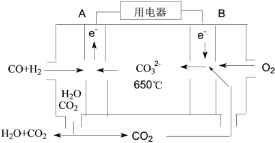
�ٸõ�ص�������ӦʽΪ_____��
������·������4 mol���ӣ�������������CO��H2�������Ϊ________L����״������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ͷǽ������������������еõ��˹㷺Ӧ��,����ش��������⡣
��1��������ͷ۵���Ҫ�ɷ�֮һ��һ�����Σ����׳�Ϊ________��Ư�۵���Ч�ɷ�Ϊ__________��д��ѧʽ����FeCl3��������ˮ������ԭ��Ϊ_________�������ӷ���ʽ��ʾ����
��2��մ��ˮ�����������ڸ��»����ϻᷢ�ڣ��÷�Ӧ�Ļ�ѧ����ʽ��_________��
��3������Ѫ�쵰���к���Fe2+������ʳ�������Σ��ᵼ��Fe2+ת��Fe3+���ж�������ά����C���Խⶾ���������ķ�����ȷ������______��
A�����������ǻ�ԭ�� B��ά����C��������
C��ά����C������ D���������η���������Ӧ
��4��ijCuSO4��H2SO4�Ļ����Һ100mL����֪��Һ�������ӵ�Ũ����ȣ�������ˮ�⣩����SO42-�����ʵ���Ũ��Ϊ6mol/L�������Һ�������ӵ�Ũ��Ϊ___________mol/L���������Һ�м������Zn��������ܽ�Zn������Ϊ____________g��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ�NA��ʾ�����ӵ�������ֵ���� ��
A.�ڳ��³�ѹ�£�11.2LN2���еķ�����Ϊ0.5NA
B.��״���£�11.2LH2O���еķ�����Ϊ0.5NA
C.�ڳ��³�ѹ�£�71gCl2����������ΪNA
D.��״���£�32gO2�к��еķ�����Ϊ2NA
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com