
【题目】K2Cr2O7溶液中存在平衡: Cr2O72-(橙色)+H2O![]() 2CrO42-(黄色)+2H+。用K2Cr2O7溶液进行下列实验:
2CrO42-(黄色)+2H+。用K2Cr2O7溶液进行下列实验:

(1)向K2Cr2O7溶液中加入30% NaOH溶液,溶液呈________色,因为________________。
(2)若向已加入NaOH溶液的(1)中再加入过量稀硫酸,则溶液呈________色,因为____________________________________________________。
(3)向K2Cr2O7溶液中逐滴加入Ba(NO3)2溶液(已知BaCrO4为黄色沉淀),则平衡向着_________方向移动,溶液颜色变化为____________。
(4)对比②和④可得出的结论是______________________________
【答案】黄 c(H+)变小,平衡向正反应方向移动,使c(CrO42-)增大 橙 加入过量稀硫酸,使得溶液中c(H+)变大,平衡向逆反应方向移动,使c(Cr2O72-)增大 正反应 橙色逐渐变浅,最后变为无色 K2Cr2O7酸性溶液氧化性强
【解析】
(1)加入少量NaOH固体,中和氢离子,氢离子浓度降低,平衡向右移动;
(2)加入酸,H+浓度增大,平衡左移,Cr2O72-浓度增大;
(3)向原溶液中加入Ba(NO3)2溶液,生成BaCrO4沉淀,CrO42-浓度降低。
(4)酸性溶液中变色,碱性溶液不变色,说明K2Cr2O7在酸性溶液中氧化性强。
(1)加入少量NaOH固体,中和氢离子,溶液中H+离子浓度降低,平衡向右移动,溶液呈黄色,故答案为:黄;c(H+)变小,平衡向正反应方向移动,使c(CrO42-)增大;
(2)加入酸,溶液中H+离子浓度增大,平衡左移,溶液中Cr2O72-离子浓度增大,溶液呈橙色,故答案为:橙;加入过量稀硫酸,使得溶液中c(H+)变大,平衡向逆反应方向移动,使c(Cr2O72-)增大;
(3)向原溶液中加入Ba(NO3)2溶液,生成BaCrO4沉淀,CrO42-浓度降低,平衡正向移动,溶液的颜色变浅,最后变为无色,故答案为:正反应;橙色逐渐变浅,最后变为无色;
(4)酸性溶液中变色,碱性溶液不变色,说明K2Cr2O7在酸性溶液中氧化性强。


 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数的值,下列说法中不正确的是
A. 标准状况下22.4 L异丁烷的分子数为NA
B. 78 g苯(C6H6)和苯乙烯(C8H8)的混合物中含有的碳氢键数一定为6NA
C. 某温度下,1L pH=3的醋酸溶液稀释到10L时,溶液中H+的数目大于0.01NA
D. 向仅含0.2 mol FeI2的溶液中持续通入Cl2,当有0.1 mol Fe2+被氧化时,转移电子的数目为0.5NA 。(不考虑Cl2与H2O的反应)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用吸附了H2的碳纳米管等材料制作的二次电池的原理如图所示。下列说法正确的是( )

A. 放电时,甲电极反应为NiO(OH)+H2O+e-=Ni(OH)2+OH-
B. 放电时,甲电极为正极,OH-移向乙电极
C. 电池放电时总反应为H2+2NiO(OH)=2Ni(OH)2
D. 充电时,电池的碳电极与直流电源的正极相连
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化亚铜(CuCl)常用作有机合成工业中的催化剂,在空气中迅速被氧化成绿色;见光则分解,变成褐色。如图是工业上用制作印刷电路的废液(含Fe3+、Cu2+、Fe2+、Cl-)生产CuCl的流程:

根据以上信息回答下列问题:
(1)生产过程中X的化学式为________。
(2)写出产生CuCl的化学方程式:__________________________________________。
(3)在CuCl的生成过程中理论上不需要补充SO2气体,结合化学方程式和必要的文字说明理由_____________________________________________________
实际生产中SO2要适当过量,原因可能是_______________________________(答一点即可)。
(4)实验探究pH对CuCl产率的影响如下表所示:
pH | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
CuCl产率/% | 70 | 90 | 82 | 78 | 75 | 72 | 70 |
析出CuCl晶体最佳pH为________,当pH较大时CuCl产率变低,原因是________________________________________________________________________。调节pH时,________(填“能”或“不能”)用相同pH的硝酸代替硫酸,理由__________________。
(5)氯化亚铜的定量
①称取样品0.25 g和过量的FeCl3溶液于锥形瓶中,充分溶解。
②用0.10 mol·L-1硫酸铈标准溶液滴定。已知:CuCl+FeCl3===CuCl2+FeCl2、Fe2++Ce4+===Fe3++Ce3+。三次平行实验结果如下(平行实验结果相差不能超过1%):
平行实验次数 | 1 | 2 | 3 |
0.25 g样品消耗硫酸铈 标准溶液的体积/mL | 24.35 | 24.05 | 23.95 |
则样品中CuCl的纯度为________(结果保留三位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高炉炼铁中发生的基本反应之一如下:FeO(s) +CO(g)![]() Fe(s)+CO2(g)(正反应是吸热反应),已知1100℃时K=0.263。
Fe(s)+CO2(g)(正反应是吸热反应),已知1100℃时K=0.263。
(1)温度升高,化学平衡移动后达到新的平衡,高炉内CO2和CO的体积比值________;平衡常数K值___________ (选填“增大”“减小”或“不变”)。
(2)1100℃时测得高炉中c(CO2)=0.025mol·L﹣1、c(CO)=0.1mol·L﹣1,在这种情况下,该反应是否处于化学平衡状态_________ (选填“是”或“否”),此时,化学反应速率是v(正)_____ v(逆)(选填“大于”“小于”或“等于”),其原因是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组设计的用化学电源使LED灯发光的装置如图。下列说法错误的是( )

A. 铜片表面有气泡生成,锌片上发生氧化反应
B. 如果将稀硫酸换成葡萄糖溶液,不能使LED灯发光
C. 装置中存在“化学能→电能→光能”的转换
D. 如果将铜片换成铁片,则锌片为正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理。某工厂对制革工业污泥中Cr(Ⅲ)的处理工艺流程如下:
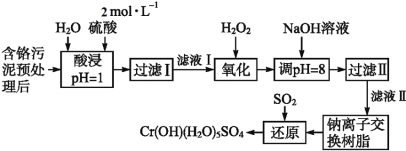
已知:①硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+。
②常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
阳离子 | Fe3+ | Mg2+ | Al3+ | Cr3+ |
沉淀完全时的pH | 3.7 | 11.1 | 5.4(>8溶解) | 9(>9溶解) |
(1)实验室用18.4 mol·L-1的浓硫酸配制480 mL 2 mol·L-1的硫酸,需量取浓硫酸_________mL;配制时所用玻璃仪器除量筒、胶头滴管、烧杯和玻璃棒外,还需__________________________。
(2)H2O2的作用是将滤液Ⅰ中的Cr3+转化为Cr2O72-,写出此反应的离子方程式:__________。
(3)加入NaOH溶液使溶液呈碱性,既可以除去某些杂质离子,同时又可以将Cr2O72-转化为CrO42-,写出该反应的离子方程式__________________。
(4)钠离子交换树脂的反应原理为:Mn+ + n NaR = MRn + n Na+,则利用钠离子交换树脂可除去滤液Ⅱ中的金属阳离子有__________________。
(5)写出上述流程中用SO2进行还原时发生反应的离子方程式:_________________。
(6)沉淀滴定法是测定粒子浓度的方法之一,为了测定某废水中SCN-浓度,可用标准AgNO3溶液滴定待测液,已知:
银盐性质 | AgCl | AgI | AgCN | Ag2CrO4 | AgSCN |
颜色 | 白 | 黄 | 白 | 砖红 | 白 |
Ksp | 1.8×10-10 | 8.3×10-17 | 1.2×10-16 | 3.5×10-11 | 1.0×10-12 |
滴定时可选为滴定指示剂的是_________(选填编号),滴定终点现象是:________。
A.NaCl B.K2CrO4 C.KI D.NaCN
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下为中学化学中常见的物质:①Cu; ②1molL﹣1的FeCl3溶液; ③CuCl2溶液;④CO2;⑤H2SO4;⑥酒精;⑦CaCO3;⑧FeSO4;⑨Ba(OH)2
(1)以上物质中属于电解质的是__;属于非电解质的是__.
(2)用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入②的溶液,至液体呈透明的红褐色氢氧化铁胶体.则反应的化学方程式为__________________;
(3)将②③⑧混合配制成浓度均为1molL﹣1的混合溶液100mL,加入一定量的铁粉,充分反应后,若铁粉无剩余,且有铜生成.则反应后的溶液中一定含有__阳离子,可能含有__阳离子.
(4)向⑨溶液中逐滴加入稀硫酸,请完成下列问题:
① 写出该反应的离子方程式:______________________________.
② 下列三种情况下,离子方程式与①相同的是__( 填序号).
A.向NaHSO4 溶液中逐滴加入Ba(OH)2溶液至溶液显中性
B.向NaHSO4 溶液中逐滴加入Ba(OH)2溶液至SO42﹣恰好完全沉淀
C.向NaHSO4 溶液中逐滴加入Ba(OH)2溶液至过量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com