
【题目】氯化亚铜(CuCl)常用作有机合成工业中的催化剂,在空气中迅速被氧化成绿色;见光则分解,变成褐色。如图是工业上用制作印刷电路的废液(含Fe3+、Cu2+、Fe2+、Cl-)生产CuCl的流程:

根据以上信息回答下列问题:
(1)生产过程中X的化学式为________。
(2)写出产生CuCl的化学方程式:__________________________________________。
(3)在CuCl的生成过程中理论上不需要补充SO2气体,结合化学方程式和必要的文字说明理由_____________________________________________________
实际生产中SO2要适当过量,原因可能是_______________________________(答一点即可)。
(4)实验探究pH对CuCl产率的影响如下表所示:
pH | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
CuCl产率/% | 70 | 90 | 82 | 78 | 75 | 72 | 70 |
析出CuCl晶体最佳pH为________,当pH较大时CuCl产率变低,原因是________________________________________________________________________。调节pH时,________(填“能”或“不能”)用相同pH的硝酸代替硫酸,理由__________________。
(5)氯化亚铜的定量
①称取样品0.25 g和过量的FeCl3溶液于锥形瓶中,充分溶解。
②用0.10 mol·L-1硫酸铈标准溶液滴定。已知:CuCl+FeCl3===CuCl2+FeCl2、Fe2++Ce4+===Fe3++Ce3+。三次平行实验结果如下(平行实验结果相差不能超过1%):
平行实验次数 | 1 | 2 | 3 |
0.25 g样品消耗硫酸铈 标准溶液的体积/mL | 24.35 | 24.05 | 23.95 |
则样品中CuCl的纯度为________(结果保留三位有效数字)。
【答案】Fe CuCl2+CuSO4+SO2+2H2O===2CuCl↓+2H2SO4 Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O,反应中生成的CuSO4和SO2为1∶1,生产CuCl的过程中消耗CuSO4和SO2的物质的量之比也为1∶1,所以理论上不需要补充SO2气体 提高Cu2+的还原速率,同时可以防止生成的Cu+被空气氧化 2 Cu2+水解程度增大,反应生成CuCl减少,产率减小 不能 硝酸会与产品CuCl发生反应 95.5%
CuSO4+SO2↑+2H2O,反应中生成的CuSO4和SO2为1∶1,生产CuCl的过程中消耗CuSO4和SO2的物质的量之比也为1∶1,所以理论上不需要补充SO2气体 提高Cu2+的还原速率,同时可以防止生成的Cu+被空气氧化 2 Cu2+水解程度增大,反应生成CuCl减少,产率减小 不能 硝酸会与产品CuCl发生反应 95.5%
【解析】
由流程图可知,向废液(含Fe3+、Cu2+、Fe2+、Cl-)中加入过量的铁粉,三价铁离子与铁粉反应转化为二价铁离子,铜离子与铁反应生成铜,然后过滤,滤渣为过量的铁和生成的铜,依据铜与铁活泼性,将滤渣溶于盐酸,铜与盐酸不反应,过滤得到滤渣即为铜,然后铜与浓硫酸反应生成硫酸铜和二氧化硫,铜与氯气反应生成氯化铜,硫酸铜、二氧化硫、氯化铜反应生成氯化亚铜。
(1)印刷电路的废液(含Fe3+、Cu2+、Fe2+、Cl-)加入铁,三价铁离子能够原铁反应生成二价铁离子,铜离子能够与铁反应生成铜,过滤后滤渣中含有铜和铁,加入盐酸,铁与盐酸反应生成氯化亚铁,铜与盐酸不反应,将铜分离出来,故答案为:Fe;
(2)依据图示可知:CuCl2、CuSO4、SO2、H2O反应生成H2SO4、CuCl,产生CuCl的化学方程式依据得失电子守恒得到:CuCl2+CuSO4+SO2+2H2O=2CuCl↓+2H2SO4,故答案为:CuCl2+CuSO4+SO2+2H2O=2CuCl↓+2H2SO4;
(3)依据图示可知:Cu+2 H2SO4(浓)![]() CuSO4+SO2↑+2H2O反应中生成的CuSO4和 SO2为1:1,CuCl2+CuSO4+SO2+2H2O=2CuCl↓+2 H2SO4反应中消耗CuSO4和SO2也为1﹕1,所以理论上不需要补充SO2气体;SO2适当过量,可以提高Cu2+的还原速率,同时可以防止生成的Cu+被空气中氧气氧化,故答案为:Cu+2 H2SO4(浓)
CuSO4+SO2↑+2H2O反应中生成的CuSO4和 SO2为1:1,CuCl2+CuSO4+SO2+2H2O=2CuCl↓+2 H2SO4反应中消耗CuSO4和SO2也为1﹕1,所以理论上不需要补充SO2气体;SO2适当过量,可以提高Cu2+的还原速率,同时可以防止生成的Cu+被空气中氧气氧化,故答案为:Cu+2 H2SO4(浓)![]() CuSO4+SO2↑+2H2O反应中生成的CuSO4和 SO2为1:1,CuCl2+CuSO4+SO2+2H2O=2CuCl↓+2 H2SO4反应中消耗CuSO4和SO2也为1﹕1,所以理论上不需要补充SO2气体;提高Cu2+的还原速率,同时可以防止生成的Cu+被空气氧化;
CuSO4+SO2↑+2H2O反应中生成的CuSO4和 SO2为1:1,CuCl2+CuSO4+SO2+2H2O=2CuCl↓+2 H2SO4反应中消耗CuSO4和SO2也为1﹕1,所以理论上不需要补充SO2气体;提高Cu2+的还原速率,同时可以防止生成的Cu+被空气氧化;
(4)依据图表CuCl产率可知pH=2产率最大为90%,当pH较大时CuCl产率变低,Cu2+水解程度增大,生成的氯化亚铜少;调节pH时,不能用具有强氧化性的硝酸替代硫酸,因为硝酸会将CuCl氧化,故答案为:2;pH较大时,Cu2+水解程度增大,反应生成CuCl减少,产率减小;硝酸会与产品CuCl发生反应;
(5)根据题目中所给数据及平行实验结果相差不能超过0.3%,滴定0.25g样品消耗硫酸铈标准溶液的平均体积是23.9ml,结合方程式可知:CuCl+FeCl3═CuCl2+FeCl2,CuCl的纯度为23.9×10-3L×0.1 molL-1×99.5gmol-1/0.25g×100%=95%,故答案为:95%。


 字词句段篇系列答案
字词句段篇系列答案科目:高中化学 来源: 题型:
【题目】下列关于金属的叙述正确的是( )
A.常温下所有的金属都是固体
B.金属具有导电性、导热性和延展性
C.所有金属都能与酸反应
D.金属元素在自然界中都是以化合态形式存在的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 化合物 的分子式为C13H9O4N2
的分子式为C13H9O4N2
B. 在碱性条件下,CH3CO18OC2H5的水解产物是CH3COOH和C2H![]() OH
OH
C. 在一定条件下,乙酸、氨基乙酸、蛋白质均能与NaOH发生反应
D. 甲苯苯环上的一个氢原子被—C3H6Cl取代,形成的同分异构体有9种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烯烃与H2发生加成反应后得到的产物是CH3-CH(CH3)2.
(1)该产物的一氯代物有 _______________种;
(2)原来烯烃的结构简式为: _________________ ;
(3)该烯烃一定条件下发生加聚反应写出加聚产物的结构简式为:_________________;
(4)写出原来的烯烃使溴的四氯化碳溶液褪色的化学反应方程式:
_______________________________________________;
(5) 系统命名法的名称______________________。
系统命名法的名称______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中只含有共价键的是( )
A.NaCl、HCl、H2O、NaOHB.Cl2、Na2S、HCl、SO2
C.Na2O2、H2O2、H2O、O3D.HBr、CO2、H2O、CS2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述正确的是
A. 标准状况下,3.2 g 14C18O中含中子数为1.4NA
B. CO燃烧热为283.0 kJ/mol,若一定量的CO完全燃烧放出热量为283.0 kJ,则消耗O2分子数为NA
C. 等体积、等物质的量浓度的NaCl和KF溶液中,阴、阳离子数目之和相等
D. 室温下,21.0 gC2H4和C4H8的混合气体中含有的原子数目为4.5 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】K2Cr2O7溶液中存在平衡: Cr2O72-(橙色)+H2O![]() 2CrO42-(黄色)+2H+。用K2Cr2O7溶液进行下列实验:
2CrO42-(黄色)+2H+。用K2Cr2O7溶液进行下列实验:

(1)向K2Cr2O7溶液中加入30% NaOH溶液,溶液呈________色,因为________________。
(2)若向已加入NaOH溶液的(1)中再加入过量稀硫酸,则溶液呈________色,因为____________________________________________________。
(3)向K2Cr2O7溶液中逐滴加入Ba(NO3)2溶液(已知BaCrO4为黄色沉淀),则平衡向着_________方向移动,溶液颜色变化为____________。
(4)对比②和④可得出的结论是______________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物F( )为一种高分子树脂,其合成路线如下:
)为一种高分子树脂,其合成路线如下:

已知:①A为苯甲醛的同系物,分子中无甲基,其相对分子质量为134;
②
请回答下列问题:
(1)X的化学名称是_________________。
(2)E生成F的反应类型为_________________。
(3)D的结构简式为_________________。
(4)由B生成C的化学方程式为_________________。
(5)芳香族化合物Y是D的同系物,Y的同分异构体能与饱和Na2CO3溶液反应放出气体,分子中只有1个侧链,核磁共振氢普显示有5种不同化学环境的氢,峰值面积比为6:2:2:1:1。写出两种符合要求的Y的结构简式___________、__________。
(6)写出以甲醛、丙醛和乙二醇为主要原料合成软质隐形眼镜高分子材料—聚甲基丙烯酸羟乙酯( )的合成路线(无机试剂自选):_________________。
)的合成路线(无机试剂自选):_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.100mol·L-1的NaOH溶液分别滴定同浓度、体积均为20.00mL的盐酸和醋酸溶液(用HA表示酸),得到2条滴定曲线,如图所示。
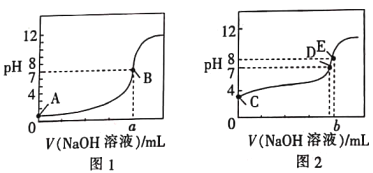
下列说法正确的是
A. 滴定醋酸的曲线是图1
B. 由图分析可得b>a=20
C. D点对应的溶液中:c(Na+)=c(A-)
D. 根据E点可计算得K(HA)=[0.05+(10-6-10-8)]×10-8/(10-6-10-8)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com