
【题目】反应N2(g)+O2(g)=2NO(g)的能量变化如图所示。
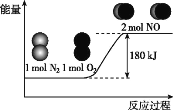
已知:断开1molN2(g)中化学键需吸收946kJ能量,断开1molO2(g)中化学键需吸收498kJ能量。下列说法正确的是( )
A.N2和O2的总能量一定高于NO的总能量
B.2NO(g)=N2(g)+O2(g),该反应为吸热反应
C.断开1molNO(g)中化学键需吸收90kJ能量
D.形成1molNO(g)中化学键可释放632kJ能量
 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
【题目】经分析,芳香族化合物A含有C、 H 、O的质量分数分别为77.8%、7.4%、14.8%,该有机物一个分子中只含有一个氧原子。
(1)通过计算,写出该有机物的分子式________________________。
(2)如果该有机物遇FeCl3溶液变为紫色,写出满足要求的所有有机物的结构简式,并用系统命名法命名________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组的同学设计了如图装置制取溴苯和溴乙烷:
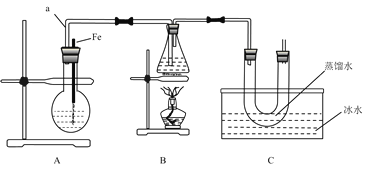
己知:乙醇在加热的条件下可与HBr反应得到溴乙烷(CH3CH2Br),二者某些物理性质如下表所示:
溶解性(本身均可作溶剂) | 沸点(℃) | 密度(g/mL) | |
乙醇 | 与水互溶,易溶于有机溶剂 | 78.5 | 0.8 |
溴乙烷 | 难溶于水,易溶于有机溶剂 | 38.4 | 1.4 |
请回答下列问题:
(1) B中发生反应生成目标产物的化学方程式为_________。
(2)根据实验目的,选择下列合适的实验步骤:①→___________(选填②③④等)。
①组装好装置,___________(填写实验操作名称);
②将A装置中的纯铁丝小心向下插入苯和液溴的混合液中;
③点燃B装置中的酒精灯,用小火缓缓对锥形瓶加热10分钟;
④向烧瓶中加入一定量苯和液溴,向锥形瓶中加入无水乙醇至稍高于进气导管口处,向U形管中加入蒸馏水封住管底,向水槽中加入冰水。
(3)简述实验中用纯铁丝代替铁粉的优点:_____。
(4)冰水的作用是_______。
(5)反应完毕后,U形管内的现象是______________;分离溴乙烷时所需的玻璃仪器有_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关反应限度的叙述正确的是
A. 使用催化剂,可降低反应的活化能,加快反应速率,改变反应限度
B. 依据焓判据:NH4HCO3受热分解可自发进行
C. 大多数化学反应在一定条件下都有一定的限度
D. FeCl3与KSCN反应达到平衡时,向其中滴加少量KCl溶液,则溶液颜色变深
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F、G均为短周期元素,原子序数依次递增。A元素原子核内无中子,B元素原子最外层电子数是次外层电子数的2倍,D是地壳中含量最多的元素,E是短周期中金属性最强的元素,F与G位置相邻,G是同周期元素中原子半径最小的主族元素。请回答下列问题:
(1)C在元素周期表中的位置为___,G的原子结构示意图是___。
(2)D与E按原子个数比1:1形成化合物甲,其电子式为___,所含化学键类型为___。向甲中滴加足量水时发生反应的化学方程式是___。
(3)E、F、G三种元素所形成的简单离子,半径由大到小的顺序是___。(用离子符号表示)
(4)用BA4、D2和EDA的水溶液组成燃料电池,电极材料为多孔惰性金属电极。在a极通入BA4气体,b极通入D2气体,则a极是该电池的___极,负极的电极反应式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A+3B=2C+D在四种不同情况下的反应速率分别为①v(A)=0.15mol·L-1·s-1 ②v(B)=0.6mol·L-1·s-1 ③v(C)=0.5mol·L-1·min-1 ④v(D)=0.45mol·L-1·s-1。则反应进行由快到慢的顺序为( )
A.④>③>①>②B.④>②>①>③
C.②>③>④>①D.④>③>②>①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“神舟七号”成功登天标志着我国的航天事业进入了新的篇章。
(1)某空间站局部能量转化系统如下图所示,其中燃料电池采用KOH溶液为电解液,燃料电池放电时的负极反应式为___________________________________。如果某段时间内氢氧储罐中共收集到33.6 L(已折算成标况)气体,则该段时间内水电解系统中转移电子的物质 的量为_________mol。

(2)在载人航天器的生态系统中,不仅要求分离出CO2,还要求提供充足的O2。某种电化学装置可实现转化2CO2 =2CO+O2,CO可用作燃料。已知该反应的阳极反应式为4OH--4e-=O2↑+2H2O,则阴极反应式为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用浓硫酸配制1.0mol/L硫酸溶液480mL,回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是 ______(填字母),配制上述溶液还需用到的玻璃仪器是_________(填仪器名称)。

(2)容量瓶上标有以下5项中的_____(填序号)
①压强 ②温度 ③容量 ④浓度 ⑤刻度线
(3)在配制过程中,下列操作使所配溶液浓度偏大的是__________ .
①未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中
②定容摇匀后,发现液面低于刻度线,又用胶头滴管加蒸馏水至刻度线
③定容时,仰视刻度线
④使用容量瓶前用蒸馏水洗涤且没干燥
(4)计算实验室配制上述溶液需用量筒量取质量分数为98%、密度为1.84g/mL的浓硫酸的体积为:_____mL。(保留小数点后一位)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学方程式中,不能正确表达反应颜色变化的是
A. 向CuSO4溶液中加入足量Zn粉,溶液蓝色消失Zn+CuSO4![]() Cu+ZnSO4
Cu+ZnSO4
B. 澄清的石灰水久置后出现白色固体Ca(OH)2+CO2![]() CaCO3↓+H2O
CaCO3↓+H2O
C. Na2O2在空气中放置后由淡黄色变为白色2Na2O2![]() 2Na2O+O2↑
2Na2O+O2↑
D. 向Mg(OH)2悬浊液中滴加足量FeCl3溶液出现红褐色沉淀3Mg(OH)2+2FeCl3![]() 2Fe(OH)3+3MgCl2
2Fe(OH)3+3MgCl2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com