
【题目】短周期主族元素W、X、Y、Z的原子序数依次增加。K、L、M均是由这些元素组成的二元化合物,甲、乙分别是元素X、Y的单质,甲是常见的固体,乙是常见的气体。K 是无色气体,是主要的大气污染物之一。0.05 mol/L丙溶液的pH为1,上述物质的转化关系如图所示。下列说法正确的是
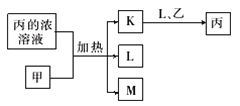
A. K、L、M 中沸点最高的是M
B. 元素的非金属性:Z>Y>X
C. 原子半径:W<X<Y
D. 丙也可由W、Y组成的某化合物与K直接反应制得
 全优点练单元计划系列答案
全优点练单元计划系列答案科目:高中化学 来源: 题型:
【题目】有关晶格能的叙述不正确的是( )
A.1mol气态金属阳离子离子和1mol气态阴离子离子结合生成1mol离子晶体时释放出的热能为离子晶体的晶格能
B.晶格能通常取正值
C.晶格能越大,形成的离子晶体越稳定
D.晶格能越大,物质的硬度反而越小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的盐酸跟过量的铁粉反应时,为了减缓反应速率但不影响生成H2的总量,可向盐酸中加入适量的
A.CaCO3(s) B.Na2SO4溶液
C.KNO3溶液 D.CuSO4(s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质或物质的主要成分对应化学式错误的是
A. 铜绿-Cu2(OH)2CO3 B. 芒硝-NaNO3·10H2O
C. 漂粉精-Ca(ClO)2 D. 水玻璃-Na2SiO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水是一个巨大的化学资源宝库.利用海水可以获得许许多多化工产品。
(1)由海水经过晾硒可制得粗盐.实验室去除掉粗盐中的泥沙所需的玻璃仪器有_________________。
(2)利用制盐后的盐卤提取溴的工艺流程如下(部分操作和条件已略去):

①溶液I→Br2的离子方程式为:Br-+BrO3-+H+→Br2+H2O(未配平),反应中氧化产物和还原产物的质量之比为____________。
②上图中低浓度尽Br2加Na2CO3,、H2SO4处理的目的是____________。
(3)盐卤蒸发冷却后析出卤块的主要成分是MgCl2此外还含Fe2+、Fe3+、Mn2+等离子,以卤块为原料制得镁的工艺流程如下(部分操作和条件巳略去)

巳知生成氢氧化物沉淀的pH如下.
沉淀物 | Fe(OH)2 | Fe(OH)3 | Mn(OH)2 | Mg(OH)2 |
开始沉淀 | 7.6 | 2.7 | 8.3 | 9.6 |
沉淀完全 | 9.6 | 3.7 | 9.8 | 11.1 |
①步骤②中需控制pH=9.8,其目的是____________________________________。
②NaClO还能除去盐卤中的尿素[CO (NH2)2],生成盐类物质和能参与大气循环的物质,其反应原理___________(用化学方程式表示),请你计算,若除去盐卤中含有的0.1 molCO (NH2)2时需消耗NaClO_____g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,在原理上可以设计成原电池的是( )
A. Ba(OH)2·8H2O与NH4Cl的反应 B. 氧化铝与硫酸的反应
C. 甲烷与氧气的反应 D. 石灰石的分解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
常见的太阳能电池有单晶硅太阳能电池、多晶硅太阳能电池、GaAs太阳能电池及铜铟镓硒薄膜太阳能电池等。
(1)Cu+在基态时的价电子排布式为______。
(2)砷、碲是第四周期的相邻元素,已知砷的第一电离能大于硒。请从原子结构的角度加以解释______。
(3)GaAs熔点1238℃,难溶于溶剂。其晶体类型为_________。
(4)AsF3的空间构型是:______________。
(5)硼酸(H3BO3)本身不能电离出H+,在水中易结合一个OH-生成[B(OH)4]-,而体现弱酸性。
①[B(OH)4]-中B原子的杂化类型为______。
②[B(OH)4]-的结构式为____________。
(6)金刚石的晶胞如下图,若以硅原子代替金刚石晶体中的碳原子,便得到晶体硅:若将金刚石晶体中一半的碳原子換成硅原子,且碳、硅原子交替,即得到碳化硅晶体(金刚砂)。
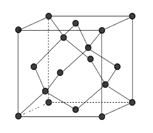
①金刚石、晶体硅、碳化硅的熔点由高到低的排列顺序是_______(用化学式表示)。
②立方氮化硼晶体的结构与金刚石相似,硬度与金刚石相当,晶胞边长为361.5pm。立方氮化硼的密度是___________g·㎝-3(B的相对原子质量为11,只要求列算式,不必计算出数值,阿伏伽徳罗常数为NA)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组采用类似制乙酸乙酯的装置(如图1),以环己醇制备环己烯
己知: 

密度(g/cm3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
环乙醇 | 0.96 | 25 | 161 | 能溶于水 |
环乙烯 | 0.81 | -103 | 83 | 难溶于水 |
(1) 制备粗品将12.5 mL环己醇加入试管A中,再加入lmL浓硫酸,摇匀后放入碎瓷片,慢加热至反应完全,在试管C内得到环己烯粗品。
①A中碎瓷片的作用是____________,导管B除了导气外还具有的作用是____________②试管C置于冰水浴中的目的是______________________。
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环乙烯在______层(填上或下),分液后用___________(填入编号)洗涤。
a. KMnO4溶液 b.稀 H2SO4 c. Na2CO3溶液
②再将环己烯按图2所示装置蒸馏,冷却水从________口进入,收集产品时,控制的温度应在______左右。
(3)以下区分环己烯精品和租品的方法,合理的是_____________。
a.用酸性高锰酸钾溶液 b.用NaOH溶液 c.测定沸点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肼(H2N-NH2)是一种高能燃料,有关化学反应的能量变化如图所示。已知断裂1 mol 化学键所需的能量(kJ):N≡N为942、O=O为500、N―N 为154,则断裂1 mol N―H 键所需的能量(kJ)是

A.194 B.391 C.516 D.658
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com