
【题目】
常见的太阳能电池有单晶硅太阳能电池、多晶硅太阳能电池、GaAs太阳能电池及铜铟镓硒薄膜太阳能电池等。
(1)Cu+在基态时的价电子排布式为______。
(2)砷、碲是第四周期的相邻元素,已知砷的第一电离能大于硒。请从原子结构的角度加以解释______。
(3)GaAs熔点1238℃,难溶于溶剂。其晶体类型为_________。
(4)AsF3的空间构型是:______________。
(5)硼酸(H3BO3)本身不能电离出H+,在水中易结合一个OH-生成[B(OH)4]-,而体现弱酸性。
①[B(OH)4]-中B原子的杂化类型为______。
②[B(OH)4]-的结构式为____________。
(6)金刚石的晶胞如下图,若以硅原子代替金刚石晶体中的碳原子,便得到晶体硅:若将金刚石晶体中一半的碳原子換成硅原子,且碳、硅原子交替,即得到碳化硅晶体(金刚砂)。
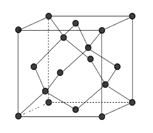
①金刚石、晶体硅、碳化硅的熔点由高到低的排列顺序是_______(用化学式表示)。
②立方氮化硼晶体的结构与金刚石相似,硬度与金刚石相当,晶胞边长为361.5pm。立方氮化硼的密度是___________g·㎝-3(B的相对原子质量为11,只要求列算式,不必计算出数值,阿伏伽徳罗常数为NA)。
【答案】 3d10 )砷的4p轨道上的电子处于半充满状态,比较稳定,气态原子失去一个电子需要的能量比较大 原子晶体 三角锥形 sp3杂化  C>SiC>Si
C>SiC>Si 
【解析】(1)铜是29号元素,其原子核外有29个电子,根据构造原理知,其基态原子核外电子排布式为:1s22s22p63s23p63d104s1或[Ar]3d104s1,则Cu+在基态时的价电子排布式为3d10;
(2)砷的价电子排布式是4s24p3,4p轨道上的电子处于半充满状态,比较稳定,气态原子失去一个电子需要的能量比较大,而硒的价电子排布式是4s2 4p4,4p轨道上失去一个电子才处于半充满状态,故第一电离能较小;
(3)GaAs熔点1238℃,难溶于溶剂,可知其晶体类型为原子晶体;
(4)AsF3分子中As原子成3个As-F单键、含有1对孤对电子,杂化轨道数为4,采取sp3杂化,故AsF3分子为三角锥型;
(5)①[B(OH)4]-中B的价层电子对=4+![]() (3+1-4×1)=4,所以采取sp3杂化;
(3+1-4×1)=4,所以采取sp3杂化;
②B原子是缺电子原子,所以该离子中还含有配位键,其结构为 ;
;
(5)①中形成的晶体都是原子晶体.由于键长C-C<C-Si<Si-Si,则熔点为金刚石>碳化硅>晶体硅;
②因为金刚石属于面心立方晶胞,即C原子处在立方体的8个顶点,6个面心,体内有4个,故根据均摊法及BN的化学式可推知,一个晶胞中各含有4个B原子、4个N原子,又因为一个BN的质量是M/NA,而一个晶胞的体积是(361.5×10-10)3cm3,故密度=质量÷体积= gcm-3。
gcm-3。


 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案科目:高中化学 来源: 题型:
【题目】为除去粗盐中的Ca2+、Mg2+、SO42- 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
![]()
(1)判断BaCl2已过量的方法是_______________________________________________。
(2)第④步中,相关的离子方程式是___________________________________________。
(3)若先用盐酸再过滤,将对实验结果产生影响,其原因是______________________________。
(4)为检验精盐纯度,需配制150 mL 0.2 mol/L NaCl(精盐)溶液,下图是该同学转移溶液的示意图,其中的错误是____________________________________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知空气-锌电池的电极反应为锌片:Zn+2OH--2e-=ZnO+H2O;碳棒:O2+2H2O+4e-=4OH-,据此判断
A.锌片负极,被氧化B.锌片负极,被还原
C.石墨正极,被氧化D.石墨正极,被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z的原子序数依次增加。K、L、M均是由这些元素组成的二元化合物,甲、乙分别是元素X、Y的单质,甲是常见的固体,乙是常见的气体。K 是无色气体,是主要的大气污染物之一。0.05 mol/L丙溶液的pH为1,上述物质的转化关系如图所示。下列说法正确的是
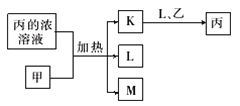
A. K、L、M 中沸点最高的是M
B. 元素的非金属性:Z>Y>X
C. 原子半径:W<X<Y
D. 丙也可由W、Y组成的某化合物与K直接反应制得
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,某饱和氢氧化钠溶液体积为V mL,溶液密度为d g·cm-3,质量分数为w,物质的量浓度为c mol·L-1,溶液中含氢氧化钠的质量为m g,该温度下NaOH的溶解度为S。
(1)用w来表示该温度下氢氧化钠的溶解度(S)为_________________。
(2)用m、V表示溶液中溶质的物质的量浓度(c)为__________________。
(3)用w、d表示溶液中溶质的物质的量浓度(c)为__________________。
(4)用c、d表示溶液中溶质的质量分数(w)为______________________。
(5)用S、d表示溶液中溶质的物质的量浓度(c)为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】扁桃酸衍生物是重要的医药中间体,以A和B为原料合成扁桃酸衍生物F路线如下:

(1) A的分子式为C2H2O3,可发生银镜反应,且具有酸性,A所含官能团名称为:__________。写出A+B→C的化学反应方程式为_______________。
(2) C中3个—OH的酸性有强到弱的顺序是:_____________。
C中3个—OH的酸性有强到弱的顺序是:_____________。
(3)E是由2分子C生成的含有3个六元环的化合物,E的分子中不同化学环境的氢原子有________种。
(4)D→F的反应类型是_________, 1 mol F在一定条件下与足量NaOH溶液反应,最多消耗NaOH的物质的量为______________mol。写出符合下列条件的F的所有同分异构体(不考虑立体异构)的结构简式:____________________。
①属于一元酸类化合物,②苯环上只有2个取代基且处于对位,其中一个是羟基
(5)己知: ![]()
A有多种合成方法,在方框中写出由乙酸合成A的路线流程图(其他原料任选)合成路线流程图示例如下:![]() _________________________________________
_________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】M是一种新型可生物降解的高分子材料,主要制造可降解纤维、塑料和医用材料,其水解最终产物为N。燃烧9.0 g的N只产生CO2和H2O,且质量分别为13.2 g和5.4 g,实验测得N在标准状况下的蒸气密度为4.02 g/L;N的核磁共振氢谱显示的峰面积之比为 1:1:1: 3
(1)通过计算确定N的分子式。____________
(2)由题知写出N的结构简式,并写出N在催化剂条件下缩聚反应合成M的化学方程式。_________________、__________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出下列反应的离子方程式。
(1)普通泡沫灭火器内的玻璃筒里盛硫酸铝溶液,铁筒里盛碳酸氢钠溶液,其化学反应的原理是________________________。
(2)对于易溶于水的正盐MnRm溶液,若pH>7,其原因是___________________。
(3)在25℃下,向0.1 L 0.002 molL1 的NaCl溶液中逐滴加入0.1 L 0.002 molL1硝酸银溶液,有白色沉淀生成向反应后的浊液中继续加入0.1 L0.002 molL1的NaI溶液,看到白色沉淀转化为黄色沉淀,产生该现象的原因用是_______________________________________。(已知:25℃时Ksp(AgCl)=1.6×10-10,Ksp(AgI)=1.5×10-16)
(4)向盛有少量草酸溶液的试管中滴加几滴酸性KMnO4溶液,震荡,溶液紫色褪去的原因是_____________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com