
����Ŀ�����ᴿ���������ơ�̼����淋��Ȼ��ƹ��壬ijѧ����������·�����

����ݲ������̻ش��������⣺
��1���������ڼ���ʱӦѡ��___ʢװ�����(����������)��
��2�����в����ں��ж�SO42�ѳ�����ȫ�ķ�����___��
��3�������۵Ļ�ѧ����ʽΪ___��
��4�������ܵ�Ŀ����___��
��5��ʵ���ҽ��в����ݵľ��岽����___��
��6��ijͬѧ�����Ƶõ��Ȼ��ƹ�������100mL0.2molL1���Ȼ�����Һ��
������NaCl��Һʱ���õ�����Ҫ������������ƽ��ҩ�ס��ձ�������������Ͳ��__��__��
�����в�����ʹ�����Ȼ�����ҺŨ��ƫС����___(�������)��
A����ˮ����ʱ���ӿ̶���
B������ƿ�ڱڸ���ˮ���δ���ﴦ��
C�����ܽ������������Һ�彦���ձ���
D���ߵ�ҡ�Ⱥ��ְ�Һ����ڿ̶����ּ�ˮ����
���𰸡����� ���ã����ϲ���Һ��ά���μ�BaCl2��Һ���������ֻ��ǣ���SO42-�ѳ�����ȫ BaCl2+Na2CO3=BaCO3��+2NaCl ��ȥ�ܽ�����Һ�й�����HCl��CO2 ����Һ�����������У��������������ò��������Ͻ��裬�����������г��ֽ϶����ʱ��ֹͣ���ȣ����������������ʹ��Һ���� ��ͷ�ι� 100mL����ƿ CD
��������
���������ơ�̼����淋��Ȼ��ƹ��壬�����̿�֪�����з������������·ֽⷴӦ���ֽ��Ĺ�������ˮ�����Ȼ�����Ӧ��ȥ��������ӣ�������̼���Ƴ�ȥ�����ı����ӣ����˺���Һ�к�NaCl��̼���ƣ��������ȥ̼���ƺ�����ΪNaCl�������õ�������NaCl���Դ˽����⡣
��1�����ȹ��壬Ӧ�������н��У��ʴ�Ϊ��������
��2����������Ȼ�����Һ��ȥ��������ӣ����������������ȫ���������жϷ���Ϊȡ�����ں����Һ������һ�Թ��У����ã����ϲ���Һ��ά���μ�BaCl2��Һ���������ֻ��ǣ���SO42�ѳ�����ȫ��
�ʴ�Ϊ�����ã����ϲ���Һ��ά���μ�BaCl2��Һ���������ֻ��ǣ���SO42�ѳ�����ȫ��
��3�������ڷ�����Ӧ�����ӷ���ʽΪBaCl2+Na2CO3=BaCO3��+2NaCl��
��4��������У��ɳ�ȥ�ܽ�����Һ�й�����HCl��CO2���ʴ�Ϊ����ȥ�ܽ�����Һ�й�����HCl��CO2��
��5�����Ȼ�����Һ�õ������Ȼ��ƣ��ɽ���Һ�����������У��������������ò��������Ͻ��裬�����������г��ֽ϶����ʱ��ֹͣ���ȣ����������������ʹ��Һ���ɣ�
�ʴ�Ϊ������Һ�����������У��������������ò��������Ͻ��裬�����������г��ֽ϶����ʱ��ֹͣ���ȣ����������������ʹ��Һ���ɣ�
��6����ʵ��������100mL0.2mol��L1���Ȼ�����Һ��Ӧѡ��100mL������ƿ���õ��������У�������ƽ��ҩ�ס��ձ�������������Ͳ��100mL����ƿ����ͷ�ιܣ�
�ʴ�Ϊ����ͷ�ιܡ�100mL����ƿ��
��A����ˮ����ʱ���ӿ̶��ߣ��������ƫС����Ũ��ƫ��A����
B������ƿ�ڱڸ���ˮ���δ���ﴦ������ʵ����Ӱ�죬��B����
C�����ܽ������������Һ�彦���ձ��⣬�������ʵ����ʵ���ƫС����Ũ��ƫС����C��ȷ��
D���ߵ�ҡ�Ⱥ��ְ�Һ����ڿ̶����ּ�ˮ���ϣ��������ƫ����Ũ��ƫС����D��ȷ��
�ʴ�Ϊ��CD��


 �»ƸԱ����ܾ�ϵ�д�
�»ƸԱ����ܾ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��KMnO4��ʵ���Һ�ҵ�Ͼ�����ҪӦ�ã��乤ҵ�Ʊ��IJ��ֹ������£�
�����̿���Ҫ�ɷ�MnO2���������KOH�����ϣ�ͨ�������ֱ��գ����ɰ���ɫ����̬���ʡ�
����ȴ����������ϸ����ϡKOH��Һ��ȡ�����ˣ��ð���ɫ��Һ��
������ɫ��Һ��ͨ��CO2����Һ��Ϊ�Ϻ�ɫ��ͬʱ���ɺ�ɫ���塣
�������ˣ����Ϻ�ɫ��Һ����Ũ������ȴ�ᾧ�����ˣ�ϴ�ӣ������KMnO4���塣
���ϣ�K2MnO4Ϊ����ɫ���壬��ǿ������Һ���ȶ����ڽ����Ի�������Һ�������绯��Ӧ��Mn�Ļ��ϼۼ������ֽ��ͣ���
��1�����У��������̿��Ŀ����___________________��
��2�����У�����K2MnO4�Ļ�ѧ����ʽ��______________________________��
��3�����У���ȡʱ��ϡKOH��Һ��ԭ����_________________��
��4�����У�CO2��K2MnO4����Һ�з�Ӧ�Ļ�ѧ����ʽ��_____________________��
��5����K2MnO4��Һ���ö��Ե缫��Ĥ����⣬Ҳ���Ƶ�KMnO4��װ����ͼ��

��b����______�������������������D��_______________��
�ڽ�ϵ缫��Ӧʽ��������KMnO4��ԭ����_______________________________��
�۴�ͳ��Ĥ�����ʱ����Ԫ��������ƫ�ͣ���֮��ȣ��������ӽ���Ĥ���������Ԫ�ص������ʣ���ԭ����______��
��6���õζ����ⶨij������ز�Ʒ�Ĵ��ȣ��������£�
��֪��Na2C2O4+H2SO4=H2C2O4+Na2SO4��5H2C2O4+2MnO4-+6H+=2Mn2++10CO2��+8H2O��Ħ��������Na2C2O4134gmol-1��KMnO4158gmol-1��
������ȡag��Ʒ�����50mL��Һ��
������ȡbgNa2C2O4��������ƿ�У�������ˮʹ���ܽ⣬�ټ�����������ᡣ
��������ƿ����Һ���ȵ�75�桫80�棬���£��â���������Һ�ζ����յ㣬������ҺVmL�����ʲ����뷴Ӧ����
�ζ��յ������Ϊ_______________����Ʒ��KMnO4�����������ı���ʽΪ_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ȼ��������еķ�ɢ������ʵ������һ�����ɺܶ���AgCl����϶��ɵļ����壬��ʢ��NaCl��Һ���Թ��еμ�AgNO3��Һ�����ú���һ���������Թܣ������Թܵ�������ͬ������ֻ��һ������������ԵĶ�������������з�����ȷ����

A����������A����������AgCl��ֱ����С
B����������B����������AgCl��ֱ������A��C֮��
C����������C����������AgCl��ֱ�����
D��������AgCl�Ĵ�С��ͬ����ֻ��B�����з�ɢ�ʵĴ�С����1~100nm֮��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA���������ӵ�������ֵ�������й�˵����ȷ����
A. 60g�����ᾧ���У�����������ĿΪNA
B. ��״���£�22.4LCCl4�к��з��ӵ���ĿΪNA
C. �����£�46gNO2��N2O4��������к�������ΪNA
D. 32gCuͶ��300mL10mol/L��Ũ�����У���ַ�Ӧ��ת�Ƶ�����ΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪������R2��ԭ�Ӻ�����n�����ӣ�Rԭ�ӵ�������Ϊm����wgR2�����е��ӵ����ʵ����ǣ� ��
A.![]() molB.
molB.![]() molC.
molC.![]() molD.
molD.![]() mol
mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ���ҿ��������᳧¯������Ҫ�ɷ�Ϊ���������P����FeS��SiO2�ȣ��Ʊ��������̷���FeSO47H2O���������Ļ�ѧʽΪ[Fe2(OH)n(SO4)3��0.5n]m���Ʊ�������ͼ��ʾ������˵������ȷ����
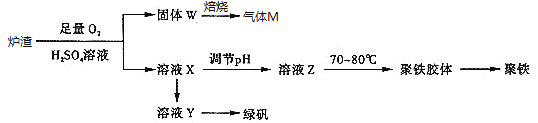
A. ¯����FeS������������ķ�Ӧ�����ӷ���ʽΪ��4FeS+3O2+12H+��4Fe3++4S��+6H2O
B. ����M�ijɷ���SO2��ͨ��˫��ˮ�õ����ᣬ��ѭ��ʹ��
C. ����ҺX�м���������ۣ���ַ�Ӧ����˵õ���ҺY���پ�����Ũ������ȴ�ᾧ�����˵Ȳ���õ��̷�
D. ��ҺZ��pHӰ�������������������������pHƫС�������¾�����������������ƫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ҵ������в�ͬ�Ļ�ѧ����ͼ�������Ҵ��ڸ��ַ�Ӧ�ж��Ѽ���˵������ȷ����

A. �Ҵ����Ʒ�Ӧ�����ٶ���
B. ��ͭ���º�O2��Ӧ�����٢۶���
C. Ũ���������¼�����170��ʱ�ķ�Ӧ�����ڢݶ��ѡ�
D. Ũ���������¼�����140��ʱ�ķ�Ӧ�����٢ݶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������CH3CH2OH�������Ʊ�1��2-����������������������������Ҵ��Ʊ�1��2-���������װ������ͼ��ʾ��
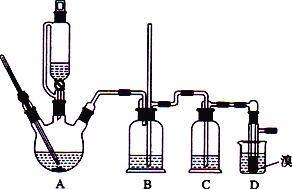
�й������б����£�
�������� | �Ҵ� | 1��2-�������� | ���� |
״̬ | ��ɫҺ�� | ��ɫҺ�� | ��ɫҺ�� |
�ܶ�/(g��cm��3) | 0.79 | 2.2 | 0.71 |
�е�/�� | 78.5 | 132 | 34.6 |
�۵�/�� | ��130 | 9 | ��116 |
�ش��������⣺
(1)װ��A�з����Ļ�ѧ����ʽΪ_________________________________����Ӧ����Ϊ________���ڴ��Ʊ�ʵ���У�Ҫ������Ѹ�ٵذѷ�Ӧ�¶���ߵ�170 �����ң�������ҪĿ����________(����ĸ)��
a ������Ӧ�� b���ٸ������������� c ��ֹ�Ҵ��ӷ� d�ӿ췴Ӧ����
(2)��װ��C��Ӧ����________(����ĸ)����Ŀ�������շ�Ӧ�п������ɵ��������塣
a��ˮ b��Ũ���� c������������Һ d������̼��������Һ
(3) װ��D��ʵ������Ϊ_______________��
(4)��1��2-��������ֲ�Ʒ���ڷ�Һ©���м�ˮ�����ã�����Ӧ��________(����������������)�㡣
(5)��Ӧ������Ӧ����ˮ��ȴװ��D������ҪĿ����____________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Թ��ǻ�ѧʵ������õIJ������������Թܼ���ʱ�����в�����ȷ���ǣ� ��
A.�Թ������ˮ�鲻һ��Ҫ���ɣ�����ʱ����Ȼ�ӷ�
B.Ӧ�ս��ԹܼУ���Ĵָ���ڶ̱���
C.�Թ���Һ��������ܳ����Թ��ݻ���1/3
D.����ʹ�Թܵ����Ȳ�λ�ڻ����Ϸ��������ƶ������м���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com