
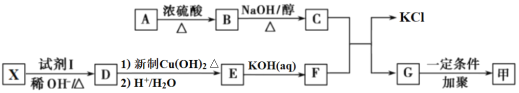
����Ŀ���л��߷��ӻ��������һ�ֳ��õĹ����߷��Ӳ��ϣ���ṹ��ʽΪ��![]() ����A��XΪԭ�ϣ����������̿��Ժϳɼף������Լ�I����һ��������Ȳ����ˮ��Ӧ�Ƶã��Լ�X������ͼ��ʾ���ķ�ֵΪ106��
����A��XΪԭ�ϣ����������̿��Ժϳɼף������Լ�I����һ��������Ȳ����ˮ��Ӧ�Ƶã��Լ�X������ͼ��ʾ���ķ�ֵΪ106��
��֪��a.��CH2OH+��CH2OH![]() ��CH2OCH2��+H2O
��CH2OCH2��+H2O
b.![]() +
+![]() +H2O
+H2O
c.�ǻ�ֱ������̼̼˫����̼����һ�ֲ��ȶ��Ľṹ���������������ŴӶ�ת��Ϊ�ȶ��ṹ��![]()
��ش��������⣺
��1����֪A��������Ԫ�ص���������Ϊ19.88%��̼Ԫ�ص���������Ϊ29.81%������Ϊ��Ԫ�غ���Ԫ�أ���A�ĺ˴Ź������������������շ壬�����֮��Ϊ2��2��1����A�Ľṹ��ʽΪ___��
��2������˵������ȷ����___��
A.�л���A�ܷ���ˮ�ⷴӦ����ˮ���������������������Ŀ�����
B.�л���X������������Na���ʷ����û���Ӧ��ͬ���칹����
C.�л���G�ķ���ʽΪC13H14O3���ܷ���ȡ�����ӳɡ���������ԭ���Ӿ۷�Ӧ
D.�л���D���������4ԭ�ӹ��ߣ�������ԭ�Ӿ����ܹ���
��3��д��B��C�Ļ�ѧ����ʽ��___��
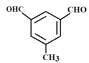
��4��H��E��ͬ���칹�壬д����������������H�Ľṹ��ʽ___��
��1molH������������Cu(OH)2��ַ�Ӧ����2molCu2O��
��H�ĺ˴Ź��������Ϲ����ĸ����շ塣
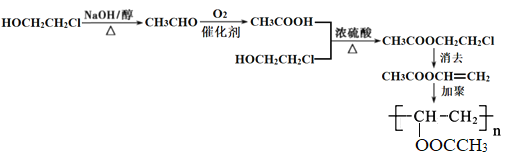
��5����������ϩ��(PVAc)��һ�����߷��Ӳ��ϣ��������ȶ�������ճ��ǿ�ȸߣ���һ�ֻ����Ľ����������AΪԭ���Ʊ���������ϩ��������___��
���𰸡�HOCH2CH2Cl B ClCH2CH2OCH2CH2Cl+NaOH��ClCH2CH2OCH=CH2+NaCl+H2O 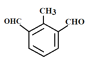 ��
��
��������
Gͨ���Ӿ۷�Ӧ���ɸ߷��ӻ�����ף��ɼĽṹ��֪��GΪ![]() ����֪A��������Ԫ�ص���������Ϊ19.88%��̼Ԫ�ص���������Ϊ29.81%������Ϊ��Ԫ�غ���Ԫ�أ���A�ĺ˴Ź������������������շ壬�����֮��Ϊ2��2��1���������̽����֪��Ϣa��G�Ľṹ��ʽ��֪A����B���ǻ��ķ��Ӽ���ˮ��Ӧ��B����C����ԭ�ӵ���ȥ��Ӧ�����Ը���G�Ľṹ��ʽ��֪A��HOCH2CH2Cl��B��ClCH2CH2OCH2CH2Cl��C��ClCH2CH2OCH��CH2������F�Ľṹ��ʽΪ
����֪A��������Ԫ�ص���������Ϊ19.88%��̼Ԫ�ص���������Ϊ29.81%������Ϊ��Ԫ�غ���Ԫ�أ���A�ĺ˴Ź������������������շ壬�����֮��Ϊ2��2��1���������̽����֪��Ϣa��G�Ľṹ��ʽ��֪A����B���ǻ��ķ��Ӽ���ˮ��Ӧ��B����C����ԭ�ӵ���ȥ��Ӧ�����Ը���G�Ľṹ��ʽ��֪A��HOCH2CH2Cl��B��ClCH2CH2OCH2CH2Cl��C��ClCH2CH2OCH��CH2������F�Ľṹ��ʽΪ![]() ��E�Ľṹ��ʽΪ
��E�Ľṹ��ʽΪ![]() ��D�Ľṹ��ʽΪ
��D�Ľṹ��ʽΪ![]() ���Լ�I����һ��������Ȳ����ˮ��Ӧ�Ƶã��Լ�X������ͼ��ʾ���ķ�ֵΪ106������Է���������106��������֪��Ϣb���D�Ľṹ��ʽ��֪X�Ľṹ��ʽΪ
���Լ�I����һ��������Ȳ����ˮ��Ӧ�Ƶã��Լ�X������ͼ��ʾ���ķ�ֵΪ106������Է���������106��������֪��Ϣb���D�Ľṹ��ʽ��֪X�Ľṹ��ʽΪ![]() ���Լ�I�Ľṹ��ʽΪCH3CHO���ݴ˽��
���Լ�I�Ľṹ��ʽΪCH3CHO���ݴ˽��
��1���������Ϸ�����֪A�Ľṹ��ʽΪHOCH2CH2Cl��
��2��A.�л���A������ԭ�ӣ��ܷ���ˮ�ⷴӦ����ˮ��������Ҷ����������������������Ŀ�������A��ȷ��B.�л���X�DZ���ȩ������������Na���ʷ����û���Ӧ��ͬ���칹���ڣ�B����C.GΪ![]() ���л���G�ķ���ʽΪC13H14O3�����б�����̼̼˫�����������ܷ���ȡ�����ӳɡ���������ԭ���Ӿ۷�Ӧ��C��ȷ��D.�л���D�DZ���ȩ�����������4ԭ�ӹ��ߣ�������ԭ�Ӿ����ܹ��棬D��ȷ����ѡB��
���л���G�ķ���ʽΪC13H14O3�����б�����̼̼˫�����������ܷ���ȡ�����ӳɡ���������ԭ���Ӿ۷�Ӧ��C��ȷ��D.�л���D�DZ���ȩ�����������4ԭ�ӹ��ߣ�������ԭ�Ӿ����ܹ��棬D��ȷ����ѡB��
��3��B��C�Ļ�ѧ����ʽΪClCH2CH2OCH2CH2Cl+NaOH��ClCH2CH2OCH=CH2+NaCl+H2O��
��4��E�Ľṹ��ʽΪ![]() ��H��E��ͬ���칹�壬��1molH������������Cu(OH)2��ַ�Ӧ����2molCu2O������2��ȩ������H�ĺ˴Ź��������Ϲ����ĸ����շ壬��˷��������Ľṹ��ʽΪ
��H��E��ͬ���칹�壬��1molH������������Cu(OH)2��ַ�Ӧ����2molCu2O������2��ȩ������H�ĺ˴Ź��������Ϲ����ĸ����շ壬��˷��������Ľṹ��ʽΪ ��
�� ��
��
��5��A��HOCH2CH2Cl���������Ʒ������֪��Ϣ��֪�����AΪԭ���Ʊ���������ϩ��������Ϊ ��
��


 �����߿����ϵ�д�
�����߿����ϵ�д� �㾦�½̲�ȫ�ܽ��ϵ�д�
�㾦�½̲�ȫ�ܽ��ϵ�д� Сѧ�̲���ȫ���ϵ�д�
Сѧ�̲���ȫ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼Ԫ�����γɵ��ʼ��仯������������Ԫ�ء��ش��������⣺
��1��̼�����⡢����������Ԫ�ع��ɻ�����CO(NH2)2���÷����и�Ԫ�صĵ縺���ɴ�С��˳��Ϊ_________������Cԭ�ӵ��ӻ���ʽΪ__________��������������ˮ����Ҫԭ����_______________��
��2��CO��̼Ԫ�صij����������N2��Ϊ�ȵ����壬��CO�ĽṹʽΪ_______��CO���Ժͺܶ���ɽ����γ�������Ni(CO)4��д����̬Niԭ�ӵĵ����Ų�ʽ__________��
��3��̼��ij�־���Ϊ��״�ṹ���������ڽ��������á���ԭ������ڸ���֮�䣬�γɼ�϶������䳣���ṹ��ƽ��ͶӰ��ͼ����ʾ�����仯ѧʽ�ɱ�ʾΪ__________

��4��ͼ��Ϊ̼��һ��ͬ��������C60���ӣ�ÿ��C60�����к�����������ĿΪ________��
��5��ͼ��Ϊ̼����һ��ͬ����������ʯ�ľ���������ԭ���������AΪ��0��0��0����BΪ��1/2��0��1/2����CΪ��1/2��1/2��0������Dԭ�ӵ��������Ϊ__________��
��6��������������Ľṹ����ʯ���ƣ�Ӳ������ʯ�൱�������߳�Ϊ361.5 pm��������������ܶ���___________g���M-3���г�����ʽ���ɣ������ӏ�����ΪNA����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ŀǰ��ҵ�ϴ����л���ˮ��һ�ַ����ǣ��ڵ��ں�pH��Mn2��Ũ�ȵķ�ˮ�м���H2O2��ʹ�л����������⡣��������¶Ա�ʵ�飨ʵ���������±�)��ʵ�����л���RŨ����ʱ��仯�Ĺ�ϵ����ͼ��ʾ������˵����ȷ����
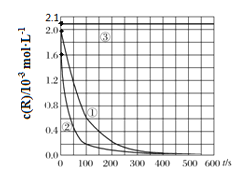
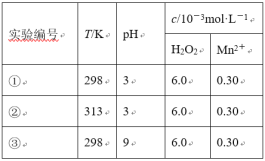
A.313Kʱ����0~100s���л���R�����ƽ������Ϊ��0.014 mol��L-1��s-1
B.�ԱȢ٢�ʵ�飬���Եó��¶�Խ��Խ�������л���R�Ľ���
C.�ԱȢ٢�ʵ�飬���Է���������ʵ�����л���R�Ľ���ٷ��ʲ�ͬ
D.ͨ����������ʵ�飬����ʹ��Ӧֹͣ��������Ӧ��ϵ�м���һ������NaOH��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Ҫ����Ԥ��ͬ������������ų���Ӧ����ṹ��ʽ����ͼ��ʾ��
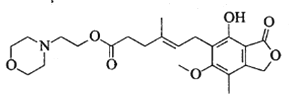
����˵����ȷ����
A. ���������ķ���ʽΪC23H30O7N
B. ���������ɷ����ӳɡ�ȡ������ȥ��Ӧ
C. ������������������̼ԭ��һ������ͬһƽ��
D. 1mol����������NaOH��Һ��ַ�Ӧ�������3mol NaOH��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧϰС��̽�����Ļ�ԭ�Լ������������ʣ�����ͼװ�ý���ʵ��(ͼ�мг�װ������ȥ)����B�����������������������ȣ��ٹ����������֪����ˮ�Ȼ��ƿ����հ�����ˮ���ش��������⣺
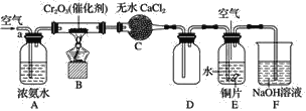
(1)B�з�����Ӧ�Ļ�ѧ����ʽ��______________________________��
(2)֤������������������������________________����Ӧ�ķ���ʽ��________________��
(3)E��ͭ������Ӧ�����ӷ���ʽ��________________________________��
(4)E�л���ͨ�������Ŀ����____________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о���ѧϰС������ȷ�Ӧʵ��չ���о����ԡ����ȷ�Ӧ��������������������������Ӧ�ų��������ȣ�������ҫ�۵Ĺ�â����ֽ©�����²����մ���������������ɳ�С�����֪Al��Al2O3��Fe��Fe2O3���ۡ��е����������
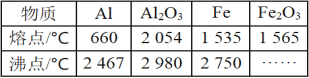
��1��ijͬѧ�Ʋ⣬���ȷ�Ӧ���õ�������������������Ͻ�������___��
��2��ijͬѧ�������Ӧ�ų��������ȣ�������ҫ�۵Ĺ�â���������п���ֻ�Ƿ����������ʵ�ȼ�շŴ����ȡ������û�ѧ�������ʵ����֤���ȷ�Ӧ�ķ�����___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�A�dz����Ľ������ʡ�����B�ǻ���ɫ���塢����C����ɫ���塣�ں��ʷ�Ӧ�����£����ǿ��������ͼ���з�Ӧ��E��Һ����ɫ��Һ��F�ǵ���ɫ��Һ��B��C��Ӧ������ɫ���档��ش�:
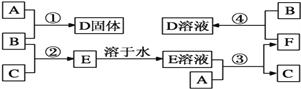
(1)A��_________��B��_________��C��_________![]() ��д��ѧʽ
��д��ѧʽ![]() ��
��
(2)��Ӧ�ٵĻ�ѧ����ʽ ______________________________________��
(3)��Ӧ�۵����ӷ���ʽ _____________________________________��
(4)��Ӧ�ܵ����ӷ���ʽ ______________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��CΪ��ѧ�������ʣ�����һ��Ϊ������ͨ������£�AΪ���壬B��C��Ϊ���塣D��E��F��G��H��X��Ϊ���������X��һ������ǿ�ᡢEΪ��ɫ���壬H�ڳ�����ΪҺ�塣����֮���ת����ϵ��ͼ��ʾ(����ijЩ��Ӧ�����Ͳ��ַ�Ӧ������ȥ)��
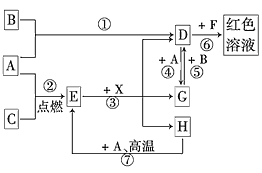
��1���ڷ�Ӧ�١����У�������������ԭ��Ӧ����________(����)��
��2��д���۵����ӷ���ʽ��________________
��3����Ӧ�ߵĻ�ѧ����ʽΪ____���÷�Ӧ��ÿ����0.3 mol��A����ת�Ƶ���_________mol���ڽ������ʱ�Ĺؼ�һ����____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������֮�������·�Ӧ��ϵ��
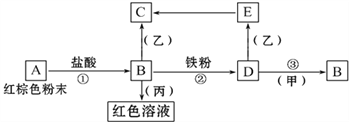
��֪��Eת����C�������ǣ��Ұ�ɫ����Ѹ�ٱ�Ϊ����ɫ������Ϊ���ɫ��
�ش�
��1�� д���������ʵĻ�ѧʽ��A______B______D________��_______��_______��__________
��2�� д��E��C��Ӧ�Ļ�ѧ����ʽ��_____________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com