
����Ŀ����һ��������ܱ������У��������»�ѧ��Ӧ��CO��g��+H2O ��g��CO2��g��+H2��g�����仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ�����
t�� | 700 | 800 | 830 | 1000 | 1200 |
K | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
�ش��������⣺
��1���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK= �� �÷�ӦΪ��Ӧ�������Ȼ���ȣ������ı�����ʹƽ��������Ӧ�����ƶ�����ƽ�ⳣ��������ţ�
��һ������ ��һ����С �ۿ������� ������С��������п���
��2�����жϸ÷�Ӧ�Ƿ�ﵽ��ѧƽ��״̬�������� ��
��a��������ѹǿ���� ��b�����������c��CO������
��c��v����H2��=v����H2O�� ��d��c��CO��=c��CO2��
��3������ͬ����CO ��g�� ��H2O ��g�� �ֱ�ͨ�뵽���Ϊ2L�ĺ����ܱ������У����з�ӦCO ��g��+H2O ��g��CO2��g��+H2��g�����õ�����������ݣ�
ʵ���� | �¶�/�� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min | ||
H2O | CO | CO2 | CO | |||
A | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
B | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
C | 1000 | 1 | 2 | c | d | t |
��ʵ��B��ƽ��ʱH2O ��g�������ʵ����� ��
��ͨ�������֪��CO��ת����ʵ��Aʵ��B������ڡ��������ڡ���С�ڡ�����
����ʵ��C�дﵽƽ������ʱ�� t3������ڡ��������ڡ���С�ڡ���
���𰸡�
��1��![]() �����ȣ���
�����ȣ���
��2��bc
��3��0.6mol�����ڣ�С��
���������⣺��1����Ӧ�Ļ�ѧ����ʽΪCO��g��+H2O ��g��CO2��g��+H2��g������K= ![]() ���ɱ������ݿ�֪�����¶�ƽ�ⳣ����С��˵������Ӧ���ȣ�ƽ�������ƶ������¶Ȳ��䣬��ƽ�ⳣ�����䣬�罵�£���ƽ�ⳣ�����������ƶ���ƽ�ⳣ�������ܼ�С��ֻ�Т���ȷ�����Դ��ǣ�K=
���ɱ������ݿ�֪�����¶�ƽ�ⳣ����С��˵������Ӧ���ȣ�ƽ�������ƶ������¶Ȳ��䣬��ƽ�ⳣ�����䣬�罵�£���ƽ�ⳣ�����������ƶ���ƽ�ⳣ�������ܼ�С��ֻ�Т���ȷ�����Դ��ǣ�K= ![]() �� ���ȣ��ۣ���2����a����Ӧǰ�������������䣬�����Ƿ�ﵽƽ��״̬��������ѹǿ�����䣬�����ж��Ƿ�ﵽƽ��״̬���ʴ���
�� ���ȣ��ۣ���2����a����Ӧǰ�������������䣬�����Ƿ�ﵽƽ��״̬��������ѹǿ�����䣬�����ж��Ƿ�ﵽƽ��״̬���ʴ���
��b�����������c��CO�����䣬��˵���ﵽƽ��״̬������ȷ����c��v����H2��=v����H2O����˵�����淴Ӧ������ȣ��ﵽƽ��״̬������ȷ����d��c��CO��=c��CO2��������˵���Ƿ�ﵽƽ��״̬���ʴ������Դ��ǣ�b c����3����ʵ��B��ƽ��ʱCO2�����ʵ���Ϊ0.4mol����֪����0.4molH2O���ɼ���ƽ��ʱH2O ��g�������ʵ���Ϊ1mol��0.4mol=0.6mol�����Դ��ǣ�0.6mol����ʵ��A��CO��ת����Ϊ ![]() =0.8��ʵ��B��CO��ת����Ϊ
=0.8��ʵ��B��CO��ת����Ϊ ![]() =0.2����A��ת���ʴ���B�����Դ��ǣ����ڣ���B��C��Ƚϣ�������ʼ���ʵ�����ͬ����C���¶Ƚϸߣ���Ӧ���ʽϴ���C�õ�ʱ���С�����Դ��ǣ�С�ڣ�
=0.2����A��ת���ʴ���B�����Դ��ǣ����ڣ���B��C��Ƚϣ�������ʼ���ʵ�����ͬ����C���¶Ƚϸߣ���Ӧ���ʽϴ���C�õ�ʱ���С�����Դ��ǣ�С�ڣ�
�����㾫����������Ҫ�����˻�ѧƽ��״̬���ʼ������ͻ�ѧƽ��״̬���жϵ����֪ʶ�㣬��Ҫ���ջ�ѧƽ��״̬�����������ȡ��� V��=V��>0�����������Ƕ�̬ƽ�⣬ƽ��ʱ��Ӧ���ڽ��У�����������Ӧ������и���ְٷֺ������䣻���䡱�������ı䣬ƽ�ⱻ���ƣ������µ������½����µĻ�ѧƽ�⣻��;���أ�����������䣬���淴Ӧ�����Ǵ�����Ӧ��ʼ�����Ǵ��淴Ӧ��ʼ�����ɽ���ͬһƽ��״̬����Ч����״̬�жϣ���v(B��)=v(B��)��v(C��):v(D��)=x : y��c(C)��C%��n(C)%�Ȳ������A��B��C��DΪ���壬��m+n��x+y��ѹǿ�㶨����ϵ��ɫ�����λʱ����ij�����ڻ�ѧ���Ķ����������γ�������ϵƽ��ʽ���㶨��m+n �� x+y���Ȳ�����ȷ�����⣮


 ״Ԫ��ȫ��ͻ�Ƶ�����ϵ�д�
״Ԫ��ȫ��ͻ�Ƶ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ����ʱ���������ɫ�̵���
A.��������Cl2��ȼ��B.����������ȼ��
C.������������ȼ��D.����������ȼ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ����������ԭ��Ӧ���ǣ� ��
A.CaCO3+2HCl=CaCl2+H2O+CO2��
B.Na2O+H2O=2NaOH
C.CaCO3=CaO+CO2��
D.Mg+2HCl=MgCl2+H2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������繤ҵ���õķ�չ���˿ڵľ�����ȫ����Դ���ż�������������Խ��Խ���ص����⣬��ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2������ȫ������ձ����ӣ�
��1����ͼΪC����������ı仯��ϵͼ�����ٱ仯���û���Ӧ�����仯ѧ����ʽ��Ϊ�� 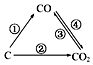
��2����ú��Ϊȼ�Ͽ�ͨ����������;����
;����C��s��+O2��g���TCO2��g����H1��0����
;�������Ƴ�ˮú����C��s��+H2O��g���TCO��g��+H2��g����H2��0����
��ȼ��ˮú����2CO��g��+O2��g���T2CO2��g����H3��0����
2H2��g��+O2��g���T2H2O��g����H4��0����
��;����ų�������������ڡ��������ڡ���С�ڡ���;����ų���������
��3���״���һ�ֿ�������Դ�����п�����Ӧ�õĹ���ǰ������֪��Ӧ2CH3OH��g��CH3OCH3��g��+H2O��g��ij�¶��µ�ƽ�ⳣ��Ϊ400�����¶��£����ܱ������м���CH3OH����Ӧ��ijʱ�̲�ø���ֵ�Ũ�����£�
���� | CH3OH | CH3OCH3 | H2O |
Ũ��/ | 0.44 | 0.6 | 0.6 |
�Ƚϴ�ʱ�����淴Ӧ���ʵĴ�С��v��v�����������������=������
��4������Һ����ʾ���Ĺ�����ʹ�õĻ�ѧ��ϴ��NF3��һ���������壬��洢������������CO2��12 000��20 000�����ڴ����е������ɳ���740��֮�ã������Ǽ��ֻ�ѧ���ļ��ܣ�
��ѧ�� | N��N | F��F | N��F |
����/kJmol��1 | 941.7 | 154.8 | 283.0 |
��ӦN2��g��+3F2��g���T2NF3��g���ġ�H=
��5��25�桢101kPaʱ����֪��
2H2O��g���TO2��g��+2H2��g����H1
Cl2��g��+H2��g���T2HCl��g����H2
2Cl2��g��+2H2O��g���T4HCl��g��+O2��g����H3
���H3���H1�͡�H2��Ĺ�ϵ��ȷ����
A.��H3=��H1+2��H2
B.��H3=��H1+��H2
C.��H3=��H1��2��H2
D.��H3=��H1����H2
��6�����������ھ�������������ˮ������������ҵ�������ΪƯ�����������������������ҿ������������е��ʷ�Ӧ����6Ag��s��+O3��g��=3Ag2O��s����H=��235.8kJmol��1 ��
��֪��2Ag2O��s��=4Ag��s��+O2��g����H=+62.2kJmol��1 ��
��O3ת��ΪO2���Ȼ�ѧ����ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�����X��Al2O3��Fe2O3��Cu��SiO2�е�һ�ֻ���������ɡ���������ʵ�飬�����й�˵����ȷ���ǣ� ��
![]()
A������I�м��ٵ�3g����һ���ǻ����
B������II���������ٵ�����һ����Cu
C�����ݲ���I��II�����жϻ����X�ijɷ�ΪAl2O3��Fe2O3��Cu��SiO2
D��������������II���Եó�m(Fe2O3)��m(Cu)=1��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һ��ֻ�������������е�ȫ���֣� Ag+��Fe3+��Al3+��H+��SO42-��CO32-��OH-��Cl-��ȡ����Һ������ʵ�飺
�ٹ۲���Һ��ۣ� ��Һ����ɫ��
��ȡ��������Һ����Ba(NO3)2��Һ�� ������
��ȡ����Һ 100 mL����������εμ� 1 mol/L��NaOH��Һ�����������ɳ������ʵ������������ NaOH ��Һ�������ϵ��ͼ��ʾ������ʵ��ش��������⣺
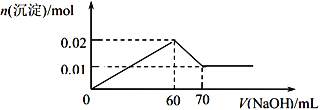
��1��������Һ�������ӵ����ӷ���ʽΪ________________________________��
��2����������ʵ���ƶϣ���Һ�и����ӵ����ʵ���Ũ�ȷֱ�Ϊ________________________________��
��3����ȡ������Һ 100 mL������������ˮ����ˣ��ٽ����ó���ϴ�ӡ����գ����ù������������ʵ���Ϊ_____________mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����100��ʱ����0.200mol�������������������2L��յ��ܱ������У�ÿ��һ����ʱ��Ը������ڵ����ʽ��з������õ������
| 0 | 2 | 4 | 6 | 8 | 10 |
c��N2O4�� | 0.100 | c1 | 0.050 | c3 | a | b |
c��NO2�� | 0.000 | 0.060 | c2 | 0.120 | 0.120 | 0.120 |
����գ�
��1���÷�Ӧ�ﵽƽ��ʱ��������������ת����Ϊ%������c2c3��ab�����������������=������
��2��2minʱ������������Ũ��c1=mol/L����0��2minʱ����ڣ�������������ƽ����Ӧ����Ϊmol/��Lmin����
��3��100��ʱ���÷�Ӧ��ƽ�ⳣ��K=
��4��������ͬ���������������������Ƕ����������壬Ҫ�ﵽ����ͬ����ƽ��״̬��������������ʼŨ����mol/L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������NH4Cl��Ca(OH)2��ȡ��������ͼA��B�dz��õ����巢��װ�á�

��1��ʵ�����ư���ʱ��Ӧ�Ļ�ѧ����ʽ��______________________________________,Ӧѡ�õ�װ����_____;������Ũ��ˮ��NaO�����ư���ʱ��Ӧѡȡ��װ����________��
��2��Ϊ�˵õ�����İ�����ʵ���ҳ�ʹ��________�����������Ӽ�ʯ�ҡ�Ũ���ᡢ�Ȼ�����ѡ��һ�����ʣ���
��3��ʵ���ҳ���_______���ռ��������ڱ�״���£���ʢ�������ļ���ƿ������ˮ��(��������ȫ���ڼ���ƿ��)����������Һ�����ʵ���Ũ��Ϊ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ƭ�����������ð֢״����ṹ��ʽ��ͼ�������й�˵��������ǣ� �� 
A.����ҵķ���ʽΪC13H18O2
B.������뱽������ͬϵ��
C.1mol ������������3mol ���������ӳɷ�Ӧ
D.������ڱ����Ϸ���ȡ����Ӧ����һ�ȴ�����4��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com