
【题目】下列各组离子中,能大量共存且加入(或通入)X试剂后发生反应的离子方程式对应正确的是
选项 | 离子组 | 试剂X | 离子方程式 |
A | Fe3+、Al3+、 | 过量的盐酸 |
|
B | 透明溶液中:Fe3+、 | 过量的铜粉 | 2Fe3++Cu═2Fe2++Cu2+ |
C | Na+、Ba2+、 | NaHSO4溶液 | H++ |
D | pH=1的溶液中:Mg2+、Fe2+、 | 双氧水 | 2Fe2++H2O2+2H+═2Fe3++2H2O |
A.AB.BC.CD.D
【答案】B
【解析】
A.Fe3+、Al3+都与SO32-发生反应,在溶液中不能大量共存,故A错误;
B.透明溶液可能是有色溶液,在透明溶液中这四种离子能大量共存,加入铜粉,铜与铁离子反应,铜不能与亚铁离子反应,发生2Fe3++Cu=2Fe2++Cu2+,故B正确;
C.加入NaHSO4溶液后,Ba2+、与硫酸根离子生成硫酸钡沉淀,正确的离子方程式为:H++SO42-+Ba2++HCO3-=BaSO4↓+CO2↑+H2O,故C错误;
D.酸性环境下硝酸具有强的氧化性,所以pH=1的溶液中,硝酸根离子与二价铁离子不共存,发生反应为3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,故D错误;
答案为B。


 孟建平名校考卷系列答案
孟建平名校考卷系列答案科目:高中化学 来源: 题型:
【题目】某课外活动小组欲利用CuO与NH3反应,研究NH3的某种性质并测定其组成,设计了如下实验装置(夹持装置未画出)进行实验。请回答下列问题:

(1)仪器a的名称为______;仪器b中可选择的试剂为______。
(2)实验室中,利用装置A,还可制取的无色气体是______(填字母)。
A.Cl2 B.O2 C.CO2 D.NO2
(3)实验中观察到装置C中黑色CuO粉末变为红色固体,量气管有无色无味的气体,上述现象证明NH3具有______性,写出相应的化学方程式______。
(4)E装置中浓硫酸的作用______。
(5)读取气体体积前,应对装置F进行的操作:______。
(6)实验完毕,若测得干燥管D增重mg,装置F测得气体的体积为n L(已折算成标准状况),则氨分子中氮、氢的原子个数比为______(用含m、n字母的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关下列装置图的叙述正确的是

A.若X为粗铜,Y为硫酸铜,K接N,则此装置可以精炼铜
B.若X为铜,Y为浓硝酸,K接M,可以形成原电池,则铁为负极
C.若X为锌,则无论K接M还是N,铁都能被保护
D.若X为银,Y为FeCl3,K接N,则此装置可以在铁上镀银
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳基能源的大量消耗使大气中CO2浓度持续不断地增加,以CO2为原料加氢合成,甲烷等能源物质具有较好的发展前景。回答下列问题:
(1)CO2催化(固体催化剂)加氢合成甲烷过程发生以下两个反应:
主反应:CO2(g)+4H2(g)![]() CH4(g)+2H2O(g) △H1=akJ·mol-1
CH4(g)+2H2O(g) △H1=akJ·mol-1
副反应:CO2(g)+H2(g)![]() CO(g)+H2O(g) △H2=41.1kJ·mol-1
CO(g)+H2O(g) △H2=41.1kJ·mol-1
已知相关的化学键键能数据如下:

则a=___。加氢合成甲烷时,通常控制温度为500℃,不能过高也不宜过低的原因是___。
(2)为了提高CO2加氢制CH4过程中CH4选择性(CH4选择性=![]() ×100%),主要是通过对催化剂的合理选择来实现。
×100%),主要是通过对催化剂的合理选择来实现。
①CO2加氢制CH4的一种催化机理如图,下列说法正确的是___(填标号)。
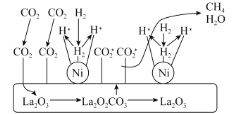
A.催化过程使用的催化剂为La2O3和La2O2CO3
B.La2O2CO3可以释放出CO2*(活化分子)
C.H2经过Ni活性中心裂解产生活化态H*的过程为放热过程
D.CO2加氢制CH4的过程需要La2O3和Ni共同催化完成
②保持500℃不变,向1L密闭容器中充入4molCO2和12molH2发生反应,若初始压强为p,20min后,主、副反应都达到平衡状态,测得此时c(H2O)=5mol·L-1,体系压强变为0.75p,则主、副反应的综合热效应为___,v(CH4)=___mol·L-1·min-1,CH4选择性=___(保留三位有效数字),主反应的平衡常数K=___。
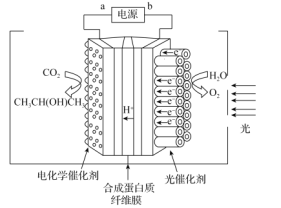
(3)CO2的光电催化反应器如图所示。以TiO2为阳极,通过光解水产生电子和质子,而后传递到阴极(Pt/CNT)诱导阴极催化还原CO2制得异丙醇。
①阴极常伴有析氢等副反应发生,为此选用了电化学催化剂,其依据是___。
②阴极生成异丙醇的电极反应为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在盛有一定量浓硝酸的试管中加入6.4 g铜片发生反应。请回答:
(1)开始阶段,观察到的现象为________________,反应的化学方程式是_____________。
(2)反应结束后,铜片有剩余,再加入少量20%的稀硫酸,这时铜片上又有气泡产生,反应的离子方程式是__________________。
(3)若6.4 g铜片消耗完时,共产生气体2.8 L(标准状况)。则整个反应过程中所消耗的硝酸的物质的量是_____________。
(4)实验室中硝酸通常保存在棕色试剂瓶中,原因是_____________(用化学方程式表示)。
(5)工业上通常用氨催化氧化法制硝酸,写出氨催化氧化的化学方程式:_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家开发设计一种天然气脱硫装置,利用如右图装置可实现:H2S+O2→H2O2 +S。已知甲池中有如下的转化:


下列说法错误的是:
A. 该装置可将光能转化为电能和化学能
B. 该装置工作时,溶液中的H+从甲池经过全氟磺酸膜进入乙池
C. 甲池碳棒上发生电极反应:AQ+2H+ +2e- =H2AQ
D. 乙池①处发生反应:H2S+I3- =3I-+S↓+2H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是一个电化学过程的示意图,回答下列问题:

(1)甲池是_______装置,乙装置中电极A的名称是__________。
(2)甲装置中通入CH4的电极反应式为_______,乙装置中电极B(Ag)的电极反应式为______,丙装置中D极的产物是________(写化学式)。
(3)一段时间,当丙池中产生112 mL(标准状况)气体时,均匀搅拌丙池,所得溶液在25 ℃时的pH=________(已知:NaCl溶液足量,电解后溶液体积为500 mL)。若要使丙池恢复电解前的状态,应向丙池中通入________(写化学式);其物质的量为____________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在298 K、1.01×105 Pa,将22 g CO2通入0.75 L 1.0 mol·L-1NaOH溶液中充分反应,测得反应放出的热量为a kJ。已知该条件下1 mol CO2通入1 L 2.0 mol·L-1NaOH溶液中充分反应放出的热量为b kJ。则CO2与NaOH反应生成NaHCO3的热化学方程式为( )。
A. CO2(g)+NaOH(aq)![]() NaHCO3(aq) ΔH=-(2b-a) kJ·mol-1
NaHCO3(aq) ΔH=-(2b-a) kJ·mol-1
B. CO2(g)+NaOH(aq)![]() NaHCO3(aq) ΔH=+(4a-b) kJ·mol-1
NaHCO3(aq) ΔH=+(4a-b) kJ·mol-1
C. CO2(g)+NaOH(aq)![]() NaHCO3(aq) ΔH=-(4a-b) kJ·mol-1
NaHCO3(aq) ΔH=-(4a-b) kJ·mol-1
D. CO2(g)+NaOH(aq)![]() NaHCO3(aq) ΔH=+(2b-a) kJ·mol-1
NaHCO3(aq) ΔH=+(2b-a) kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~I分别表示中学化学中常见的一种物质,它们之间相互关系如下图所示(部分反应物、生成物没有列出)。已知H为固态氧化物,F是红褐色难溶于水的沉淀,且A、B、C、D、E、F六种物质中均含同一种元素。

请填写下列空白:
(1)A、B、C、D、E、F六种物质中所含的同一种元素的名称是________。
(2)反应①的化学方程式为_____________________________________
反应③的离子方程式为________________________
反应⑧的化学方程式为_____________________________________
(3)反应⑥过程中的现象是______________________________。
(4)1molI发生反应后生成的A高温下与足量的水蒸气反应,生成的气体换算成标准状况下占______L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com