
【题目】某校学生课外活动小组的同学设计如图所示实验装置,用来验证一氧化碳具有还原性,回答下列问题:(提示:C+CO2![]() 2CO C+H2O(g)
2CO C+H2O(g)![]() CO+H2)
CO+H2)

(1)写出装置A中所发生反应的离子方程式:____________。
(2)装置B中最适宜的试剂是________________。
(3)若实验中没有装置C,使装置B与装置D直接相连,会对实验造成的影响是________。
(4)按照如图装置进行实验时,首先进行的操作是__________。
(5)根据实验中的___________现象,可证明CO具有还原性,有关反应的化学方程式是:__________。
(6)若要根据装置F中澄清石灰水变浑浊的现象确认一氧化碳具有还原性,应在图中装置_____与________之间连接图中的________装置(填序号)。
①![]() NaHCO3溶液 ②
NaHCO3溶液 ② 碱石灰 ③
碱石灰 ③![]() NaOH溶液 ④
NaOH溶液 ④![]() 浓H2SO4
浓H2SO4
【答案】CaCO3+2H+═Ca2++H2O+CO2↑ 饱和的碳酸氢钠溶液 没有除去气体中的水蒸气,高温下水蒸气与炭反应生成H2和CO,H2也能还原CuO,从而干扰对CO还原性的验证 检查装置气密性 E装置中黑色CuO变成红色 CO+CuO![]() Cu+CO2 D E ②
Cu+CO2 D E ②
【解析】
本题是探究CO还原性的实验设计题,利用C和CO2反应生成的CO还原氧化铜,结合氧化铜变红色粉末和石灰水变浑浊来推测CO的还原性,但因CO2中混有的水汽也能和C反应生成CO和H2,生成的H2有还原性对实验有干扰,因此CO2必须干燥处理。
(1)装置A中是盐酸和石灰石反应生成二氧化碳、氯化钙和水,其反应离子方程式为:CaCO3+2H+═Ca2++H2O+CO2↑;
(2)实验室用盐酸和石灰石制取二氧化碳,该反应放出的热量导致盐酸挥发,所以制取的二氧化碳中含有氯化氢气体,为除去氯化氢气体,选取的试剂应能除去氯化氢气体且不和二氧化碳反应,则只能选取可溶性的饱和碳酸氢盐,一般常用饱和的碳酸氢钠溶液;
(3)实验中没有装置C,使装置B与装置D直接相连,则CO2中混有的水汽会与碳反应生成还原性的H2,影响CO还原性的判断;
(4)因存在气体制备,整套实验装置需密封,故实验前,需对整套装置进行气密性检验;
(5)利用E装置中的黑色氧化铜变为红色,可知道氧化铜被还原为铜,推测CO具有还原性,发生反应的化学方程式为CO+CuO![]() Cu+CO2;
Cu+CO2;
(6)和二氧化碳的反应中,二氧化碳不可能完全转化为一氧化碳,所以从D装置出来的气体中含有二氧化碳,为防止原来二氧化碳的干扰,应先把D出来的二氧化碳除去,再将一氧化碳气体通过E装置,二氧化碳是酸性氧化物,所以用碱性物质除去,所以选②。


 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案科目:高中化学 来源: 题型:
【题目】一种由CuO和KHC2O4溶液反应的到的蓝色结晶[KaCub(C2O4)cdH2O]。为测定其组成,进行了如下实验:
步骤1称取3.5400 g该晶体,加入过量稀硫酸,待样品完全溶解后加入适量水,配制成100 mL溶液A.
步骤2量取20.00 mLA溶液,滴加0.2000 mol L-1 KMnO4溶液至恰好完全反应时,消耗KMnO4溶液8.00 mL。
步骤3另取20.00 mLA溶液,加入足量NaOH溶液,充分反应后,经过滤、洗涤、灼烧、称重,得到黑色固体粉末0.16 g。
己知:步骤2 中发生反应:2MnO4- + 5H2C2O4 + 6H+ = 2Mn2+ +10CO2↑ + 8H2O。
(1)步骤1中配制溶液A时,需要用到的玻璃仪器有烧杯、玻璃棒、_____。
(2)3.5400 g 该样品中含 n(C2O42-)= ____mol。
(3)3.5400 g 该样品中含 n(Cu2+)= ____mol。
(4)通过计算确定该蓝色晶体的化学式__________(计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有三种金属单质A、B、C,其中A的焰色反应为黄色,B、C是常见金属。三种金属单质A、B、C与气体甲、乙、丙及物质D、E、F、G、H之间发生如下转化关系(图中有些反应的产物和反应的条件没有标出)。
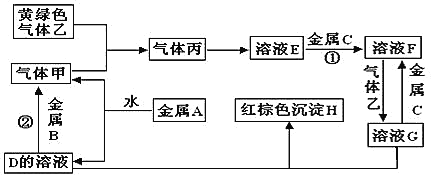
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:A__________; G___________。
(2) 写出反应①的化学方程式:__________;写出反应②的离子方程式:_________。
(3)说出黄绿色气体乙的一种用途__________________。
(4)区别E、F两种溶液最简单的方法是______,实验室检验G中所含的金属离子时,常在G的溶液中加入_____溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的数值,下列说法正确的是( )
A. 将含1molFeCl3的溶液滴入沸水中,所制得的Fe(OH)3胶体粒子为NA
B. 常温常压下,1 mol甲基(-CH3)所含电子数为10NA
C. 常温常压下,92g的NO2和N2O4混合气体含有的原子数为6NA
D. 标准状况下,11.2L三氯甲烷中含有的极性共价键数目为1.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无机化合物可根据其组成和性质进行分类
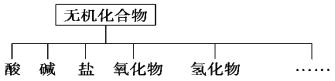
(1)图中所示的物质分类方法的名称是________。
(2)以Na、K、H、O、S、N中任两种或三种元素组成合适的物质,分别填在下表中②③⑥后面。
物质类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
化学式 | ①HCl ②____ | ③________ ④Ba(OH)2 | ⑤Na2CO3 ⑥______ | ⑦CO2 ⑧Na2O | ⑨NH3 ⑩H2O2 |
(3)写出⑦转化为⑤的化学方程式:___________。
(4)实验室制备⑦常用______和______反应,检验该气体的方法是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】JohnB.Goodenough等三位科学家因为在锂离子电池研究领域的突出贡献获得2019年诺贝尔化学奖。碳酸锂是一种常见的锂离子电池原料,一种以锂辉石为原料制取碳酸锂的工艺如图:(锂辉石:LiAl(SiO3)2,也表示为Li2O·Al2O3·4SiO2,还含微量的钠、钙、镁等元素)
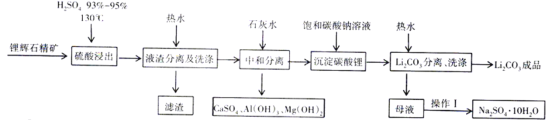
[查阅资料]:Li2CO3为无色单斜晶系结晶体,熔点618℃,溶于硫酸,微溶于水,在冷水中的溶解度比热水中大。
(1)在“硫酸浸出”流程,将硫酸加热到130℃的目的是___________________________。
(2)工业上高温煅烧FePO4、Li2CO3和草酸晶体(H2C2O4·2H2O)的混合物制取电池材料磷酸亚铁锂(LiFePO4),反应的化学方程式为__________________________________。
(3)LiFePO4含有Fe、Li两种金属元素,它们的焰色反应的颜色分别是___________
A.黄色、紫红色B.绿色、黄色C.无焰色反应、紫红色D.黄色、无焰色反应
(4)在“Li2CO3分离、洗涤”流程,用热水洗涤的原因是___________________________。
(5)某浓差电池的原理示意如图所示,可用该电池从浓缩海水中提取LiCl溶液。
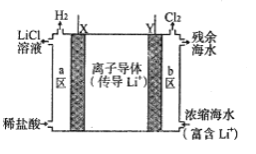
电池中的Y电极为________(填“正极”或“负极”或“阳极”或“阴极”)。X极的电极反应方程式为:________________________________________________。Y极每生成标况下22.4LCl2,有_________molLi+经过离子导体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯元素是最重要的“成盐元素”,广泛存在于自然界的多种矿物中。
(1)氯的原子结构示意图为______ 。根据氯的原子结构示意图可得出氯的哪些性质 (写出一条)_______ 。
(2)氢气能在氯气中燃烧,观察到的现象为___________ 。
(3)氯气是有毒气体,贮氯罐发生泄漏时可向贮氯罐周围的空气中喷洒稀NaOH溶液。氯气与NaOH反应的化学方程式为____________ 。
(4)水玻璃(硅酸钠的水溶液)中滴入稀盐酸,可生产硅酸胶体,反应的离子方程式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在20 L的密闭容器中按物质的量之比为1∶2充入CO和H2,发生反应:CO(g)+2H2(g)![]() CH3OH(g) ΔH。测得CO的转化率随温度及不同压强下的变化如图所示,p2和195 ℃时n(H2)随时间的变化结果如表所示。下列说法正确的是( )
CH3OH(g) ΔH。测得CO的转化率随温度及不同压强下的变化如图所示,p2和195 ℃时n(H2)随时间的变化结果如表所示。下列说法正确的是( )
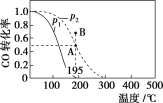
p2及195 ℃ 时n(H2)随时间变化
t/min | 0 | 1 | 3 | 5 |
n(H2)/mol | 8 | 5 | 4 | 4 |
A. p1>p2,ΔH<0
B. 在p2及195 ℃ 时,反应前3 min的平均速率v(CH3OH)=0.8 mol·L-1·min-1
C. 在p2及195 ℃ 时,该反应的平衡常数为25
D. 在B 点时,v正>v逆
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸亚铁晶体(FeC2O4·2H2O)是一种黄色难溶于水的固体,受热易分解,是生产电池、涂料以及感光材料的原材料。为探究纯净草酸亚铁晶体热分解的产物,设计装置图如下:
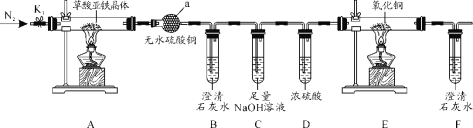
(1)仪器a的名称是______。
(2)从绿色化学考虑,该套装置存在的明显缺陷是_________。
(3)实验前先通入一段时间N2,其目的为__________。
(4)实验证明了气体产物中含有CO,依据的实验现象为_______。
(5)草酸亚铁晶体在空气易被氧化,检验草酸亚铁晶体是否氧化变质的实验操作是____。
(6)称取5.40g草酸亚铁晶体用热重法对其进行热分解,得到剩余固体质量随温度变化的曲线如下图所示:

①上图中M点对应物质的化学式为_________。
②已知400℃时,剩余固体是铁的一种氧化物,试通过计算写出M→N发生反应的化学方程式:_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com