
【题目】一种由CuO和KHC2O4溶液反应的到的蓝色结晶[KaCub(C2O4)cdH2O]。为测定其组成,进行了如下实验:
步骤1称取3.5400 g该晶体,加入过量稀硫酸,待样品完全溶解后加入适量水,配制成100 mL溶液A.
步骤2量取20.00 mLA溶液,滴加0.2000 mol L-1 KMnO4溶液至恰好完全反应时,消耗KMnO4溶液8.00 mL。
步骤3另取20.00 mLA溶液,加入足量NaOH溶液,充分反应后,经过滤、洗涤、灼烧、称重,得到黑色固体粉末0.16 g。
己知:步骤2 中发生反应:2MnO4- + 5H2C2O4 + 6H+ = 2Mn2+ +10CO2↑ + 8H2O。
(1)步骤1中配制溶液A时,需要用到的玻璃仪器有烧杯、玻璃棒、_____。
(2)3.5400 g 该样品中含 n(C2O42-)= ____mol。
(3)3.5400 g 该样品中含 n(Cu2+)= ____mol。
(4)通过计算确定该蓝色晶体的化学式__________(计算过程)。
【答案】100 mL容量瓶、胶头滴管 0.02 0.01 3.5400 g 该样品中含 n(Cu2+)为0.01mol,含n(C2O42-)为0.02mol,由电荷守恒可知含n(K+) =2n(C2O42-)- 2n(Cu2+)=0.02mol,则含n(H2O) =![]() =0.02mol,则A中n(K+):n(Cu2+):n(C2O42-):n(H2O) =2:1:2:2,故化学式为K2Cu(C2O4)2·2H2O
=0.02mol,则A中n(K+):n(Cu2+):n(C2O42-):n(H2O) =2:1:2:2,故化学式为K2Cu(C2O4)2·2H2O
【解析】
(1)配制成100 mL溶液A的操作步骤为溶解、转移、洗涤、定容、装瓶,实验中用到的玻璃仪器有烧杯、玻璃棒、100 mL容量瓶、胶头滴管,故答案为:100 mL容量瓶(胶头滴管);
(2)由题给方程式可得关系式2MnO4-~5C2O42-,20.00 mLA溶液消耗高锰酸钾的物质的量为0.2×8×10-3mol,则3.5400 g 该样品中含 n(C2O42-)=0.2×8×10-3mol×5×![]() =0.02mol,故答案为:0.02;
=0.02mol,故答案为:0.02;
(3)由铜原子个数守恒可得关系式Cu2+~CuO,20.00 mLA溶液得到CuO的物质的量为![]() =0.002mol,3.5400 g 该样品中含 n(Cu2+)=0.002mol×5=0.01mol,答案为:0.01;
=0.002mol,3.5400 g 该样品中含 n(Cu2+)=0.002mol×5=0.01mol,答案为:0.01;
(4)3.5400 g 该样品中含 n(Cu2+)为0.01mol,含n(C2O42-)为0.02mol,由电荷守恒可知含n(K+) =2n(C2O42-)- 2n(Cu2+)=0.02mol,则含n(H2O) =![]() =0.02mol,则A中n(K+):n(Cu2+):n(C2O42-):n(H2O) =2:1:2:2,故化学式为K2Cu(C2O4)2·2H2O。
=0.02mol,则A中n(K+):n(Cu2+):n(C2O42-):n(H2O) =2:1:2:2,故化学式为K2Cu(C2O4)2·2H2O。


 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:高中化学 来源: 题型:
【题目】下列图像分别表示有关反应的反应过程与能量变化的关系。据此判断下列说法正确的是
A. 石墨转变为金刚石的反应是吸热反应
B. 白磷比红磷稳定
C. S(g)=S(s) ΔH>0
D. H2(g)+I2(g)![]() 2HI(g) ΔH>0
2HI(g) ΔH>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法正确的是
A.标准状况下,22.4LNO和22.4LO2混合后的分子总数为2NA
B.0.1molL-1的氨水中,溶液中各微粒的物质的量存在以下关系:n(![]() )+n(NH3)+n(NHH2O)=0.1mol
)+n(NH3)+n(NHH2O)=0.1mol
C.已知氢气的热值为143kJg-1,则氢气充分燃烧的热化学方程式可表示为:H2(g)+![]() O2(g)=H2O(l) ΔH=-286kJmol1
O2(g)=H2O(l) ΔH=-286kJmol1
D.用酸性高锰酸钾溶液检验火柴头燃烧产生的SO2气体,当10mL0.1molL-1的酸性高锰酸钾溶液刚好褪色时,转移的电子总数为0.0025NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.化合物甲和化合物乙的混合粉末是汽车安全气囊中存放的化学物质,经组成分析,确定该混合粉末仅含 Na、Fe、N、O 四种元素。为研究安全气囊工作的化学原理,进行以下实验操作:
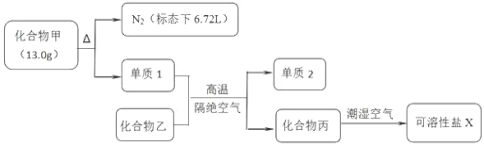
请回答下列问题:
(1)工业上冶炼单质2的化学方程式为 ________;
(2)若化合物丙在空气中转化为碳酸氢盐,则反应的化学方程式为 ________;
(3)化合物甲可用下列方法制备:30℃时,将水合肼(N2H4H2O)、亚硝酸甲酯(CH3ONO)、NaOH 混合,充分反应后先回收得到 CH3OH,母液降温结晶,过滤得到化合物甲。写出用该法制备化合物甲的化学反应方程式 ________。
II.晶体硅是一种重要的非金属材料。实验室用 SiHCl3 与过量 H2 反应制备纯硅的装置如下(热源及夹持装置略)。制备纯硅的主要反应为:SiHCl3+H2 = Si(纯)+3HCl
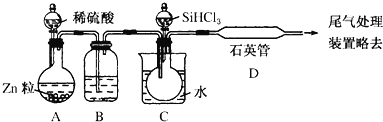
已知①SiHCl3 沸点 33.0℃,上述反应在 1000~1100℃进行;②SiHCl3 能与 H2O 强烈反应,在空气中易自燃。
请回答下列问题:
(1)下列说法不正确的是___________;
A.装置B中的溶液可以是浓硫酸
B.装置C中的烧瓶需要加热,其目的是使滴入烧瓶中的 SiHCl3 气化
C.装置D中观察到的现象是有固体物质生成
D.装置D可以采用普通玻璃管代替石英管
E.为保证制备纯硅实验的成功,关键的操作步骤有检查实验装置的气密性,控制好反应温度以及排尽装置中的空气、干燥气体
F.尾气处理装置中可以将导管直接插入盛有NaOH 溶液的烧杯中
(2)为检验某粗硅中存在的铁元素,可采取的实验操作方法是__________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某科研小组采用电解锰粉(主要成分为Mn和少量含Fe、Ni、Pb、P、Si等元素的单质或其化合物)为原料制备高纯氯化锰。
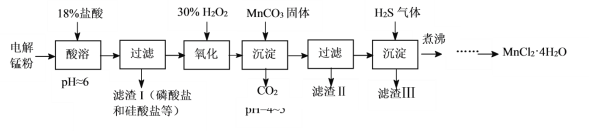
已知:①Mn是一种比Fe活泼的金属。
②H2S气体具有较强的还原性,如:H2S+H2O2=S↓+2H2O。
③相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mol·L-1计算)
Fe3+ | Fe2+ | Mn2+ | Ni2+ | Pb2+ | |
开始沉淀的pH | 1.1 | 5.8 | 8.6 | 6.7 | 8.0 |
沉淀完全的pH | 3.2 | 8.8 | 10.1 | 9.2 | 8.8 |
(1)酸溶时盐酸要缓慢滴加的原因是___。
(2)加入MnCO3固体时发生反应的离子方程式为___。MnCO3固体也可用下列物质代替___。(填写编号)
A.MnO B.MnSO4 C.Mn(OH)2 D.MnCl2
(3)通入H2S气体可使Pb2+、Ni2+生成硫化物沉淀,如:H2S(aq)+Pb2+(aq)![]() PbS(s)+2H+(aq),该反应的平衡常数K=___[用Ka1(H2S)、Ka2(H2S)及Ksp(PbS)表示]。
PbS(s)+2H+(aq),该反应的平衡常数K=___[用Ka1(H2S)、Ka2(H2S)及Ksp(PbS)表示]。
(4)煮沸的目的是___。
(5)已知MnCl2·4H2O在106℃时失去一分子结晶水,198℃失去全部结晶水。请补充完整由煮沸后的滤液获得高纯(>99.99%)MnCl2·4H2O晶体(MnCl2的溶解度曲线如图所示)的实验方案:将煮沸后的滤液冷却至室温,___(实验中须使用的试剂是:30%H2O2)。
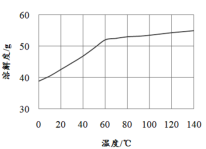
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的性质与用途具有对应关系的是( )
A.NaClO溶液具有碱性,可用于杀菌消毒
B.NH3具有还原性,可用于检验HCl泄漏
C.FeCl3溶液能与Cu反应,可用于蚀刻印刷电路板
D.漂白粉在空气中不稳定,可用于漂白纸浆
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应A2+B2===2AB的能量变化如图所示,则下列说法正确的是( )
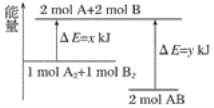
A. 该反应是吸收能量的反应
B. 1molA—A键和1molB—B键断裂能放出xkJ的能量
C. 2molA—B键断裂需要吸收ykJ的能量
D. 2molAB的总能量高于1molA2和1molB2的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室要配制100mL1.0mol·L-1的NaCl溶液,试回答下列各题。
(1)经计算,应该用托盘天平称取NaCl固体_________g。
(2)若用NaCl固体配制溶液,下列仪器中,不需要用到的是_________(填序号)。
A.锥形瓶,B.200mL容量瓶,C.烧杯,D.胶头滴管,E.药匙,F.托盘天平,G.洗瓶
(3)若要实施配制,除上述仪器外,尚缺的仪器或用品是_________、_________;
(4)在使用前必须检查容量瓶是否______。
(5)配制过程有以下操作:A.移液 B.称量 C.洗涤 D.定容 E.溶解 F.摇匀。其正确的操作顺序应是_________ (填序号)。
(6)下列四项错误操作会导致所得溶液浓度偏高的是______(填序号)。
A.定容时仰视容量瓶刻度线
B.定容时俯视容量瓶刻度线
C.将溶解冷却的溶液转入容量瓶后就直接转入定容操作
D.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,便补充几滴水至刻度处
(7)若实验过程中出现如下情况如何处理?加蒸馏水时不慎超过了刻度:______;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校学生课外活动小组的同学设计如图所示实验装置,用来验证一氧化碳具有还原性,回答下列问题:(提示:C+CO2![]() 2CO C+H2O(g)
2CO C+H2O(g)![]() CO+H2)
CO+H2)

(1)写出装置A中所发生反应的离子方程式:____________。
(2)装置B中最适宜的试剂是________________。
(3)若实验中没有装置C,使装置B与装置D直接相连,会对实验造成的影响是________。
(4)按照如图装置进行实验时,首先进行的操作是__________。
(5)根据实验中的___________现象,可证明CO具有还原性,有关反应的化学方程式是:__________。
(6)若要根据装置F中澄清石灰水变浑浊的现象确认一氧化碳具有还原性,应在图中装置_____与________之间连接图中的________装置(填序号)。
①![]() NaHCO3溶液 ②
NaHCO3溶液 ② 碱石灰 ③
碱石灰 ③![]() NaOH溶液 ④
NaOH溶液 ④![]() 浓H2SO4
浓H2SO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com