
【题目】已知25℃时,几种难溶电解质的溶度积常数Ksp如下表所示(当某种离子浓度≤10-5mol·L-1时,认为完全沉淀):
![]()

下列说法正确的是( )
A.相同温度下,溶度积常数越大相应物质的溶解度就越大
B.欲用1LNaCl溶液将0.01molAgBr转化为AgCl沉淀,则c(NaCl)≥3.61mol/L
C.在饱和Ag2CrO4溶液中加入K2CrO4能使溶液由图中Y点变为X点
D.AgCl悬浊液中存在平衡:AgCl(s)![]() Ag+(aq)+Cl-(aq),往其中加入少量NaCl固体,平衡向左移动,溶液中离子的总浓度会减小
Ag+(aq)+Cl-(aq),往其中加入少量NaCl固体,平衡向左移动,溶液中离子的总浓度会减小
【答案】B
【解析】
A. 相同类型的难溶物,其溶度积越大,溶解度就越大,不同类型的难溶物不具有可比性,故A错误;
B. 当AgBr完全转化为AgCl时,溶液中c(Br-)=0.01 molL1,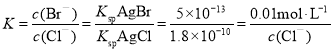 ,得到c(Cl-)=3.6 molL1,加上沉淀所需要的0.01 molL1,共3.61 molL1,因此c(NaCl)≥3.61 molL1,故B正确;
,得到c(Cl-)=3.6 molL1,加上沉淀所需要的0.01 molL1,共3.61 molL1,因此c(NaCl)≥3.61 molL1,故B正确;
C. 加入K2CrO4能使溶液平衡向生成Ag2CrO4的方向移动,CrO42-离子浓度增大,Ag+减小,所以不会变为X点,应从Y点向Z点移动,故C错误;
D. AgCl悬浊液中存在平衡:AgCl(s) ![]() Ag+(aq)+Cl-(aq),加入NaCl固体,平衡向左移动,因为引入了Na+,溶液中离子的总浓度会增大,故D错误。
Ag+(aq)+Cl-(aq),加入NaCl固体,平衡向左移动,因为引入了Na+,溶液中离子的总浓度会增大,故D错误。
综上所述,答案为B。


 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案科目:高中化学 来源: 题型:
【题目】化学常用的酸碱指示剂酚酞的结构简式如图所示,下列关于酚酞的说法错误的是( )
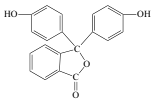
A.酚酞的分子式为C20H14O4
B.酚酞具有弱酸性,且属于芳香族化合物
C.1mol酚酞最多与2molNaOH发生反应
D.酚酞在碱性条件下能够发生水解反应,呈现红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲胺(CH3NH2)的性质与氨气相似。已知pKb=-lgKb,pKb(CH3NH2·H2O)=3.4,pKb(NH3·H2O)=4.8。常温下,向10.00 mL 0. 1000 mol·L-1的甲胺溶液中滴加0. 0500 mol·L-1的稀硫酸,溶液中c(OH-)的负对数pOH=-lgc(OH-)]与所加稀硫酸溶液的体积(V)的关系如图所示。下列说法错误的是
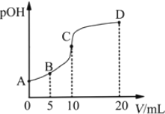
A.B点对应的溶液的pOH>3.4
B.甲胺溶于水后存在平衡:CH3NH2+H2O![]() CH3NH
CH3NH![]() +OH-
+OH-
C.A、B、C三点对应的溶液中,水电离出来的c(H+):C>B>A
D.A、B、C、D四点对应的溶液中,c(CH3NH3+)的大小顺序:D>C>B>A
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物。某工厂以孔雀石为主要原料制备CuSO4·5H2O,主要步骤如下:
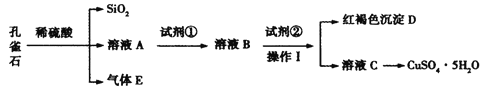
已知该条件下,通过调节溶液的酸碱性而使 Fe3+、Fe2+、Cu2+生成沉淀的 pH 分别如下:
物质 | 开始沉淀时的pH | 完全沉淀时的pH |
Fe(OH)3 | 2.2 | 3.2 |
Fe(OH)2 | 7.6 | 9.6 |
Cu(OH)2 | 4.7 | 6.4 |
请回答下列问题:
(1)为了提高孔雀石酸浸时的速率,除适当增加浓硫酸浓度外,还可以采取的措施有:___(写一种)。
(2)试剂①是双氧水,把 Fe2+氧化成 Fe3+的目的是___。根据如图有关数据,你认为工业上氧化操作时应采取的条件是___。
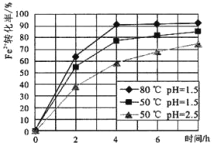
(3)试剂②为CuO,其目的是调节溶液的 pH 保持在___范围。操作Ⅰ的名称是___。
(4)溶液 C 得到CuSO4·5H2O的主要步骤是___、___、过滤、洗涤、干燥。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成有机玻璃单体的一种方法如下,下列有关说法正确的是( )
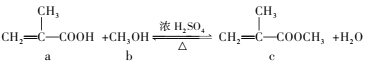
A.a、b、c均易溶于水和有机溶剂
B.与a具有相同官能团的同分异构体还有1种
C.a、c分子中碳原子一定在同一平面上
D.a、c均能发生加成、氧化、取代和还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钨在自然界主要以钨(+6价)酸盐的形式存在。黑钨矿的主要成分是铁和锰的钨酸盐,化学式常写成FeWO4、MnWO4。黑钨矿冶炼金属钨的流程如下图(已知:钨酸是一种难溶性强酸、对热不稳定)。其中A、B、C都是钨的化合物。完成下列填空:

(1)上述从黑钨矿获得单质钨的过程中属于氧化还原反应的是(填数字序号)__________。
(2)操作①的名称为__________,得到的滤液为钨酸的钠盐,写出反应②的化学方程式______________。该过程中产品C为_________,从产品C获得纯度较高的钨的另一反应原料应该为___________。
(3)若制得的钨中含有少量金属铁,为测定其中金属钨的含量(已知金属钨不溶于盐酸),甲同学用下列装置进行测定:
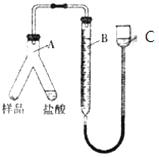
相关实验步骤:
①加好称量好的样品和盐酸,记录B的液面位置;
②检查气密性。
③待A中不再有气体产生并恢复至室温后,记录B的液面位置;
④将A中盐酸与样品混合;
正确的操作顺序是_________________(填序号)
(4)若实验用样品的质量为a g,加入20mL盐酸与之充分反应后,测得排出水的体积为VL(标准状况下),测得的H2的体积应为___________L,样品中的钨的质量分数的计算式为______________。
(5)在读取C装置液面数据时,应先____________,再平视读数,若样品中含有不溶于酸,也不与酸反应的物质,则测得钨的质量分数将_________(填“偏大”、“偏小”或“不受影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25 ℃时,Ka(HF)=3.6×10-4,Ksp(CaF2)=1.46×10-10,现向1 L 0.2 mol·L-1HF溶液中加入1 L 0.2 mol·L-1 CaCl2溶液,则下列说法中,正确的是
A. 25 ℃时,0.1 mol·L-1 HF溶液中pH=1
B. Ksp(CaF2)随温度和浓度的变化而变化
C. 该体系中没有沉淀产生
D. 该体系中HF与CaCl2反应产生沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关金属及其化合物的不合理的是( )
A. 将废铁屑加入![]() 溶液中,可用于除去工业废气中的
溶液中,可用于除去工业废气中的![]()
B. 铝中添加适量钾,制得低密度、高强度的铝合金,可用于航空工业
C. 盐碱地(含较多![]() 等)不利于作物生长,可施加熟石灰进行改良
等)不利于作物生长,可施加熟石灰进行改良
D. 无水![]() 呈蓝色,吸水会变为粉红色,可用于判断变色硅胶是否吸水
呈蓝色,吸水会变为粉红色,可用于判断变色硅胶是否吸水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组设计如图所示装置,用CuCl2·2H2O晶体和SOCl2获取无水CuCl2并回收过量的SOCl2。
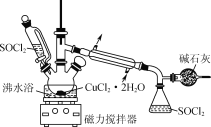
已知:SOCl2的熔点为-105℃,沸点为76℃,遇水剧烈反应生成两种酸性气体。
回答下列问题:
(1)CuCl2·2H2O晶体和SOCl2发生反应的化学方程式是___。
(2)碱石灰除了能吸收SO2、HCl等酸性气体,还能起到的作用为__。
(3)某同学用“间接碘量法”测定无水CuCl2样品中铜元素的百分含量,操作步骤如下:
步骤1:取0.2500g试样溶于水,加入过量KI固体充分反应,生成白色CuI沉淀。
步骤2:滴入几滴淀粉溶液。
步骤3:再滴入0.1000mol·L-1Na2S2O3溶液,发生的反应为2S2O32-+I2=S4O62-+2I-,恰好完全反应时,消耗Na2S2O3溶液18.00mL。
①恰好完全反应时的实验现象为__。
②计算试样中铜元素的质量分数__(写出计算过程)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com