
【题目】下列说法中正确的是
A.摩尔是用于计量微观粒子集体的物理量
B.CO2的摩尔质量为44g
C.0.5mol水中约含6.02×1023个H
D.标准状况下1 mol任何物质体积均为22.4L
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质。为了提纯氯化钾,先将样品溶于适量水中,充分搅拌后过滤,在将滤液按下图所示步骤进行操作。
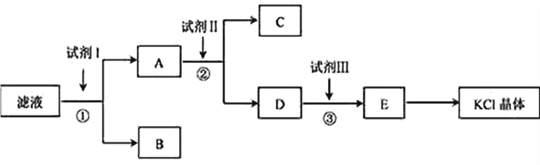
回答下列问题:
(1)起始滤液的pH_______7(填“大于”、“小于”或“等于”),其原因是______________。
(2)试剂I的化学式为________,①中发生反应的离子方程式为_________________________。
(3)试剂Ⅱ的化学式为___________,②中加入试剂Ⅱ的目的是__________________________;
(4)试剂Ⅲ的名称是___________,③中发生反应的离子方程式为________________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从海水中提取溴,主要反应为:2Br-+Cl2=Br2+2Cl-,下列说法正确的是
A.溴离子具有氧化性B.氯气是还原剂
C.该反应属于复分解反应D.氯气的氧化性比溴单质强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在高温高压下CO具有极高的化学活性,能与多种单质或化合物反应.
(1)若在恒温恒容的容器内进行反应C(s)+H2O(g)CO(g)+H2(g),则可用来判断该反应达到平衡状态的标志有 . (填字母)
a.容器内的压强保持不变
b.容器中H2浓度与CO浓度相等
c.容器中混合气体的密度保持不变
d.CO的生成速率与H2的生成速率相等
(2)CO一空气燃料电池中使用的电解质是搀杂了Y2O3的ZrO2晶体,它在高温下能传导O2 . 该电池负极的电极反应式为 .
(3)一定条件下,CO与H2可合成甲烷,反应方程式为:CO(g)+3H2(g)CH4(g)+H2O(g)
①一定条件下,该反应能够自发进行的原因是 .
②已知H2(g)、CO(g)和 CH4(g)的燃烧热分别为285.8kJmol﹣1、283.0kJmol﹣1和890,0kJmol﹣1 .
写出CO与H2反应生成CH4和CO2的热化学方程式:
(4)工业上可通过甲醇羰基化法制取甲酸甲酯,反应方程式为:CH3OH(g)+CO(g) ![]() HCOOCH3(g)△H=﹣29.1kJmol﹣1 . 科研人员对该反应进行了研究.部分研究结果如图所示:
HCOOCH3(g)△H=﹣29.1kJmol﹣1 . 科研人员对该反应进行了研究.部分研究结果如图所示: 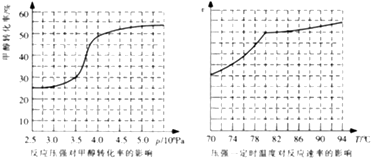
①从反应压强对甲醇转化率的影响“效率“看,工业制取甲酸甲酯应选择的压强是 .
②实际工业生产中采用的温度是80℃,其理由是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某铁柱需长期浸入水下,为了减少腐蚀,下列措施中不能达到目的是
A.在铁柱上铆上一些锌片B.将铁柱与直流电源的正极相连
C.在铁柱表面涂上一层较厚的沥青D.在铁柱表面镀锡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于纯净物、混合物、强电解质、弱电解质的正确组合是
纯净物 | 混合物 | 强电解质 | 弱电解质 | 非电解质 | |
A | 纯盐酸 | 水煤气 | 硫酸 | 醋酸 | 干冰 |
B | 冰醋酸 | 福尔马林 | 硫酸钡 | 亚硫酸 | 三氧化硫 |
C | 油酯 | 淀粉 | 苛性钾 | 氢硫酸 | 碳酸钙 |
D | 重水 | 纤维素 | 氯化钠 | 次氯酸 | 氯气 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA代表阿伏加德罗常数的值,下列说法正确的是( )
A.0.1mol的OH﹣中含有的电子数为0.9NA
B.标准状况下,11.2 L CCl4所含分子数为0.5NA
C.6.02×1022个 CH4所含氢原子数为0.4NA
D.常温常压下,28 g N2中所含原子个数为NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com