
【题目】已知:p[c(HX)/c(X-)]=-lg[c(HX)/c(X-)]。室温下,向0. 10 mol/LHX溶液中滴加0.10 mol/L NaOH溶液,溶液pH随p[c(HX)/c(X-)]变化关系如图。下列说法不正确的是
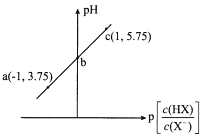
A. 溶液中水的电离程度:a<b<cB. 图中b点坐标为(0,4.75)
C. c点溶液中:c(Na+) =l0c(HX)D. 室温下HX的电离常数为10-4. 75
【答案】C
【解析】
电离平衡常数只受温度的影响,因此用a或c点进行判断,用a点进行分析,c(HX)/c(X-)=10-1,c(H+)=10-3.75mol·L-1,HX的电离平衡常数的表达式Ka=c(X-)×c(H+)/c(HX),代入数值,Ka=10-4.75,由于a、b、c均为酸性溶液,因此溶质均为“HX和NaX”,不可能是NaX或NaX和NaOH,pH<7说明HX的电离程度大于X-的水解程度,即只考虑HX电离产生H+对水的抑制作用,然后进行分析;
电离平衡常数只受温度的影响,因此用a或c点进行判断,假设用a点进行分析,c(HX)/c(X-)=10-1,c(H+)=10-3.75mol·L-1,HX的电离平衡常数的表达式Ka=c(X-)×c(H+)/c(HX),代入数值,Ka=10-4.75,由于a、b、c均为酸性溶液,因此溶质均为“HX和NaX”;
A、根据上述分析,pH<7说明HX的电离程度大于X-的水解程度,HX电离出H+对水电离起到抑制作用,H+浓度越小,pH越大,对水的电离抑制能力越弱,即溶液中水的电离程度:a<b<c,故A说法正确;
B、根据上述分析,HX的电离平衡常数Ka=10-4.75,b点时,c(HX)/c(X-)=1,则c(H+)=10-4.75mol·L-1,b点坐标是(0,4.75),故B说法正确;
C、c点溶液中c(Na+)+c(H+)=c(OH-)+c(X-),根据c点坐标,c(HX)/c(X-)=10,代入电荷守恒得到c(Na+)+c(H+)=c(OH-)+10c(HX),因为溶液显酸性,c(H+)>c(OH-),推出c(Na+)<10c(HX),故C说法错误;
D、根据上述分析,故D说法正确。


科目:高中化学 来源: 题型:
【题目】曲美替尼是一种抑制黑色素瘤的新型抗癌药物,下面是合成曲美替尼中间体G的反应路线:

已知:①D分子中有2个6元环;

请回答:
(1)化合物A的结构简式___________。A生成B的反应类型___________。
(2)下列说法不正确的是___________。
A.B既能表现碱性又能表现酸性
B.1moC在碱溶液中完全水解最多可以消耗4 molOH-
C.D与POCl3的反应还会生成E的一种同分异构体
D.G的分子式为C16H18O3N4
(3)写出C→D的化学方程式____________________________________________。
(4)X是比A多2个碳原子的A的同系物,写出符合下列条件的X可能的结构简式:_______________________________________________________。
①1H-NMR谱显示分子中有3种氢原子,②IR谱显示分子中有苯环与-NH2相连结构
(5)流程中使用的DMF即N,N-二甲基甲酰胺结构简式为 ,是常用的有机溶剂。设计以甲醇和氨为主要原料制取DMF的合成路线(用流程图表示,其他无机试剂任选)。_____________
,是常用的有机溶剂。设计以甲醇和氨为主要原料制取DMF的合成路线(用流程图表示,其他无机试剂任选)。_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图(1)和图(2)是A、B两种物质的核磁共振氢谱。已知A、B两种物质都是烃类,都含有6个氢原子。请根据图(1)和图(2)两种物质的核磁共振氢谱图选择出可能属于图(1)和图(2)的两种物质( )

A. A是C3H6;B是C6H6
B. A是C2H6;B是C3H6
C. A是C2H6;B是C6H6
D. A是C3H6;B是C2H6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下0.1mol/L的CH3COOH溶液加水稀释过程中,下列数值一定变小的是
A. c(H+) B. c (H+) /c(CH3COOH)
C. c (H+)·c(OH-) D. c(OH-)/c (H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T℃,分别向10 mL浓度均为1![]() 的两种弱酸HA,HB中不断加水稀释,并用pH传感器测定溶液
的两种弱酸HA,HB中不断加水稀释,并用pH传感器测定溶液![]() 。所得溶液pH的两倍(2pH)与溶液浓度的对数(lgc)的关系如图所示。已知:pKa=-lgKa,下列叙述正确的是( )
。所得溶液pH的两倍(2pH)与溶液浓度的对数(lgc)的关系如图所示。已知:pKa=-lgKa,下列叙述正确的是( )

A.弱酸的Ka随溶液浓度的降低而增大
B.a点对应的溶液中c(HA)=0.1mol/L,pH=4
C.弱酸![]() 的pK≈5
的pK≈5
D.酸性: HA<HB
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下将NaOH溶液滴入二元弱酸H2X溶液中,混合溶液中的离子浓度与溶液pH的变化关系如图所示。下列叙述正确的是( )
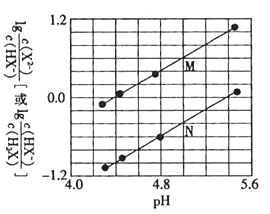
A.Ka1(H2X)的数量级为![]()
B.曲线N表示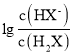 与pH的变化关系
与pH的变化关系
C.NaHX溶液中:c(H+)<c(OH-)
D.当混合物呈中性时,c(Na+)>c(X2-)>c(HX-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列是八种环状的烃类物质:
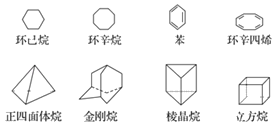
(1)互为同分异构体的有___和___、___和___(填写名称)。
(2)正四面体烷的二氯取代产物有___种;金刚烷的一氯取代产物有___种。
(3)化合物A的相对分子质量为86,所含碳的质量分数为55.8%,氢的质量分数为7.0%,其余为氧。
①A的分子式为___。
②A有多种同分异构体,写出五个同时满足下列条件的同分异构体的结构简式:
a.能发生水解反应b。能使溴的四氯化碳溶液褪色
___、___、___、___、___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,c(CH3COOH)+c(CH3COO-)=0.1mol·L-1的醋酸、醋酸钠混合溶液中,c(CH3COOH)、c(CH3COO-)与pH的关系如图所示。下列有关该溶液的叙述不正确的是( )
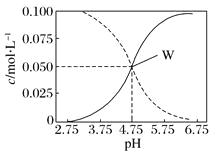
A. pH=5的溶液中:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-)
B. 溶液中:c(H+)+c(Na+)=c(CH3COO-)+c(OH-)
C. 由W点可以求出25℃时CH3COOH的电离常数
D. pH=4的溶液中:c(H+)+c(Na+)+c(CH3COOH)-c(OH-)=0.1mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列是科研小组设计的一个氮氧化物原电池,两边的阴影部分为a,b惰性电极,分别用导线与烧杯的m,n(惰性电极)相连接,工作原理示意图如图:
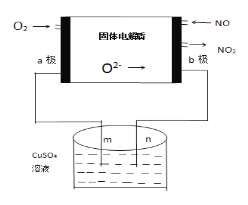
①a为___极,b极的电极反应式____________。
②在标准状况下,通入112mL的O2,可观察到烧杯中n处有_____生成,(假设烧杯中的溶液的体积为200mL,体积不变)最后反应终止时烧杯中溶液的pH为______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com