
【题目】(1)室温下,0.1 mol/L的下列溶液中,①NH4Al(SO4)2 ②NH4HSO4 ③HCl ④(NH4)2SO4 ⑤NH4Cl ⑥NH4HCO3 ,pH由大到小的顺序为__________(填写序号)
(2)加热,逐渐蒸干FeSO4溶液,得到的物质为___________。(填化学式)
(3)如图是0.1 mol/L电解质溶液的pH随温度变化的图象。

①其中符合0.1 mol/L NH4Al(SO4)2溶液的pH随温度变化的曲线是_____(填写罗马数字)
②25 ℃时,0.1 mol/L的NH4Al(SO4)2溶液中2c(![]() )-c(
)-c(![]() )-3c(Al3+)=____(填数值)。
)-3c(Al3+)=____(填数值)。
(4)室温时,向100 mL 0.1 mol/L的NH4HSO4溶液中滴加0.1 mol/L NaOH溶液,所得溶液的pH与所加NaOH溶液体积的关系曲线如图所示:

试分析图中a、b、c、d四个点,水的电离程度最大的是____;在b点,溶液中各离子浓度由大到小的排列顺序是______________。
【答案】 ⑥⑤④①③② Fe2(SO4)3和Fe(OH)3 Ⅰ 10-3 mol/L a点 c(Na+)>c(![]() )>c(
)>c(![]() )>c(OH-)=c(H+)
)>c(OH-)=c(H+)
【解析】(1)室温下,0.1 mol/L的下列溶液中,②NH4HSO4的电离方程式为:NH4HSO4=NH4++ H++ SO42-,且铵根离子水解,故c(H+)>0.1mol/L,pH<1;③HCl为强酸,完全电离,c(H+)=0.1mol/L,pH=1;铝离子水解程度大于铵根离子,故①NH4Al(SO4)2水解程度大于④(NH4)2SO4 ,pH:①<④;⑤NH4Cl、⑥NH4HCO3铵根离子是④(NH4)2SO4的一半,水解产生的氢离子浓度较小,而HCO3-也水解,结合氢离子,氢离子浓度减小,pH最大的是⑥NH4HCO3,pH由大到小的顺序为:⑥⑤④①③②;(2)蒸干FeSO4溶液,Fe2+易被氧化生成Fe3+,而Fe3+水解生成Fe(OH)3,且等物质的量的Fe(OH)3与硫酸不能完全中和,故蒸干FeSO4溶液得到Fe2(SO4)3和Fe(OH)3;(3)①NH4Al(SO4)2水解,溶液呈酸性,升高温度其水解程度增大,pH减小,符合的曲线为Ⅰ;②根据电荷守恒,可以求出25 ℃时,0.1 mol/L的NH4Al(SO4)2溶液中2c(SO42-)-c(NH4+)-3c(Al3+)= c(H+)- c(OH-)=10-3mol/L-10-11mol/L![]() 10-3mol/L;(4)a、b、c、d四个点,根据反应量的关系,a点恰好消耗完H+,溶液中只有(NH4)2SO4与Na2SO4;b、c、d三点溶液均含有NH3H2O,(NH4)2SO4可以促进水的电离,而NH3H2O抑制水的电离.b点溶液呈中性,即溶液含有(NH4)2SO4、Na2SO4、NH3H2O三种成分,a点时c(Na+)=c(SO42-),b点时c(Na+)>c(SO42-),根据N元素与S元素的关系,可以得出c(SO42-)>c(NH4+),故c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+)。
10-3mol/L;(4)a、b、c、d四个点,根据反应量的关系,a点恰好消耗完H+,溶液中只有(NH4)2SO4与Na2SO4;b、c、d三点溶液均含有NH3H2O,(NH4)2SO4可以促进水的电离,而NH3H2O抑制水的电离.b点溶液呈中性,即溶液含有(NH4)2SO4、Na2SO4、NH3H2O三种成分,a点时c(Na+)=c(SO42-),b点时c(Na+)>c(SO42-),根据N元素与S元素的关系,可以得出c(SO42-)>c(NH4+),故c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+)。


 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案科目:高中化学 来源: 题型:
【题目】可逆反应达到化学平衡状态的重要特征是 ( )
A. 反应停止了 B. 正、逆反应的速率都为0
C. 正、逆反应都还在进行 D. 正、逆反应的速率相等且不为0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解9.6 g。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如下图所示(已知硝酸只被还原为NO气体),下列分析或结果错误的是

A. 原混合酸中HNO3的物质的量为0.1 mol
B. OA段产生的是NO,AB段的反应为Fe+2Fe3+ == 3Fe2+,BC段产生氢气
C. 第二份溶液中最终溶质为FeSO4
D. H2SO4浓度为2.5 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列烷烃的沸点:甲烷:﹣162℃;乙烷:﹣89℃;丁烷:﹣1℃;戊烷:36℃.根据以上数据推断丙烷的沸点可能是( )
A.约﹣40℃
B.低于﹣162℃
C.低于﹣89℃
D.高于36℃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如右图所示a、b、c、d分别是几种常见漏斗的上部,A、B、C、D是实际操作中各漏斗的下部插入容器中的示意图,请指出A、B、C、D分别与a、b、c、d相匹配的组合及其组合后装置在实验中的应用,例如:C和a组合,用于制取气体.①A与组合,用于 , ②B与组合,用于 ,
③B与组合,用于 , ④D与组合,用于 . 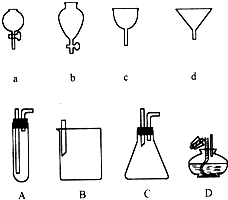
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于NO的叙述正确的是 ( )
A. NO易溶于水,所以可用排空气法收集
B. NO是一种有刺激性气味的红棕色气体
C. 常温常压下,含等质量氧元素的NO和CO的体积相等
D. NO不能通过化合反应获得
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在室温下,向Cu(IO3)2饱和溶液中加入足量的经稀硫酸酸化的KI溶液,产生碘化亚铜(CuI)沉淀,溶液由蓝色变为棕黄色,反应前加入淀粉溶液不变蓝,反应后加入淀粉溶液变为蓝色.
(1)该反应中氧化剂是;
(2)该反应的氧化产物是;
(3)1mol氧化剂在反应中得到电子的物质的量为;
(4)某反应体系中有物质:Bi2(SO4)3、NaMnO4、H2O、MnSO4、NaBiO3、Na2SO4、H2SO4 . 请将NaBiO3之外的反应物与生成物分别填入以下空格内,配平化学计量数,并用单线桥表示电子转移的方向和数目. ![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com