
【题目】如右图所示a、b、c、d分别是几种常见漏斗的上部,A、B、C、D是实际操作中各漏斗的下部插入容器中的示意图,请指出A、B、C、D分别与a、b、c、d相匹配的组合及其组合后装置在实验中的应用,例如:C和a组合,用于制取气体.①A与组合,用于 , ②B与组合,用于 ,
③B与组合,用于 , ④D与组合,用于 . 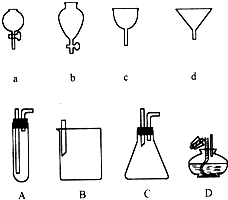
科目:高中化学 来源: 题型:
【题目】某温度下,在甲、乙、丙、丁四个恒容密闭容器中投入H2和I2,发生反应:H2 (g) +I2 (g)![]() 2HI(g) 。反应体系中各物质浓度的有关数据如下。
2HI(g) 。反应体系中各物质浓度的有关数据如下。
容器 | 起始浓度 | 平衡浓度 | |
c(H2)/mol·L-1 | c(I2)/mol·L-1 | c(HI)/mol·L-1 | |
甲 | 0.01 | 0.01 | 0.004 |
乙 | 0.01 | 0.02 | a |
丙 | 0.02 | 0.01 | b |
丁 | 0.02 | 0.02 | —— |
下列判断正确的是
A. 平衡时,H2的转化率:丁>甲
B. 平衡时,乙中H2的转化率等于20%
C. HI的平衡浓度:a=b>0.004
D. 丙中条件下,该反应的平衡常数K = 4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某100mL溶液可能含有Na+、NH4+、Fe3+、CO32-、SO42-、Cl-中的若干种,取该溶液进行连续实验,实验过程如下(所加试剂均过量,气体全部逸出)下列说法不正确的是:
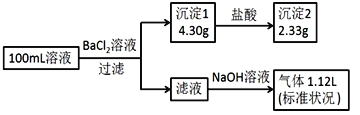
A. 原溶液一定存在CO32-、SO42-、NH4+
B. 原溶液一定存在Cl-,一定不存在Fe3+
C. 可能存在Na+,可以通过焰色反应证明其是否存在
D. 若原溶液中不存在Na+,则c(Cl-)<0.1mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国“长征二号F”运载火箭发射现场.可以看到从火箭的下部喷射出大量的红棕色的气体,关于这种红棕色气体的认识正确的是
A.是溴蒸气,火箭发射时作氧化剂
B.是二氧化氮气体,火箭发射时作还原剂
C.是溴蒸气,火箭发射时作还原剂
D.是二氧化氮气体,火箭发射时作氧化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)室温下,0.1 mol/L的下列溶液中,①NH4Al(SO4)2 ②NH4HSO4 ③HCl ④(NH4)2SO4 ⑤NH4Cl ⑥NH4HCO3 ,pH由大到小的顺序为__________(填写序号)
(2)加热,逐渐蒸干FeSO4溶液,得到的物质为___________。(填化学式)
(3)如图是0.1 mol/L电解质溶液的pH随温度变化的图象。

①其中符合0.1 mol/L NH4Al(SO4)2溶液的pH随温度变化的曲线是_____(填写罗马数字)
②25 ℃时,0.1 mol/L的NH4Al(SO4)2溶液中2c(![]() )-c(
)-c(![]() )-3c(Al3+)=____(填数值)。
)-3c(Al3+)=____(填数值)。
(4)室温时,向100 mL 0.1 mol/L的NH4HSO4溶液中滴加0.1 mol/L NaOH溶液,所得溶液的pH与所加NaOH溶液体积的关系曲线如图所示:

试分析图中a、b、c、d四个点,水的电离程度最大的是____;在b点,溶液中各离子浓度由大到小的排列顺序是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用右图表示的一些物质或概念间的从属关系中不正确的是( )
X | Y | Z | |
A | 氧化物 | 化合物 | 纯净物 |
B | 胶体 | 分散系 | 混合物 |
C | 含氧酸 | 一元酸 | 酸 |
D | 碱性氧化物 | 金属氧化物 | 氧化物 |

A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】液氨气化后,分解产生的氢气可作为氢氧燃料电池的燃料。氨气分解反应的热化学方程式如下:2NH3(g) ![]() N2 (g) + 3H2(g) ΔH = + a kJ·mol-1 (a>0)。请回答下列问题:
N2 (g) + 3H2(g) ΔH = + a kJ·mol-1 (a>0)。请回答下列问题:
已知:2H2 (g) + O2 (g) =2H2O(l) ΔH1 = - b kJ·mol-1
NH3 (g) ![]() NH3(l) ΔH2 = - c kJ·mol-1
NH3(l) ΔH2 = - c kJ·mol-1
(1)氨气自发分解的反应条件为________(填“高温”、“ 低温”、“ 任何条件下”),4NH3(l) + 3O2 (g) = 2N2 (g) + 6H2O(l) 的 ΔH3 =_____________kJ·mol-1。
(2)H2O的电子式为_____________,水能发生电离:2H2O(l) ![]() H3O++OH-,液氨也能发生类似的电离。请写出液氨的电离方程式____________________________________。
H3O++OH-,液氨也能发生类似的电离。请写出液氨的电离方程式____________________________________。
(3)液氨气化后,分解产生的氢气可作为氢氧燃料电池的燃料,在KOH电解质溶液中,电池负极的电极反应为__________________________________________,实验室中用氢氧燃料电池作为电源采用Pt电极对液氨进行电解可以得到H2和N2 ,若电解过程中阳极收集得到4.48L气体(标况),则转移的电子的数目是_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com