
【题目】2013年12月17日,中国国土资源部召开新闻发布会,宣布在广东沿海珠江口盆地东部海域首次钻获高纯度可燃冰。可燃冰的主要成分是甲烷,甲烷既是清洁的燃料,也是重要的化工原料。
(1)甲烷和二氧化碳重整制合成气,对于温室气体的治理具有重大意义。
已知:CH4(g)+CO2(g)![]() 2CO(g)+2H2(g)ΔH=+247.3 kJ·mol-1
2CO(g)+2H2(g)ΔH=+247.3 kJ·mol-1
CH4(g)![]() C(s)+ 2H2(g) ΔH=+75 kJ·mol-1
C(s)+ 2H2(g) ΔH=+75 kJ·mol-1
①反应2CO(g)![]() C(s)+CO2(g)在一定条件下能自发进行的原因是 。
C(s)+CO2(g)在一定条件下能自发进行的原因是 。
②合成甲醇的主要反应是:2H2(g)+CO(g)![]() CH3OH(g)ΔH=-90.8 kJ·mol-1,T ℃下此反应的平衡常数为160。某时刻测得各组分的浓度如下:
CH3OH(g)ΔH=-90.8 kJ·mol-1,T ℃下此反应的平衡常数为160。某时刻测得各组分的浓度如下:
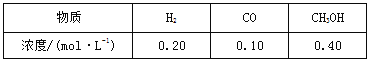
比较此时正、逆反应速率的大小:v(正) v(逆)(填“>”、“<”或“=”)。生产过程中,合成气要进行循环,其目的是 。
③在一恒容密闭容器中,要提高反应2H2(g)+CO(g)![]() CH3OH(g)中CO的转化率,可以采取的措施是 。
CH3OH(g)中CO的转化率,可以采取的措施是 。
a.升温
b.加入催化剂
c.增加CO的浓度
d.加入H2
e.加入惰性气体
f.分离出甲醇
(2)以甲烷为燃料的新型电池,其成本大大低于以氢为燃料的传统燃料电池,如图是目前研究较多的一类固体氧化物燃料电池工作原理示意图。
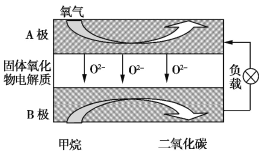
①B极为电池 极,电极反应式为 。
②若用该燃料电池作电源,用石墨作电极电解100 mL 1 mol/L的硫酸铜溶液,当两极收集到的气体体积相等时,理论上消耗甲烷的体积为 (标况下)。
【答案】(1)①ΔH<0
②> 提高原料的利用率 ③df
(2)①负 CH4 + 4O2--8e- ![]() CO2+ 2H2O
CO2+ 2H2O
② 1.12 L
【解析】本题主要考查化学反应原理,意在考查考生在理解所学各部分化学知识的本质区别与内在联系的基础上,运用所掌握的知识进行必要的分析、类推或计算,解释、论证一些具体化学问题的能力。(1)①用已知的第二个反应减去第一个反应得:2CO(g)![]() C(s)+CO2(g)ΔH=+75 kJ·mol-1-247.3 kJ·mol-1 =-172.3 kJ·mol-1。该反应的ΔH<0,是放热反应,而熵ΔS<0,所以在一定条件下能自发进行。②该时刻下=100<K=160,所以平衡正向移动,v(正)>v(逆)。因为反应是可逆反应,为了提高原料的利用率,合成气要进行循环。③升高温度,平衡向逆反应方向移动,CO的转化率减小;使用催化剂,平衡不移动,CO的转化率不变;增加CO的浓度,CO的转化率减小;加入惰性气体,平衡不移动,CO的转化率不变。
C(s)+CO2(g)ΔH=+75 kJ·mol-1-247.3 kJ·mol-1 =-172.3 kJ·mol-1。该反应的ΔH<0,是放热反应,而熵ΔS<0,所以在一定条件下能自发进行。②该时刻下=100<K=160,所以平衡正向移动,v(正)>v(逆)。因为反应是可逆反应,为了提高原料的利用率,合成气要进行循环。③升高温度,平衡向逆反应方向移动,CO的转化率减小;使用催化剂,平衡不移动,CO的转化率不变;增加CO的浓度,CO的转化率减小;加入惰性气体,平衡不移动,CO的转化率不变。
(2)①B极通入的气体是甲烷,甲烷发生氧化反应,故B极是电池的负极。电池总反应为CH4+2O2![]() CO2+2H2O,因为电解质是固体氧化物,所以正极O2发生还原反应生成O2-,电极反应式为O2+4e-
CO2+2H2O,因为电解质是固体氧化物,所以正极O2发生还原反应生成O2-,电极反应式为O2+4e-![]() 2O2-,用总方程式减去正极反应式即得负极反应式。②电解CuSO4溶液时,阴极生成Cu,阳极生成O2。当Cu2+被电解完之后,水电离产生的H+即被还原为H2。0.1 mol Cu2+被还原时,阳极生成0.05 mol O2;此后再电解0.1 mol H2O时,生成0.1 mol H2和0.05 mol O2,两极收集到的气体体积相等。电路中一共转移0.4 mol电子,需要CH4的物质的量为0.4 mol/8 =0.05 mol,V(CH4)= 1.12 L。
2O2-,用总方程式减去正极反应式即得负极反应式。②电解CuSO4溶液时,阴极生成Cu,阳极生成O2。当Cu2+被电解完之后,水电离产生的H+即被还原为H2。0.1 mol Cu2+被还原时,阳极生成0.05 mol O2;此后再电解0.1 mol H2O时,生成0.1 mol H2和0.05 mol O2,两极收集到的气体体积相等。电路中一共转移0.4 mol电子,需要CH4的物质的量为0.4 mol/8 =0.05 mol,V(CH4)= 1.12 L。


 同步奥数系列答案
同步奥数系列答案科目:高中化学 来源: 题型:
【题目】【选修2 :化学与技术】
某工厂的镀铜废水中含有CN-和Cr2O72一离子,需要处理达标后才能排放。该厂拟用下列流程进行废水处理,回答下列问题:
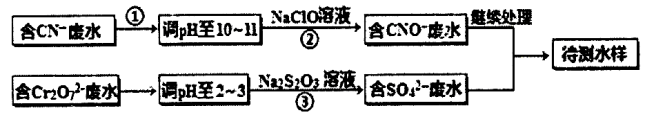
(1)流程中可用pH 试纸测定溶液的pH,pH试纸的使用方法是_______;
(2)步骤②中反应无气体放出,该反应的离子方程式为____;
(3)步骤③中,每处理1.0molCr2O7—时转移电子数为6NA,该反应的离子方程式为_____;
(4)取少量待测水样于试管中,加入NaOH 溶液,观察到有蓝色沉淀生成,再加Na2S溶液,蓝色沉淀转化成黑色沉淀,产生该现象对应的离子方程式为_________。
(5)含氰化物的废水必须经检测达标后(排放标准为CN—的含量<0.5mg/L)才能排放。现取该法处理 后的废水100.0mL,用“试银灵”为指示剂、1.0×10-4mol/L的AgNO3标准溶液滴定,终点时溶液由黄色变为橙红色,消耗标准液的体积为5.00mL,反应的离子方程式为Ag + 2CN—=[Ag(CN)2]一,该水样中CN-的含量为________mg/L(不考虑Cr等元素的干扰)。该厂处理后的废水能否合法排放________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g),该反应的能量变化如图所示:
CH3OH(g)+H2O(g),该反应的能量变化如图所示:
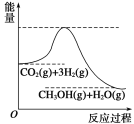
(1)你认为该反应为____________(填放热或吸热)反应.
(2)恒容容器中,对于以上反应,能加快反应速率的是 。
a.升高温度 b.充入He c.加入催化剂 d.降低压强
(3)在体积为2 L的密闭容器中,充入1 mol CO2和3 mol H2,测得CO2的物质的量随时间变化如下表所示。
t/min | 0 | 2 | 5 | 10 | 15 |
n(CO2)/mol | 1 | 0.75 | 0.5 | 0.25 | 0.25 |
从反应开始到5min末,用H2浓度变化表示的平均反应速率v(H2)= ;反应达到平衡状态,此时H2的转化率为 。
(4)在相同温度、容积不变的条件下,能说明该反应已达平衡状态的是 (填序号)。
a.CO2、H2、CH3OH、H2O的浓度均不再变化
b.v生成(CH3OH)=v消耗(CO2)
c.n(CO2)∶n(H2)∶n(CH3OH)∶n(H2O)=1∶1∶1∶1
d.容器中混合气体的密度保持不变
e. H2的消耗速率与CH3OH的消耗速率之比为3∶1
f.体系压强不变
(5)以CH3OH、空气、氢氧化钾溶液为原料,石墨为电极可构成然料电池,该电池中负极上的电极反应式是:_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子序数由小到大排列的四种短周期元素X、Y、Z、W,其中X、Z、W与氢元素可组成XH3、H2Z和HW共价化合物;Y与氧元素可组成Y2O和Y2O2的离子化合物。
(1)写出Y2O2的电子式:____ _,其中含有的化学键是___ _。
(2)用电子式表示Y2O的形成过程________ _______。
(3)X、Z、W三种元素的最高价氧化物对应的水化物中,稀溶浓氧化性最强的是_____(填化学式)。
(4)XH3、H2Z和HW三种化合物,其中一种与另外两种都能反应的是__________(填化学式)。
(5)由X、Y组成的化合物分子中.X、W原子的最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物,试写出反应的化学方程式_______________ ____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是
A.用硫氰化钾溶液检验Fe3+:Fe3++3SCN﹣![]() Fe(SCN)3↓
Fe(SCN)3↓
B.向海带灰浸出液中加入稀硫酸、双氧水:2I﹣+2H++H2O2![]() I2+2H2O
I2+2H2O
C.磨口玻璃试剂瓶被烧碱溶液腐蚀:SiO2+2Na++2OH﹣![]() Na2SiO3↓+H2O
Na2SiO3↓+H2O
D.NaHCO3溶液和少量Ba(OH)2溶液混合:+OH﹣+Ba2+![]() H2O+BaCO3↓
H2O+BaCO3↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组以H2O2分解为例,探究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照表中所示方案完成实验。
实验编号 | 反应物 | 催化剂 |
① | 10 mL 2% H2O2溶液 | 无 |
② | 10 mL 5% H2O2溶液 | 无 |
③ | 10 mL 5% H2O2溶液 | 1 mL 0.1 mol·L-1 FeCl3溶液 |
④ | 10 mL 5% H2O2溶液+少量HCl溶液 | 1 mL 0.1 mol·L-1 FeCl3溶液 |
⑤ | 10 mL 5% H2O2溶液+少量NaOH溶液 | 1 mL 0.1 mol·L-1 FeCl3溶液 |
(1)催化剂能加快化学反应速率的原因是 。
(2)常温下5% H2O2溶液的pH约为6,H2O2的电离方程式为 。
(3)实验①和②的目的是 。
实验时由于没有观察到明显现象而无法得出结论。资料显示,通常条件下H2O2 稳定,不易分解。为了达到实验目的,你对原实验方案的改进是 。
(4)实验③④⑤中,测得生成氧气的体积随时间变化的关系如图所示。

分析图像能够得出的实验结论是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电-Fenton法是用于水体里有机污染物降解的高级氧化技术。其反应原理如图所示,其中电解产生的H2O2与Fe2+发生Fenton反应:Fe2++H2O2![]() Fe3++OH- +·OH,生成的羟基自由基(·OH)能氧化降解有机污染物。下列说法不正确的是
Fe3++OH- +·OH,生成的羟基自由基(·OH)能氧化降解有机污染物。下列说法不正确的是
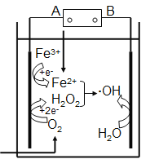
A.电源的A极是负极
B.电解池中只有O2、Fe3+发生还原反应
C.阳极上发生电极反应:H2O-e-![]() ·OH + H+
·OH + H+
D.消耗1molO2,可以产生4mol ·OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验式相同,但既不是同系物,又不是同分异构体的是 ( )
A.1-戊烯和2-甲基丙烯
B.甲醛和甲酸甲酯
C.1-丁醇与甲醚
D.丙酸和甲酸乙酯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH3经一系列反应可以得到HNO3和NH4NO3,如下图所示。
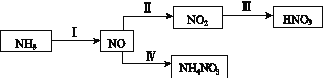
(1)Ⅰ中,NH3和O2在催化剂作用下反应,其化学方程式是______________。
(2)Ⅱ中,2NO(g)+O2(g)![]() 2NO2(g)。在其他条件相
2NO2(g)。在其他条件相
同时,分别测得NO的平衡转化率在不同压强(p1、p2)下随温度变化的曲线(如图)。
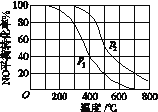
①比较p1、p2的大小关系:p1________p2(填“<”,“>”或“=”)
②随温度升高,该反应平衡常数变化的趋势是________(填“增大”,“减小”或“不变”)。
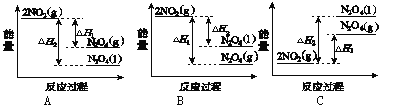
(3)Ⅲ中,降低温度,将NO2(g)转化为N2O4(l),再制备浓硝酸。
①已知:2NO2(g)![]() N2O4(g) ΔH12NO2(g)
N2O4(g) ΔH12NO2(g)![]() N2O4(l) ΔH2
N2O4(l) ΔH2
下列能量变化示意图中,正确的是(选填字母)________。
②N2O4与O2、H2O化合的化学方程式是____________________。
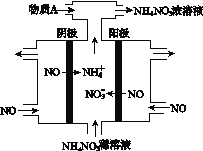
(4)Ⅳ中,电解NO制备NH4NO3,其工作原理如图所示。为使电解产物全部转化为NH4NO3,需补充A。A是______,说明理由:__________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com