
【题目】700℃时,向容积为2 L的密闭容器中充入一定量的CO和H2O,发生反应:CO(g)+H2O(g)![]() CO2(g)+H2(g),反应过程中测定的部分数据见下表(表中t2>t1):
CO2(g)+H2(g),反应过程中测定的部分数据见下表(表中t2>t1):
反应时间/min | n(CO)/mol | n(H2O)/mol |
0 | 1.20 | 0.60 |
t1 | 0.80 | |
t2 | 0.20 |
下列说法正确的是
A. 反应在t1 min内的平均速率为v(H2)=![]() mol·L-1·min-1
mol·L-1·min-1
B. 保持其他条件不变,起始时向容器中充入0.60 mol CO和1.20 mol H2O,达到平衡时n(CO2)=0.40mol
C. 保持其他条件不变,向平衡体系中再通入0.20 mol H2O,与原平衡相比,达到新平衡时CO转化率不变,H2O的体积分数不变
D. 温度升高至800 ℃,上述反应平衡常数为0.64,则正反应为放热反应
【答案】BD
【解析】
A.根据v=![]() ,计算v(CO),结合化学反应速率之比等于化学计量数之比计算v(H2);
,计算v(CO),结合化学反应速率之比等于化学计量数之比计算v(H2);
B.CO与H2O按物质的量比1:1反应,充入0.60 mol CO和1.20 mol H2O与充入1.20 mol CO和0.6mol H2O到达平衡时对应生成物的浓度、物质的量相同;
C.保持其他条件不变,增加一种反应物的浓度,平衡向正反应方向移动,另一种反应物的转化率增大;
D.根据平衡时各物质的浓度计算700℃时的平衡常数,比较不同温度下的平衡常数大小可判断反应的吸放热。
A.v(H2)=v(CO)=![]() =
=![]() mol·L-1·min-1,故A错误;
mol·L-1·min-1,故A错误;
B.CO与H2O按物质的量比1:1反应,充入0.60 mol CO和1.20 mol H2O与充入1.20 mol CO和0.6mol H2O,平衡时生成物的浓度对应相同,t1min时n(CO)=0.8mol,n(H2O)=0.6mol-0.4mol=0.2mol,t2min时n(H2O)=0.2mol,说明t1min时反应已经达到平衡状态,根据化学方程式可知,则生成的n(CO2)=0.4mol,故B正确;
C.保持其他条件不变,向平衡体系中再通入0.20molH2O,与原平衡相比,平衡向右移动,达到新平衡时CO转化率增大,H2O转化率减小,H2O的体积分数会增大,故C错误;
D.t1min时反应已经达到平衡状态,此时c(CO)=0.4mol/L,c(H2O)=0.1mol/L,c(CO2)=c(H2)=0.2mol/L,则K=![]() =1,温度升至800℃,上述反应平衡常数为0.64,说明温度升高,平衡是向左移动的,那么正反应为放热反应,故D正确;
=1,温度升至800℃,上述反应平衡常数为0.64,说明温度升高,平衡是向左移动的,那么正反应为放热反应,故D正确;
答案选BD。


科目:高中化学 来源: 题型:
【题目】某化学兴趣小组同学拟用如下装置制备纯净干燥的CO2,并与Na2O2样品反应(杂质不反应),通过测定量气管中氧气体积,计算出样品纯度(即质量分数)。

(1)A中装稀盐酸的仪器的名称是______________,B中的试剂a最好选用___________,E装置的作用____________________________。
(2)D装置中的现象为________________________;恢复到原温度后,读取F装置量气管刻度前必要的操作是___________________________________________________________。
(3)若无C装置,你认为对实验结果有何影响___________。(填“偏大”、“偏小”或“无影响”)。
(4)若取2.0gNa2O2样品充分反应后,F中收集到224mL氧气(折算成标准状况,不考虑氧气在水中的溶解),则样品纯度为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有研究预测,到2030年,全球报废的电池将达到1100万吨以上。而目前废旧电池的回收率却很低。为了提高金属资源的利用率,减少环境污染,应该大力倡导回收处理废旧电池。下面是一种从废电池正极材料(含铝箔、LiCoO2、Fe2O3及少量不溶于酸碱的导电剂)中回收各种金属的工艺流程:
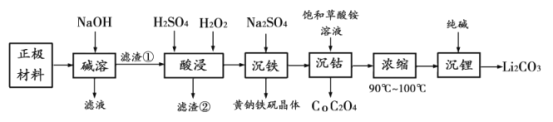
资料:1.黄钠铁矾晶体颗粒粗大,沉淀速度快,易于过滤。
2.钴酸锂难溶于水、碳酸锂的溶解度随温度升高而降低。
回答下列问题:
(1)为了提高碱溶效率可以__,__。(任答两种)
(2)从经济效益的角度考虑,为处理“碱溶”后所得滤液,可向其中通入过量CO2,请写出所发生反应的化学反应方程式__。
(3) “酸浸”时有无色气体产生,写出发生反应的离子方程式__。
(4) “沉铁”时采用的“黄钠铁矾法”与传统的通过调整溶液pH的“氢氧化物沉淀法”相比,金属离子的损失少,请分析并说明原因:___。
(5) “沉锂”后得到碳酸锂固体的实验操作为__。
(6)已知黄钠铁矾的化学式为NaxFey(SO4)m(OH)n。为测定黄钠铁矾的组成,进行了如下实验:①称取4.850g样品,加盐酸完全溶解后,配成100.00mL溶液;②量取25.00mL溶液,加入足量的KI,用0.2500molL-1Na2S2O3溶液进行滴定(反应2Fe3++2I-=2Fe2++I2,I2+2Na2S2O3=2NaI+Na2S4O6),消耗30.00mLNa2S2O3溶液至终点。③另取25.00mL溶液,加足量BaCl2溶液充分反应后,过滤、洗涤、干燥后得沉淀1.165g。
用Na2S2O3溶液进行滴定时,使用的指示剂为__;计算出黄钠铁矾的化学式__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列几种物质:
①MgCl2 ②H2O ③Al ④H2O2 ⑤Na2O2 ⑥Ca(OH)2 ⑦HClO ⑧I2
(1)只含有离子键的是(选填序号,下同)________。
(2)含有共价键的离子化合物是________。
(3)属于共价化合物的是________。
(4)熔融状态时和固态时,都能导电的是________。
(5)HClO的电子式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列反应的热化学方程式为
①CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH1=-870.3kJ·mol-1
②C(s)+O2(g)=CO2(g) ΔH2=-393.5kJ·mol-1
③H2(g)+![]() O2(g)=H2O(l) ΔH3=-285.8kJ·mol-1
O2(g)=H2O(l) ΔH3=-285.8kJ·mol-1
则反应2C(s)+2H2(g)+O2(g)=CH3COOH(l)的ΔH为( )
A.-488.3kJ·mol-1
B.-191kJ·mol-1
C.-476.8kJ·mol-1
D.-1549.6kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知B是酒的主要成分、C是食醋的主要成分。下图是相关有机物的转换关系:
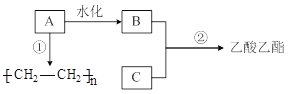
完成下列填空。
(1)A的结构简式为______,工业上生产A所需的矿物资源是______。
(2)请写出C的官能团名称___________。
(3)反应②的化学方程式为_____________。
(4)实验室用如图装置制取乙酸乙酯。实验时需预先在用于收集乙酸乙酯的试管b中加入_____溶液。实验结束后,发现试管b中的液体分两层,乙酸乙酯在____层(填“上”或“下”),分离乙酸乙酯的实验操作方法是_______。
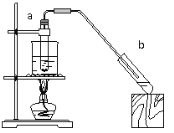
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的转化在给定条件下均能通过一步反应实现的是
A. NaAlO2(aq)![]() AlCl3
AlCl3![]() Al2O3
Al2O3
B. N2![]() NO2
NO2![]() HNO3
HNO3
C. NaCl(饱和)![]() NaHCO3
NaHCO3![]() Na2CO3
Na2CO3
D. FeS2![]() SO3
SO3![]() H2SO4
H2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能证明碳酸的酸性比硅酸强的事实是
A. 二氧化碳溶于水且能反应生成碳酸,二氧化硅不溶于水不能与水反应生成硅酸
B. 在高温下,二氧化硅与碳酸钠能发生反应:SiO2+Na2CO3![]() Na2SiO3+CO2↑
Na2SiO3+CO2↑
C. 二氧化硅的熔点比二氧化碳的熔点高
D. 二氧化碳通入硅酸钠溶液中,生成白色胶状沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中的反应,属于同一反应类型的是
A. 由溴丙烷水解制丙醇;由丙烯与水反应制丙醇
B. 由甲苯硝化制对硝基甲苯;由甲苯氧化制苯甲酸
C. 由氯代环己烷消去制环己烯;由丙烯加溴制![]() 二溴丙烷
二溴丙烷
D. 由乙酸和乙醇制乙酸乙酯;由苯甲酸乙酯水解制苯甲酸和乙醇
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com