
【题目】海洋中有丰富的食品、矿产、能源、药物和水产资源,下图为海水利用的部分过程,下列有关说法正确的是
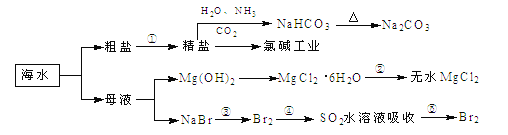
A. 制取NaHCO3的反应是利用其溶解度小于NaCl和NH4Cl
B. ①粗盐提纯中除去杂质离子Mg2+、Ca2+、SO42-时,必须先除Ca2+后除SO42-
C. 在工段③、④、⑤中,溴元素均被氧化
D. 工业上通过电解饱和MgCl2溶液制取金属镁
【答案】A
【解析】
A项,“侯氏制碱法”的基本原理是:在浓氨水中通入足量的二氧化碳,生成碳酸氢铵溶液,然后在此盐溶液中加入细的食盐粉末,碳酸氢钠由于在该状态下溶解度很小,呈晶体析出,析出的碳酸氢钠加热分解即可制得纯碱;B项,粗盐溶于水,加入氢氧化钠溶液除去镁离子,再加入氯化钡溶液,除去硫酸根离子,最后加碳酸钠溶液除去钙离子和钡离子;或者粗盐溶于水,先加氯化钡溶液,除去硫酸根离子,再加入氢氧化钠溶液除去镁离子,最后加碳酸钠溶液,除去钙离子和钡离子;C项,第④步骤,Br2+SO2+2H2O=2HBr+H2SO4,溴元素被还原;D项,工业上通过电解熔融状态的MgCl2制取金属镁。
A项,“侯氏制碱法”中发生NH3+CO2+NaCl+H2O=NH4Cl+ NaHCO3反应,是利用NaHCO3的溶解度比较小的规律,故A项正确;B项,粗盐溶于水,先加入氢氧化钠溶液、再加氯化钡溶液、最后加碳酸钠溶液,先后除去Mg2+、SO42- 、Ca2+;或先加氯化钡溶液、加入氢氧化钠溶液、最后加碳酸钠溶液,先后除去SO42-、Mg2+、Ca2+;所以没有先后之分,故B项错误;C项,第③、⑤步骤,溴元素被氧化,第④步骤,Br2+SO2+2H2O=2HBr+H2SO4,溴元素被还原,故C项错误;D项,电解饱和MgCl2溶液制得的是Cl2和H2,工业上通过电解熔融状态的MgCl2制取金属镁,故D项错误;正确选项A。


科目:高中化学 来源: 题型:
【题目】有8种物质:①甲烷 ②苯 ③聚乙烯 ④聚异戊二烯(![]() ) ⑤2-丁炔 ⑥环乙烷 ⑦邻二甲苯 ⑧2-甲基-1,3-丁二烯,既能使酸性高锰酸钾溶液褪色,又能与溴水反应使之褪色的是
) ⑤2-丁炔 ⑥环乙烷 ⑦邻二甲苯 ⑧2-甲基-1,3-丁二烯,既能使酸性高锰酸钾溶液褪色,又能与溴水反应使之褪色的是
A. ③④⑤⑧ B. ④⑤⑦⑧ C. ④⑤⑧ D. ③④⑤⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质分类的叙述错误的是
A. 饱和食盐水属于混合物B. 碳酸钠既属于钠盐又属于碳酸盐
C. 胆矾属于混合物D. 纯净物一般可分成单质和化合物两类
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来环境问题突出,大气污染更为严重。回答下面问题
(1)下列选项中属于重点城市空气质量日报首要污染物的是_____
A.CO2 B.SO2 C.可吸入颗粒物 D.H2S
(2)汽车尾气常含有CO、NO等有毒气体,汽车气缸中生成NO的化学方程式是___________
(3)汽车排气管装有的三元催化装置,可以消除CO、NO等的污染,反应机理如下(以Pt催化剂为例)
I:NO+Pt(S)=NO(S)(Pt(S)表示催化剂,NO(S)表示吸附态NO,下同)
II:CO+Pt(S)=CO(S)
III:NO(S)=N(S)+O(S)
IV:CO(S)+O(S)=CO2+2Pt(S)
V:N(S)+N(S)=N2+2Pt(S)
VI:NO(S)+N(S)=N2O+2Pt(S)
尾气中反应物及生成物浓度随温度的变化关系如下图。
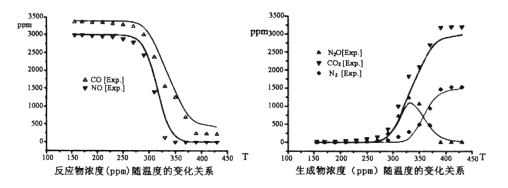
回答下面问题
①汽车尾气消污反应最适宜的反应温度是____
A. 250℃ B.300℃ C.330℃ D.400℃
②330℃以下的低温区发生的主要反应的化学方程式是___________
③低温区N2O选择性高于N2,由此可推断出:V反应的活化能____Ⅵ反应的活化能(填
“<”、“>”或“=”),理由是_______________
④结合反应机理和图像温度位于330℃—400℃时,升高温度,V反应的反应速率_____,(填“增大”、“减小”或“不变”,下同),Ⅳ反应的反应速率__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化氢(H2O2)在医药、化工、民用等方面有广泛的应用。回答下面问题:
(1)最早制备H2O2使用的原料是易溶于水的BaO2和稀硫酸,发生反应的化学方程式是____。
(2)目前工业制备H2O2的主要方法是蒽醌法。反应流程如下:
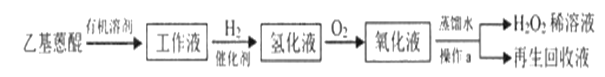
已知:乙基蒽醌是反应中的催化剂。
①蒽醌法所用原料的物质的量之比为____。
②操作a是____。
③再生回收液的成分是____。
(3)测量过氧化氢浓度常用的方法是滴定法,某次测定时,取20. 00mL过氧化氢样品,加入过量硫酸酸化,用0. l000mol/L的KMnO4标准溶液滴定至终点,消耗10. 00mL,滴定时发生反应的离子方程式为 ___,该样品中H2O2的物质的量浓度为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】.某同学利用下列实验探究金属铝与铜盐溶液反应:

下列说法正确的是
A. 由实验1可以得出结论:金属铝的活泼性弱于金属铜
B. 溶液中阴离子种类不同是导致实验1、2出现不同现象的原因
C. 实验2中生成红色物质的离子方程式:Al+Cu2+→Al3++Cu
D. 由上述实验可推知:用砂纸打磨后的铝片分别与c(H+)均为0.2 mol/L的盐酸和硫酸反应,后者更剧烈
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于卤化氢的说法中不正确的是( )
A. 卤素原子序数越大,其氢化物越稳定
B. 卤素原子序数越大,其氢化物越不稳定
C. 卤化氢稳定性的顺序为HF>HCl>HBr>HI
D. 卤素单质与氢气越难反应,生成的氢化物越不稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.SiO2溶于水且显酸性
B.SiO2是制造太阳能电池的常用材料
C.SiO2是酸性氧化物,它不与任何酸反应
D.水玻璃可用作木材防火剂,向其溶液中通入CO2气体,有白色凝胶状固体析出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】臭氧是理想的烟气脱硝剂,其脱硝反应为:2NO2(g)+O3(g)![]() N2O5(g)+O2(g),反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是( )
N2O5(g)+O2(g),反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是( )
A | B | C | D |
|
|
|
|
升高温度, | 0~3s内,反应速率为: | t1时仅加入催化剂, | 达平衡时,仅改变x,则x为c(O2) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com