
【题目】有机物M的结构结构简式如图所示。关于M,下列说法正确的是( )
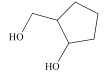
A.分子中所有碳原子可能共平面
B.M的同分异构体中,能与饱和NaHCO3溶液反应有9种
C.可使酸性高锰酸钾溶液褪色
D.1molM与足量的钠反应可以生成22.4LH2
【答案】C
【解析】
A.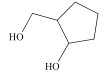 分子结构中的碳原子均为sp3杂化,则分子中所有碳原子不可能共平面,故A错误;
分子结构中的碳原子均为sp3杂化,则分子中所有碳原子不可能共平面,故A错误;
B.M的分子式为C6H12O2,同分异构体中,能与饱和NaHCO3溶液反应,说明含有-COOH,则相当于C5H12的烷烃中氢原子被-COOH取代,其中CH3CH2CH2CH2CH3有三种等效氢,CH(CH3)2CH2CH3有4种等效氢,C(CH3)3有1种等效氢,故满足条件的同分异构体共有8种,故B错误;
C.分子结构中的醇羟基能被酸性高锰酸钾溶液氧化,则M可使酸性高锰酸钾溶液褪色,故C正确;
D.1molM与足量的钠反应可以生成1molH2,标准状况下体积为22.4LH2,选项中未标明是否是标准状况,故D错误;
故答案为C。


科目:高中化学 来源: 题型:
【题目】二氧化硫是危害最为严重的大气污染物之一,它主要来自化石燃料的燃烧,研究CO催化还原SO2的适宜条件,在燃煤电厂的烟气脱硫中具有重要价值。
Ⅰ.从热力学角度研究反应
(1) C(s)+O2(g)![]() CO2(g) ΔH1=-393.5 kJ·mol-1
CO2(g) ΔH1=-393.5 kJ·mol-1
CO2(g)+C(s)![]() 2CO(g) ΔH2=+172.5 kJ·mol-1
2CO(g) ΔH2=+172.5 kJ·mol-1
S(s)+O2(g)![]() SO2(g) ΔH3=-296.0 kJ·mol-1
SO2(g) ΔH3=-296.0 kJ·mol-1
写出CO 还原SO2的热化学方程式:_________________。
(2)关于CO还原SO2的反应,下列说法正确的是______。
A.在恒温恒容条件下,若反应体系压强不变,则反应已达到平衡状态
B.平衡状态时,2v正(CO)=v逆(SO2)
C.其他条件不变,增大SO2的浓度,CO的平衡转化率增大
D.在恒温恒压的容器中,向达到平衡状态的体系中充入N2,SO2的平衡转化率不变
Ⅱ.NOx的排放主要来自于汽车尾气,包含NO2和NO,有人提出用活性炭对NOx进行吸附,发生反应如下:
反应a:C(s)+2NO(g)![]() N2(g)+CO2(g) ΔH=-34.0kJ/mol
N2(g)+CO2(g) ΔH=-34.0kJ/mol
反应b:2C(s)+2NO2(g)![]() N2(g)+2CO2(g) ΔH=-64.2kJ/mol
N2(g)+2CO2(g) ΔH=-64.2kJ/mol
(3)对于反应a,在T1℃时,借助传感器测得反应在不同时间点上各物质的浓度如下:
时间(min) 浓度(mol·L-1) | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.00 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
①0~10min内,NO的平均反应速率v(NO)=___________,当升高反应温度,该反应的平衡常数K___________(选填“增大”、“减小”或“不变”)。
②30min后,只改变某一条件,反应重新达到平衡;根据上表中的数据判断改变的条件可能是___________(填字母)。
A.加入一定量的活性炭 B.通入一定量的NO
C.适当缩小容器的体积 D.加入合适的催化剂
(4)①某实验室模拟反应b,在密闭容器中加入足量的C和一定量的NO2气体,维持温度为T2℃,如图为不同压强下反应b经过相同时间NO2的转化率随着压强变化的示意图。请从动力学角度分析,1050kPa前,反应b中NO2转化率随着压强增大而增大的原因_____________;在1100kPa时,NO2的体积分数为___________。
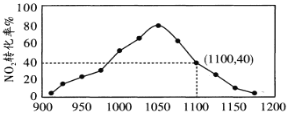
②用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数(记作Kp);在T2℃、1.1×106Pa时,该反应的化学平衡常数Kp=___________(计算表达式表示);已知:气体分压(P分)=气体总压(P总)×体积分数。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(实验1)探究草酸的制备:
实验室用硝酸氧化淀粉(C6H12O6)水解液法(水浴加热)制备草酸,其反应为:C6H12O6+12HNO3 = 3H2C2O4+9NO2↑+3NO↑+9H2O ,装置如图所示:
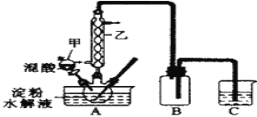
(1)仪器乙的名称为:_________,其接通冷水与水浴加热三颈瓶的先后顺序是:________
(2)烧杯C中盛放的溶液是___________,装置的B作用是______________
(实验2)探究草酸的不稳定性:
已知:草酸晶体(H2C2O4·2H2O)无色,易溶于水,熔点为101℃,受热易脱水、升华,170℃以上分解产生H2O、CO和CO2,其酸性比碳酸强,其钙盐难溶于水。
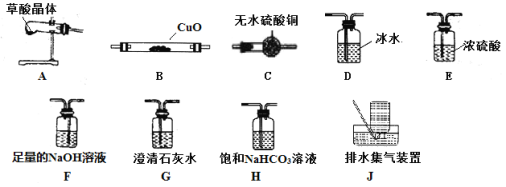
(3)请选取以上的装置证明草酸晶体分解的产物(可重复使用,加热装置和连接装置已略去)。仪器装置连接顺序为:A→_______→______→______→_______→E→B→G→_______。
(4)若实验结束后测得B管质量减轻4.8g,则至少需分解草酸晶体的质量为_________g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现对三种不同的镁铝合金样品进行编号,做以下实验探究。
(1)取样品①m1g,加入过量NaOH溶液,充分反应后过滤;往滤液中通入过量CO2气体:将所得沉淀过滤、洗涤、烘干,灼烧,得到固体的质量仍然为m1g.合金中镁的质量分数为_____(保留2位小数,下同)。
(2)取样品②m2g,与足量稀硫酸反应,固体完全溶解时得到气体的体积为VL(标准状况)。m2的取值范围是_____。
(3)取样品③0.918g与30.00mL、2.00mL盐酸充分反应后,得到672mL气体(标准状况)。剩余合金0.306g(认为合金中镁、铝与酸的反应同时发生)。然后在反应后所得体系中继续加1.00mol/L的NaOH溶液,恰好使所有铝元素均不以沉淀形式存在。则需要加入1.00mol/L的NaOH溶液_____mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系如图所示(图中有些反应的生成物和反应的条件没有标出)。
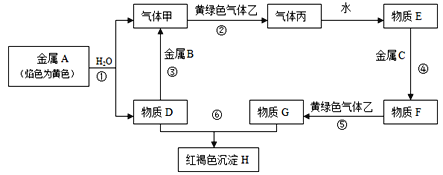
请回答下列问题:
(1)写出下列物质的化学式:B_____________, C_______________,F_____________, 乙_______________,
(2)写出下列反应的离子方程式:反应①____________________;反应⑤____________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】光电池在光照条件下可产生电流,如图装置可以实现光能源的充分利用,双极性膜可将水解离为H+和OH-,并实现其定向通过。下列说法不正确的是( )
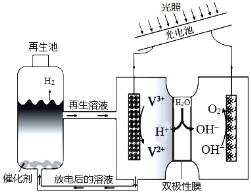
A.该装置可利用光能实现水的分解
B.光照过程中阴、阳极区溶液中的pH均基本不变
C.再生池中的反应为2V2++2H+![]() 2V3++H2↑
2V3++H2↑
D.每有1molOH-通过双极性膜,可产生5.6L(标准状况)的O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:2NO(g)+Br2(g)![]() 2NOBr(g) △H=-a kJ·mol-1 (a>0),其反应机理如下
2NOBr(g) △H=-a kJ·mol-1 (a>0),其反应机理如下
①NO(g)+Br2(g)![]() NOBr2(g) 快 ②NO(g)+NOBr2(g)
NOBr2(g) 快 ②NO(g)+NOBr2(g)![]() 2NOBr(g) 慢
2NOBr(g) 慢
下列有关该反应的说法正确的是( )
A. 该反应的速率主要取决于①的快慢
B. NOBr2是该反应的催化剂
C. 正反应的活化能比逆反应的活化能小a kJ·mol-1
D. 增大Br2(g)浓度能增大活化分子百分数, 加快反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烟气的脱硝(除![]() )技术和脱硫(除
)技术和脱硫(除![]() )技术都是目前环境科学研究的热点。
)技术都是目前环境科学研究的热点。
(1)工业上可以采用“质子膜电解槽”对烟气进行脱硫脱硝,其工艺如图甲所示:
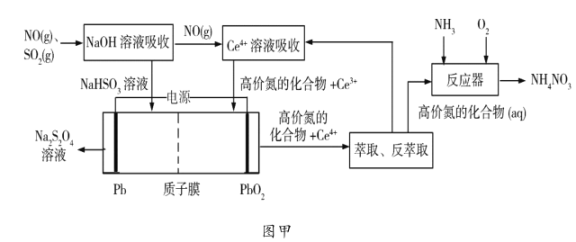
①![]() 溶液吸收
溶液吸收![]() 主要反应的化学方程式为___________;
主要反应的化学方程式为___________;
②电解的主要目的是______________,阴极的电极反应式为______________;
③“高价氮的化合物”中NO2在反应器中发生化合反应的化学方程式为______;
(2)利用活性焦炭的吸附作用,可以对烟气进行脱硫和脱硝。被吸附的![]() 与活性焦炭反应生成
与活性焦炭反应生成![]() 和
和![]() ,当生成
,当生成![]() 时,转移电子的物质的量为__________
时,转移电子的物质的量为__________![]() ;
;
(3)一定条件下,将一定浓度NOx(NO2和NO的混合气体)通入![]() 的
的![]() 乳浊液中,发生的反应如下:
乳浊液中,发生的反应如下:![]() ,
,![]() ,改变
,改变![]() ,
,![]() 的去除率变化情况如图乙所示。
的去除率变化情况如图乙所示。
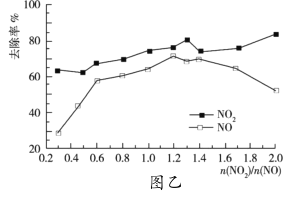
①当![]() 大于1.4时,
大于1.4时,![]() 去除率升高,但
去除率升高,但![]() 的去除率却降低。其可能的原因是__;
的去除率却降低。其可能的原因是__;
②![]() 和
和![]() 发生的主要反应为
发生的主要反应为![]() 。保持
。保持![]() 的初始浓度不变,改变
的初始浓度不变,改变![]() ,将反应后的混合气体通入
,将反应后的混合气体通入![]() 乳浊液中吸收。为节省
乳浊液中吸收。为节省![]() 的用量,又能保持
的用量,又能保持![]() 去除效果,则
去除效果,则![]() 合适的值约为___________;
合适的值约为___________;
(4)已知:![]() ,
,![]() ,则
,则![]() ______________________。
______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com