
【题目】《天工开物》记载:“凡埏泥造瓦,掘地二尺余,择取无砂粘土而为之”,“凡坯既成,干燥之后,则堆积窖中燃薪举火”,“浇水转釉(主要为青色),与造砖同法”。下列说法错误的是
A. 粘土是制作砖瓦和陶瓷的主要原料
B. “燃薪举火”使粘土发生复杂的物理化学变化
C. 沙子和粘土的主要成分均为硅酸盐
D. 烧制后自然冷却成红瓦,浇水冷却成青瓦
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源: 题型:
【题目】下列属于氧化还原反应的是
A. 2Na+2H2O![]() 2NaOH+H2↑+Cl2↑ B. NaOH+HCl═NaCl+H2O
2NaOH+H2↑+Cl2↑ B. NaOH+HCl═NaCl+H2O
C. CaO+H2O═Ca(OH)2 D. NH4Cl![]() NH3↑+HCl↑
NH3↑+HCl↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
实验序号 | A溶液 | B溶液 |
① | 20 mL 0.1 mol·L-1H2C2O4溶液 | 30 mL 0.01 mol·L-1KMnO4溶液 |
② | 20 mL 0.2 mol·L-1H2C2O4溶液 | 30 mL 0.01 mol·L-1KMnO4溶液 |

(1)该反应的离子方程式 。(已知H2C2O4是二元弱酸)
(2)该实验探究的是 因素对化学反应速率的影响。相同时间内针筒中所得CO2的体积大小关系是 < (填实验序号)。
(3)若实验①在2 min末收集了2.24 mL CO2(标准状况下),则在2 min末, c(MnO4-)=__________mol/L(假设混合液体积为50 mL)
(4)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定 来比较化学反应速率。(一条即可)
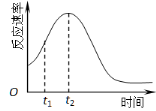 (5)小组同学发现反应速率总是如图,其中t1~t2时间内速率变快的主要原因可能是:
(5)小组同学发现反应速率总是如图,其中t1~t2时间内速率变快的主要原因可能是:

① ;② 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯酸钾和浓盐酸之间有下列反应:2KClO3 + 4HCl(浓)== 2 KCl + Cl2↑+ 2ClO2 + 2H2O。
(1)该反应中发生还原反应的物质是__________。氧化产物是___________。
(2)用双线桥标出方程式中的电子得失___________。
2KClO3 + 4HCl(浓)== 2 KCl + Cl2↑+ 2ClO2 + 2H2O
(3)当有0.2mol电子发生转移时,生成的氯气的体积为_____L(标准状况)。被氧化的HCl的物质的量为____mol。
(4)若分别用①KMnO4(还原产物是Mn2+)②MnO2(还原产物是Mn2+)③Ca(ClO)2(还原产物是Cl2)氧化浓盐酸制备氯气,当浓盐酸足量且这三种氧化剂的物质的量相同时,生成氯气的物质的量最少的是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列10种物质:①饱和食盐水;②乙醇;③铁片;④液态硫酸;⑤碳酸钙固体⑥干冰;⑦熔融硫酸钾;⑧铝条;⑨烧碱;⑩石墨。
(1)用序号回答,能导电的是_____。属于电解质的是_____。属于非电解质的是_____。
(2)写出③与水反应的化学方程式,并用单线桥表示电子转移的方向和数目__________。
(3)写出⑧与⑨的水溶液反应的离子方程式是_______________________。
(4)储氢纳米碳管的成功研制体现了科技的进步。用电弧法合成的碳纳米管常伴有大量的杂质-碳纳米颗粒。这种碳纳米颗粒可用氧化气化法提纯。其反应中的反应物和生成物有C、CO2、H2SO4、K2Cr2O7、K2SO4、Cr2(SO4)3和H2O 七种。请用上述物质填空并配平化学方程式:
C +_____ +□H2SO4-□ +□ +□Cr2(SO4)3+□H2O。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在等温等压条件下,化学反应方向的判据为:ΔH-TΔS<0 反应能正向自发进行,ΔH-TΔS=0 反应达到平衡状态, ΔH-TΔS>0 反应不能自发进行。设反应A=D+E ΔH-TΔS=(-4 500+11T) J·mol-1,要防止反应发生,温度必须( )
A.高于409 KB.低于136 K
C.高于136 K而低于409 KD.低于409 K
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了探究“二氧化碳是否在有水存在时才能和过氧化钠反应”,某课题研究小组的同学们设计了如下图的实验装置,分别进行了甲、乙两次实验:
实验甲:干燥的二氧化碳和过氧化钠的反应。在干燥的试管Ⅱ中装入Na2O2,在通入CO2之前,关闭K1和K2。在试管Ⅰ内装入试剂X后,打开K1和K2,通入CO2,几分钟后,将带火星的木条插入试管Ⅲ的液面上,观察到木条不复燃,且Ⅱ中的淡黄色没有变化。
实验乙:潮湿的二氧化碳和过氧化钠的反应。在试管Ⅰ内装入试剂Y,其他操作同实验甲,观察到木条复燃,且Ⅱ中的淡黄色变为白色。

试回答下列问题:
(1)在装入Na2O2后,通入CO2前,关闭K1和K2的目的是_________________________________________________________。
(2)在实验甲中,试剂X是______________;在实验乙中,试剂Y是_____________。
(3)根据上述两个实验现象,得到的结论是___________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com