
【题目】关于晶体的叙述中,正确的是( )
A.原子晶体中,共价键的键能越大,熔、沸点越高
B.分子晶体中,分子间的作用力越大,该分子越稳定
C.分子晶体中,共价键的键能越大,熔、沸点越高
D.某晶体溶于水后,可电离出自由移动的离子,该晶体一定是离子晶体
科目:高中化学 来源: 题型:
【题目】白酒、食醋、蔗糖、淀粉等均为家庭厨房中常用的物质,利用这些物质能完成下列实验的是
①检验自来水中是否含氯离子 ②鉴别食盐和小苏打 ③蛋壳能否溶于酸 ④白酒中是否含甲醇
A. ①②B. ①④C. ②③D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)向AlCl3溶液中,滴加少量NaOH溶液,现象是________________________
继续滴加NaOH溶液至过量,现象是_______________。
(2)钠与水反应的离子方程式为_______________,该反应中氧化剂是_______________,产生1mol H2时,转移电子的物质的量为_______________mol。
(3)经常有人因误食亚硝酸钠(NaNO2)而中毒。原因是NaNO2像食盐一样既有咸味,又有很强毒性。已知亚硝酸钠能发生如下反应:2NaNO2+4HI=2NO+I2+2NaI+2H2O
①该反应的氧化剂是_______,被氧化的是_________元素。
②若此反应中电子转移数目为0.5mol,则被氧化的还原剂的物质的量为___________。
【答案】 产生白色沉淀 白色沉淀消失 2Na + 2H2O ![]() 2Na++ 2OH- + H2↑ 水或H2O 2 NaNO2 碘(或I) 0.5 mol
2Na++ 2OH- + H2↑ 水或H2O 2 NaNO2 碘(或I) 0.5 mol
【解析】(1)向AlCl3溶液中,滴加少量NaOH溶液,发生反应AlCl3+3NaOH═Al(OH)3↓+3NaCl,现象是产生白色沉淀;继续滴加NaOH溶液至过量,发生反应Al(OH)3+NaOH═NaAlO2+2H2O,现象是白色沉淀消失;(2)钠与水反应生成氢氧化钠与氢气,反应离子方程式为:2Na + 2H2O ![]() 2Na++ 2OH- + H2↑,反应中水中H元素化合价由+1价降低为0价,水是氧化剂,生成1molH2时转移电子的物质的量为1mol×2=2mol;(3)①反应:2NaNO2+4HI=2NO+I2+2NaI+2H2O中,元素化合价的变化分别如下:氮元素:NaNO2 →NO,由+3价→+2价,得电子,所以NaNO2是氧化剂;碘元素,HI→I2,由-1价→0价,失电子,被氧化的是碘元素;②根据反应:2NaNO2+4HI=2NO+I2+2NaI+2H2O可知,若此反应中电子转移数目为0.5mol,则被氧化的还原剂的物质的量为0.5 mol。
2Na++ 2OH- + H2↑,反应中水中H元素化合价由+1价降低为0价,水是氧化剂,生成1molH2时转移电子的物质的量为1mol×2=2mol;(3)①反应:2NaNO2+4HI=2NO+I2+2NaI+2H2O中,元素化合价的变化分别如下:氮元素:NaNO2 →NO,由+3价→+2价,得电子,所以NaNO2是氧化剂;碘元素,HI→I2,由-1价→0价,失电子,被氧化的是碘元素;②根据反应:2NaNO2+4HI=2NO+I2+2NaI+2H2O可知,若此反应中电子转移数目为0.5mol,则被氧化的还原剂的物质的量为0.5 mol。
【题型】综合题
【结束】
19
【题目】国际化学年的中国宣传口号是“化学-----我们的生活,我们的未来”。学习化学应该明白“从生活中来,到生活中去”道理。请填空:
(1)①若金属钠等活泼金属着火时,应该_______________用来灭火。
②经火焰灼烧,焰色反应为浅紫色(透过蓝色钴玻璃)的元素是。_______________
③胃舒平(含有氢氧化铝)可治疗胃酸过多,其反应的离子反应方程式为:_______________。
④明矾能净水,其电离方程式是_______________。
(2)过氧化钠作潜艇供氧剂时发生的化学反应方程式是_____________。
(3)加热Al片的实验现象是_________________,原因是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将7.8克镁和铝的混合粉末溶于900ml浓度为1mol/L的盐酸中,完全反应可收集到标准状况下气体8.96升,向反应后的混合溶液中逐滴加入2mol/L的氢氧化钠溶液,试计算:
(1)原金属混合物中含铝克;
(2)当加入ml氢氧化钠溶液时,Mg2+、Al3+恰好完全沉淀;
(3)当再加入ml氢氧化钠溶液时,Al(OH)3恰好完全溶解,此时可得沉淀克.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一定体积CH4、C2H6、C3H8组成的混合气体,是同温同压下H2密度的15倍。则混合气体中CH4、C2H6、C3H8、的体积比不可能是: ( )
A. 2∶1∶2 B. 2∶3∶1 C. 1∶4∶1 D. 5∶3∶5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业产生的废气COX、NOX、SOX 对环境有害,若能合理的利用吸收,可以减少污染,变废为宝.
(1)有一种用CO2生产甲醇燃料的方法:CO2+3H2CH3OH+H2O 已知:CO2(g)+3H2(g)═CH3OH(g)+H2O(l)△H=﹣akJmol﹣1;
2H2(g)+O2(g)═2H2O(l)△H=﹣b kJmol﹣1;
CH3OH(g)═CH3OH(l)△H=﹣c kJmol﹣1;
则表示CH3OH(l)燃烧热的热化学方程式为: .
(2)光气(COCl2)是一种重要的化工原料,用于农药、医药、聚酯类材料的生产,工业上通过Cl2(g)+CO(g)COCl2(g)制备.图1为此反应的反应速率随温度变化的曲线,图2为某次模拟实验研究过程中容器内各物质的浓度随时间变化的曲线.回答下列问题: 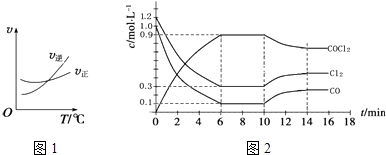
①0~6min内,反应的平均速率v(Cl2)=;
②10min改变的条件是 , 该反应平衡常数变化的趋势是(填“增大”、“减小”或“不变”).
(3)利用氨水可以将SO2和NO2吸收,原理如图3所示:NO2被吸收的离子方程式是 . 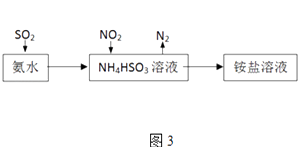
(4)用粗硅作原料,熔融盐电解法制取硅烷原理如图4,判断B为电源的极,电解时阳极的电极反应式为 . 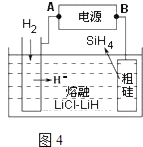
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com