
【题目】设 NA 表示为阿伏加德罗常数,下列叙述中,正确的是( )
A.常温常压下,16 g O2和O3的混合物中共含有NA个氧原子
B.假设1 mol氯化铁完全转化为氢氧化铁胶体,则分散系中胶体微粒数为NA
C.78 g Na2O2 固体中所含阴、阳离子总数为4NA
D.在铜与硫有反应中,1 mol铜原子参加反应失去的电子数为2NA
【答案】A
【解析】
A. O2和O3都是由O原子构成,16 g O2和O3的混合物中含氧原子物质的量n(O)=![]() =1 mol,则含O原子的数目为NA个,A正确;
=1 mol,则含O原子的数目为NA个,A正确;
B. 氯化铁完全转化为氢氧化铁胶体,由于胶粒是许多Fe(OH)3的集合体,则1 mol氯化铁水解产生胶体微粒数小于NA,B错误;
C. 78 g Na2O2固体物质的量为1 mol,其中含2 mol Na+,1 mol O22﹣,含离子总物质的量是3 mol,C错误;
D. Cu与S发生反应生成Cu2S,铜元素化合价从0价变化为+1价,1 mol Cu原子参加反应失去 1 mol电子,故转移的电子数为NA,D错误;
故合理选项是A。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】硼铁混合精矿含有硼镁石[MgBO2(OH)]、磁铁矿(Fe3O4) 、磁黄铁矿(Fe2S)、晶质铀矿(UO2)等,以该矿为原料制备MgSO4H2O和硼酸(H3BO3)的工艺流程如下:
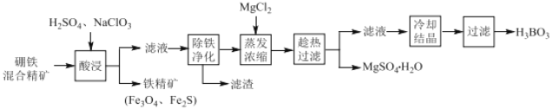
已知:UO22+在pH为4~5的溶液中生成UO2(OH)2沉淀。
回答下列问题:
(1)“酸浸”时,为了提高浸出率可采取的措施有:_______________________(至少答两个措施),该步骤中NaClO3可将UO2转化为UO22+,则该反应的离子方程式为 ________ 。
(2)“除铁净化”需要加入 ______ (填化学式)把溶液pH调节至4~5,滤渣的成分是____。
(3)“蒸发浓缩”时,加入固体MgCl2的作用是 ______________________ 。
(4)铁精矿(Fe3O4、Fe2S)经过一系列加工后,可用于制备氢氧化铁固体。已知T℃Ksp[Fe(OH)3]=4.0×10-39、Ksp[Fe(OH)2]=8.0×10-16 、Kw=10-a,回答下列问题:
①在T℃,假设Fe3+水解的离子方程式是:Fe3+(aq)+3H2O(l)= Fe(OH)3 (s)+3H+(aq),则该条件下Fe3+水解反应的平衡常数K=___________(用含a的字母表示)。
②在T℃向饱和的Fe(OH)3、Fe(OH)2混合溶液中,加入少量NaOH固体(忽略溶液体积变化),则溶液中的![]() 会________(填“变大”“变小”或“不变”),请结合相关数据推理说明:____________________________ 。
会________(填“变大”“变小”或“不变”),请结合相关数据推理说明:____________________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NaHC2O4溶液的pH < 7。常温下,向pH=8.4的Na2C2O4溶液中滴加0.1mol/L的HCl溶液,溶液pH与pOH[pOH=-lgc(OH-)]的变化关系如图所示,下列各点所示溶液中微粒的物质的量浓度关系一定正确的是

A. a点:c(H+)+c(HC2O4-)+2c(H2C2O4)=c(OH-)
B. b点:c(Cl-)>c(H2C2O4)+c(HC2O4-)+c(C2O42-)
C. c点:c(Na+)=c(HC2O4-)+ c(C2O42-)+c(Cl-)
D. d点:c(OH-)+ c(Cl-)>c(H+)+2c(H2C2O4)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)葡萄酒中SO2最大使用量为0.25 g·L-1,取300.00 mL葡萄酒,通过适当的方法使 所含SO2全部逸出并用H2O2将其全部氧化为H2SO4,然后用0.090 0 mol·L-1NaOH标准溶液进行滴定。
①滴定前排气泡时,应选择下图中的________(填序号)。
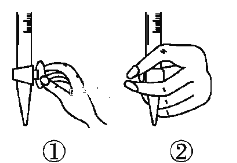
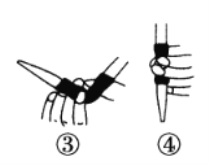
②若用50 mL滴定管进行实验,当滴定管中的液面在刻度“10”处,则管内液体的体积___(填序号)。
①=10 mL ②=40 mL ③<10 mL ④>40 mL。
③上述滴定实验中,可选择___为指示剂,选择该指示剂时如何判断反应到达滴定终点:_____。
④滴定终点读数时俯视刻度线,则测量结果比实际值________(填“偏高”、“偏低”或“无影响”)。
(2)某学生用0.100molL-1的KOH标准溶液滴定未知浓度的盐酸,其操作为:
A.移取20mL待测盐酸溶液注入洁净的锥形瓶中,并加入2~3滴酚酞;
B.用标准溶液润洗滴定管2~3次;
C.把盛有标准溶液的碱式滴定管固定好,调节滴定管使尖嘴处充满溶液;
D.取标准KOH溶液注入碱式滴定管至刻度“0”以上2~3cm 处;
E.调节液面至“0”或“0”以下刻度,记下读数;
F.把锥形瓶放在滴定管下面,用标准KOH溶液滴定至终点并记下刻度。
实验编号 | KOH溶液的浓度(mol/L) | 滴定完成时,KOH溶液滴入的体积(mL) | 待测盐酸溶液的体积(mL) |
1 | 0.10 | 22.62 | 20.00 |
2 | 0.10 | 22.72 | 20.00 |
3 | 0.10 | 22.80 | 20.00 |
①正确操作步骤的顺序是(用序号字母填写)___________________________
②根据上述数据,可计算出该盐酸的浓度约为______________(保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】福酚美克是一种影响机体免疫力功能的药物,可通过以下方法合成:
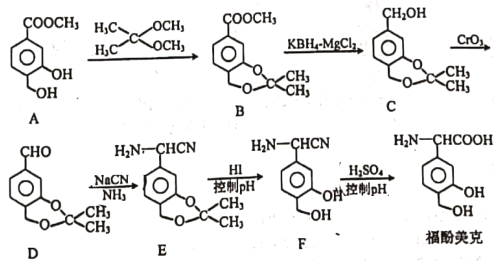
(1)B中的含氧官能团有________和_________(填名称);
(2)C→D的转化属于_________反应(填反应类型).
(3)已知E→F的转化属于取代反应,则反应中另—产物的结构简式为______。
(4) A (C9H10O4)的一种同分异构体X满足下列条件:
I.X分子有中4种不同化学环境的氢。
II. X能与FeCl3溶液发生显色反应。
III. lmol X最多能与4 mol NaOH发生反应
写出该同分异构体的结构简式:_____________。
(5)已知:![]()
![]()
![]() +R3CHO,根据已有知识并结合相关信息.
+R3CHO,根据已有知识并结合相关信息.
写出以  为原料制备
为原料制备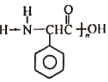 的合成路线流程图(无机试剂任用)。____________
的合成路线流程图(无机试剂任用)。____________
合成路线流程图示例如下:CH3CH2Br![]() CH3CH2OH
CH3CH2OH ![]() CH3COOCH2CH3
CH3COOCH2CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列装置由甲、乙两部分组成(如图所示),甲是将废水中乙二胺[H2N(CH2)2NH2]氧化为环境友好物质形成的化学电源。当电池工作时,下列说法错误的是( )
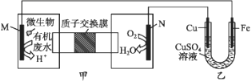
A. 甲中H+透过质子交换膜由左向右移动
B. M极电极反应式:H2N(CH2)2NH2+4H2O-16e-![]() 2CO2↑+N2↑+16H+
2CO2↑+N2↑+16H+
C. 一段时间后,乙中CuSO4溶液浓度基本保持不变
D. 当N极消耗0.25 mol O2时,则铁极增重16 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定的条件下,下列选项所示的物质间转化均能实现的是( )
A.Na ![]() Na2O
Na2O![]() NaOH
NaOH
B.MgCO3![]() MgCl2
MgCl2![]() Mg
Mg
C.Al2O3![]() Al
Al![]() Fe
Fe
D.Fe2O3![]() FeCl3
FeCl3![]() FeCl2(aq)
FeCl2(aq)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙二醛(OHC–CHO)是重要的精细化工产品。工业上电解乙二醛和盐酸的混合液制备乙醛酸(OHC–COOH)的装置如图所示,通电后,阳极产物将乙二醛氧化为乙醛酸。下列说法错误的是()
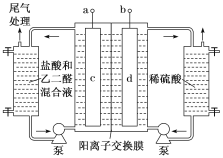
A.a为电源的正极,c电极反应式为2Cl–-2e–=Cl2
B.当1mol乙二醛氧化成1mol乙醛酸时,阴极生成22.4L(标准状况)气体
C.电解过程中稀H2SO4电解液的浓度保持不变
D.阳极液中盐酸的作用有生成氧化剂、增强溶液导电性、提供离子平衡阴极区电荷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学探究Ba(OH)2和H2SO4反应的实质,利用下图装置进行实验。向20 ml 0.01 mol/L Ba(OH)2 溶液中滴入几滴酚酞溶液,然后向其中匀速逐滴加入2 ml 0.2 mol/L H2SO4溶液。

(1)实验过程中溶液中的现象为________、 ________。
(2)该反应的离子方程式是__________________。
(3)画出反应过程中溶液电导率变化示意图__________________。
(4)解释反应过程中溶液电导率出现上述变化的原因___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com