
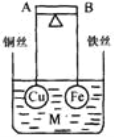
【题目】如图所示,杠杆 AB 两端分别挂有体积相同.质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向烧杯中央滴入 M 的浓溶液,一段时间后, 下列有关杠杆的偏向判断正确的是(实验过程中,不考虑两球的浮力变化)( )
A. 当 M为盐酸、杠杆为导体时,A 端高,B 端低
B. 当 M为 AgNO3、杠杆为导体时,A 端高,B 端低
C. 当 M为 CuSO4、杠杆为导体时,A 端低,B 端高
D. 当 M为 CuSO4、杠杆为绝缘体时,A 端低,B 端高
【答案】C
【解析】
A. 当 M为盐酸、杠杆为导体时,该装置形成原电池,铁为负极,铜为正极,铁不断的溶解质量减少,铜球上溶液中的氢离子反应生成氢气,所以B端质量减少,A端质量不变,会出现A 端低,B 端高的现象,故错误;B. 当 M为 AgNO3、杠杆为导体时,铁为原电池的负极,质量减少,铜为原电池的正极,银离子得到电子生成银,铜球的质量增加,所以A 端低,B 端高,故错误;C. 当 M为 CuSO4、杠杆为导体时,铁为原电池的负极,溶解质量减少,铜为原电池的正极,溶液中的铜离子得到电子生成铜单质,铜球质量增加,A 端低,B 端高,故正确。D. 当 M为 CuSO4、杠杆为绝缘体时,不能形成原电池,铁和硫酸铜反应生成硫酸亚铁和铜,铁球质量增加,铜球质量不变,A 端高,B 端低,故错误。故选C。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
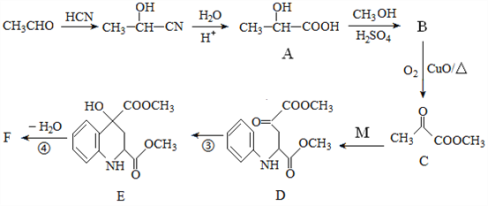
【题目】药物F具有抗肿瘤、降血糖、降血压等多种生物活性,其合成路线如下:
已知:M的结构简式为: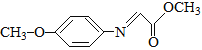 。
。
请回答下列问题:
(1)A的化学名称是_______________,③的反应类型是___________。
(2)C中官能团的名称是__________________________。
(3)写出F的结构简式__________________________。
(4)已知A在一定条件下能生成可降解的聚酯,请写出该反应化学方程式:_____________。
(5)满足下列条件的M的同分异构体有_______种(不含立体异构)。
①能够发生银镜反应。
②含有硝基(–NO2),且硝基直接连在苯环上。
③含有苯环且苯环上只有两个取代基。
其中核磁共振氢谱为四组峰且峰面积之比为6∶2∶2∶1的结构简式为________(写出一种即可)。
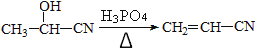
(6)写出用乙醛为原料制备高分子化合物聚丙烯腈的合成路线(无机试剂任选):____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某芳香烃A,其相对分子质量为104,碳的质量分数为92.3%。
(1)A的分子式为________________。
(2)A可与溴的四氯化碳溶液反应,其化学方程式为____________________,该反应类型为_______。
(3)已知:![]()
![]()
![]() 。则A与稀、冷的KMnO4溶液在碱性条件下反应的过程可表示:_____________。
。则A与稀、冷的KMnO4溶液在碱性条件下反应的过程可表示:_____________。
(4)一定条件下,A与氢气反应,得到的化合物中碳的质量分数为85.7%,写出此化合物的结构简式__________________。
(5)在一定条件下,由A聚合得到的高分子化合物的结构简式为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是几种常见的化学电源示意图,有关说法不正确的是

A. 上述电池分别属于一次电池、二次电池和燃料电池
B. 干电池在长时间使用后,锌筒被破坏
C. 铅蓄电池工作过程中,每通过2mol电子,负极质量减轻207g
D. 氢氧燃料电池是一种具有应用前景的绿色电源
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】联氨(N2H4)常温下为无色液体,可用作火箭燃料。下列说法不正确的是( )
①2O2(g)+N2(g)=N2O4(l) ΔH1
②N2(g)+2H2(g)= N2H4(l) ΔH2
③O2(g)+2H2(g)=2H2O(g) ΔH3
④2 N2H4(l)+N2O4(l)=3N2(g)+4H2O(g) ΔH4=1048.9 kJ·mol-1
A. ΔH4﹦2ΔH32ΔH2ΔH1
B. O2(g)+2H2(g)![]() 2H2O(l) ΔH5,ΔH5>ΔH3
2H2O(l) ΔH5,ΔH5>ΔH3
C. 1 mol O2(g)和2 mol H2(g)具有的总能量高于2 mol H2O(g)
D. 联氨和N2O4作火箭推进剂的原因之一是反应放出大量的热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究Na2SO3溶液的性质,在白色点滴板的a、b、c、d四个凹槽中滴入Na2SO3溶液,再分别滴加下图所示的试剂。

下列关于实验现象的解释或结论正确的是
选项 | 实验现象 | 解释或结论 |
A | a中无明显现象 | Na2SO3和H2O2一定不发生反应 |
B | b中加稀H2SO4后才产生淡黄色沉淀 | SO32和S2两种离子一定不能大量共存 |
C | c中加BaCl2溶液后产生白色沉淀且红色褪去 | Ba2++ SO32 == BaSO3↓,使SO32水解平衡逆向移动,红色褪去 |
D | d中产生白色沉淀 | 原Na2SO3溶液中含有SO42 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化不可能通过一步实现直接完成的是( )
A.Al(OH)3→Al2O3B.Al2O3→Al(OH)3
C.Al→NaAlO2D.AlCl3→Al(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)高铁酸钾(K2FeO4)不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。如图是高铁电池的模拟实验装置:

①该电池放电时正极的电极反应式为_______________________________________;若维持电流强度为1 A,电池工作十分钟,理论上消耗Zn______ g(计算结果保留一位小数,已知F=96500 C·mol-1)。
②盐桥中盛有饱和KCl溶液,此盐桥中氯离子向______(填“左”或“右”)移动;若用阳离子交换膜代替盐桥,则钾离子向________(填“左”或“右”)移动。
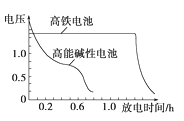
③下图为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有__________。
(2)有人设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图所示,电池正极的电极反应式是__________________________,A是________。

(3)利用原电池工作原理测定汽车尾气中CO的浓度,其装置如图所示。该电池中O2-可以在固体介质NASICON (固溶体)内自由移动,工作时O2-的移动方向________(填“从a到b”或“从b到a”),负极发生的电极反应式为__________________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数值。下列有关叙述正确的是( )
A. 14 g乙烯和丙烯混合气体中的氢原子数为2NA
B. 1 mol N2与4 mol H2反应生成的NH3分子数为2NA
C. 1 mol Fe溶于过量硝酸,电子转移数为2NA
D. 标准状况下,2.24 L CCl4含有的共价键数为0.4NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com