
【题目】大气污染越来越成为人们关注的问题,烟气中的NOx必须脱除(即脱硝)之后才能排放。
(1)CO和H2可作为能源和化工原料,应用十分广泛。 反应CO(g)+H2O(g) ![]() H2(g)+CO2(g)的平衡常数随温度的变化如表所示。
H2(g)+CO2(g)的平衡常数随温度的变化如表所示。
温度/℃ | 400 | 500 | 830 | 1 000 |
平衡常数K | 10 | 9 | 1 | 0.6 |
①从上表可以推断:此反应是__________(填“吸”或“放”)热反应。
②在830 ℃下,若开始时向恒容密闭容器中充入CO与H2O均为1 mol,则达到平衡后CO的转化率为________。
(2)在汽车尾气系统中装置催化转化器,可有效降低NOx和CO的排放。
已知:①2CO(g)+O2(g) ![]() 2CO2(g) ΔH=566.0 kJ·mol1
2CO2(g) ΔH=566.0 kJ·mol1
②N2(g)+O2(g) ![]() 2NO(g) ΔH=+180.0 kJ·mol1
2NO(g) ΔH=+180.0 kJ·mol1
③2NO(g)+O2(g) ![]() 2NO2(g) ΔH=116.5 kJ·mol1
2NO2(g) ΔH=116.5 kJ·mol1
回答下列问题:
①CO的燃烧热为 _________。若1 mol N2(g)、1 mol O2(g) 分子中化学键断裂时分别需要吸收946 kJ、498 kJ的能量,则1 mol NO(g) 分子中化学键断裂时需吸收的能量为_________kJ。
②写出CO将NO2还原为单质反应的热化学方程式为 ____________________
(3)汽车排气管上的催化转化器,发生上述的CO将NO2还原为单质反应。在一定温度下,将一定量的CO和NO2充入2L固定容积的容器中,回答以下问题:
①能说明该反应达到平衡状态的是_____________(填字母标号)。
A.2υ正(NO2)=υ逆(N2)
B. 混合气体的平均相对分子质量保持不变
C.气体总压强不再变化
D. ΔH保持不变
E.混合气体的密度不再变化
②从反应开始到5min,生成了0.08mol N2,则5min内υ(CO)=___molL1min1。
③25min时,物质浓度变化如图所示,则改变的条件可能是___________(填字母标号)。
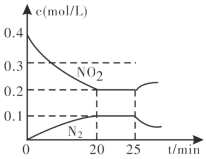
A.缩小容器体积
B.增加NO2的浓度
C.降低温度
D.升高温度
【答案】放 50% 283kJ/mol 631.75 2NO2(g)+4CO(g)=N2(g)+4CO2(g) ΔH= -1196kJ/mol BC 0.032 D
【解析】
(1)①由表中数据可知,升高温度,K变小,说明反应逆向进行,即正反应为放热反应;
②在830 ℃下,K=1,故可利用K和三段式计算CO的转化率;
(2) ①根据燃烧热的概念判断,反应热与键能的关系计算;
②根据盖斯定律计算此反应的反应热,写出热化学方程式;
(3)①可逆反应达到平衡状态,一定满足正逆反应速率相等,各组分的浓度、百分含量不再变化,据此进行判断;
②前5min 内N2变化浓度为0.04mol/L,根据平均反应速率公式计算CO的平均反应速率;
③根据反应的特点,浓度、压强、温度对化学平衡的影响分析解答。
(1)①由表中数据可知,升高温度,K变小,说明反应逆向进行,即正反应为放热反应;
②在830 ℃下,K=1,设转化CO物质的量为x
CO(g)+H2O(g) ![]() H2(g)+CO2(g)
H2(g)+CO2(g)
起始(mol) 1 1 0 0
转化(mol) x x x x
平衡(mol) 1-x 1-x x x
平衡常数K=![]() =
=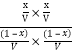 =1,解得,x=0.5,即CO转化率为
=1,解得,x=0.5,即CO转化率为![]() 100%=50%;
100%=50%;
因此,本题正确答案是:放;50%;
(2) ①已知2CO(g)+O2(g) ![]() 2CO2(g) ΔH=566.0 kJ·mol1,可以知道1molCO完全燃烧生成1molCO2时释放的能量为
2CO2(g) ΔH=566.0 kJ·mol1,可以知道1molCO完全燃烧生成1molCO2时释放的能量为![]() =283kJ,则CO的燃烧热为283kJ/mol;
=283kJ,则CO的燃烧热为283kJ/mol;
由反应②可知,1molN2(g)和1molO2反应生成2molNO(g)吸收180.0 kJ热量,根据反应热与键能的关系可得946 kJ·mol1+498 kJ·mol1-2![]() E(氮氧键)= 180.0 kJ·mol1,则有E(氮氧键)= 631.75 kJ·mol1;
E(氮氧键)= 180.0 kJ·mol1,则有E(氮氧键)= 631.75 kJ·mol1;
②CO将NO2还原为单质的化学方程式为2NO2(g)+4CO(g)=N2(g)+4CO2(g),结合反应:
①2CO(g)+O2(g) ![]() 2CO2(g) ΔH=566.0 kJ·mol1
2CO2(g) ΔH=566.0 kJ·mol1
②N2(g)+O2(g) ![]() 2NO(g) ΔH=+180.0 kJ·mol1
2NO(g) ΔH=+180.0 kJ·mol1
③2NO(g)+O2(g) ![]() 2NO2(g) ΔH=116.5 kJ·mol1
2NO2(g) ΔH=116.5 kJ·mol1
根据盖斯定律可以知道,①![]() 2-②-③可得: 2NO2(g)+4CO(g)=N2(g)+4CO2(g),则ΔH =(566.0 kJ·mol1)
2-②-③可得: 2NO2(g)+4CO(g)=N2(g)+4CO2(g),则ΔH =(566.0 kJ·mol1)![]() 2-(+180.0 kJ·mol1)-(116.5 kJ·mol1),则CO将NO2还原为单质的热化学方程式为:2NO2(g)+4CO(g)=N2(g)+4CO2(g) ΔH= -1196kJ/mol,
2-(+180.0 kJ·mol1)-(116.5 kJ·mol1),则CO将NO2还原为单质的热化学方程式为:2NO2(g)+4CO(g)=N2(g)+4CO2(g) ΔH= -1196kJ/mol,
因此,本题正确答案是:283kJ/mol ;631.75 ;2NO2(g)+4CO(g)=N2(g)+4CO2(g) ΔH= -1196kJ/mol;
(3)①A. 反应2NO2(g)+4CO(g) N2(g)+4CO2(g)中,若2υ正(NO2)=υ逆(N2),说明正反应速率和逆反应速率不相等,不能说明反应达到平衡状态;
B. 混合气体的质量始终不变,气体的总物质的量不确定,则混合气体的相对分子质量为变量,当容器内混合气体的平均相对分子质量保持不变时,说明反应达到平衡状态;
C. 在恒温、恒容条件下,反应2NO2(g)+4CO(g) N2(g)+4CO2(g)进行过程中气体总物质的量不断变化,压强也在变化,当容器内混合气体的压强保持不变,说明达到平衡状态;
D. 反应热大小只与起始和终止状态有关,ΔH保持不变,不能说明反应达到平衡状态;
E.混合气体的质量和体积始终不变,则容器内混合气体的密度保持不变,混合气体的密度不再变化不能说明反应达到平衡状态。
因此,本题正确答案是:BC;
②2NO2(g)+4CO(g)=N2(g)+4CO2(g),从反应开始到5min,生成了0.08mol N2,
则5min内υ(CO)=![]() =0.032molL1min1;
=0.032molL1min1;
因此,本题正确答案是:0.032;
③由图像可知,25min时,改变条件的瞬间NO2和N2的浓度都不变,改变条件后,NO2浓度增大,N2浓度减小,说明平衡逆向移动,故改变的条件应该是升高温度,选D,
因此,本题正确答案是:D。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】雾霾天气严重影响人们的生活,其中氮氧化物和硫氧化物是造成雾霾天气的主要原因之一,以下方法可以消除氮氧化物和硫氧化物的污染。
(1)用活性炭还原法可处理氮氧化物,向某密闭容器中加入一定量的活性炭和NO,发生反应:![]() △H<0,在一定条件下,反应进行到不同时间测得各物质的浓度如下表。
△H<0,在一定条件下,反应进行到不同时间测得各物质的浓度如下表。
时间/min 浓度/mol·L-1 | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.00 | 0.52 | 0.40 | 0.40 | 0.44 | 0.44 |
N2 | 0 | 0.24 | 0.30 | 0.30 | 0.28 | 0.28 |
CO2 | 0 | 0.24 | 0.30 | 0.30 | 0.28 | 0.28 |
①0~10min内,NO的平均反应速率v(NO)=_______________。
②在恒容条件下,能判断该反应一定达到化学平衡状态的标志是_________(填字母编号)。
a.v正(N2)=2v逆(NO) b.反应体系的压强不再发生改变
c.![]() 不变 d.混合气体的密度保持不变
不变 d.混合气体的密度保持不变
③30min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是___________。
(2)NH3催化还原氮氧化物技术是目前应用最广泛的烟气氮氧化物脱除技术。已知c(NO2):c(NO)=1:1时脱氮效果最佳,若生成1mol N2时反应放出的热量为Q kJ。此时对应的脱氮反应的热化学方程式为_____________________________________________________。
(3)利用钠碱循环法可脱除烟气中的SO2。
①在钠碱循环法中,Na2SO3溶液作为吸收液,可由NaOH溶液吸收SO2制得,该反应的离子方程式是_____________________。
②吸收液吸收SO2的过程中,pH随n(![]() ):n(
):n(![]() )变化关系如下表:
)变化关系如下表:
n( | 91:9 | 1:1 | 9:91 |
pH | 8.2 | 7.2 | 6.2 |
当吸收液的pH降至约为6时,需送至电解槽再生。再生示意图如下:
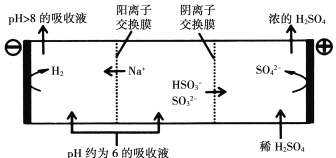
写出![]() 在阳极放电的电极反应式:_______________________________________,当阴极室中溶液pH升至8以上时,吸收液再生并循环利用。
在阳极放电的电极反应式:_______________________________________,当阴极室中溶液pH升至8以上时,吸收液再生并循环利用。
(4)利用喷雾干燥法脱硫工艺是除去SO2的常见方法,先将含SO2的废气溶于水,再用饱和石灰浆吸收。该温度下吸收液中c(Ca2+)一直保持为0.50 mol·L-1,已知KSP(CaSO3)=1.4×10-7,求吸收后溶液中![]() 的浓度______________________。
的浓度______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F、G是前四周期的七种元素,其原子序数依次增大。A的基态原子中没有成对电子;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D及其同主族元素的氢化物沸点变化趋势如图(D的氢化物沸点最高);F是地壳中含量最高的金属元素;G与F同主族。请回答下列问题:
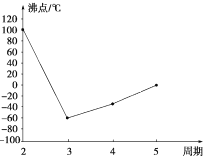
(1)写出F元素基态原子的核外电子排布式:____________。
(2)B、C、D三种元素电负性由大到小的顺序是____________(用元素符号表示)。
(3)有关上述元素的下列说法,正确的是________(填序号)。
①CA3沸点高于BA4,主要是因为前者相对分子质量较大
②配合物Ni(BD)4常温下为液态,易溶于CCl4、苯等有机溶剂,因此固态Ni(BD)4属于离子晶体
③C的氢化物的中心原子采取sp2杂化
④F单质的熔点高于E单质,是因为F单质的金属键较强
⑤比G的原子序数少1的元素第一电离能高于G
(4)CA3分子的立体构型为________,1 mol B2A4分子中含有________个σ键;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NH4HCO3![]() NH3↑+CO2↑+H2O↑。为了将混有硫酸钠、碳酸氢铵的NaCl提纯,并制得纯净的NaCl溶液,某学生设计如下实验方案:
NH3↑+CO2↑+H2O↑。为了将混有硫酸钠、碳酸氢铵的NaCl提纯,并制得纯净的NaCl溶液,某学生设计如下实验方案:
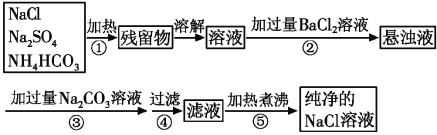
(1)操作④中所需的玻璃仪器有_________________________________。
(2)操作②为什么不用硝酸钡溶液,其理由是________________________________。
(3)进行操作②后,如何判断SO![]() 已除尽,方法是___________________________。
已除尽,方法是___________________________。
(4)操作③的目的是__________,其相应的离子方程式为:____________________。
(5)说明此设计方案不严密之处____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组热化学方程式中,化学反应的ΔH前者大于后者的是( )
①C(s)+O2(g)===CO2(g); C(s)+![]() O2(g)===CO(g)
O2(g)===CO(g)
②S(s)+O2(g)===SO2(g); S(g)+O2(g)===SO2(g)
③H2(g)+![]() O2(g)===H2O(l); 2H2(g)+O2(g)===2H2O(l)
O2(g)===H2O(l); 2H2(g)+O2(g)===2H2O(l)
④2KOH(aq)+H2SO4(aq)===K2SO4(aq)+2H2O(l);2KOH(aq)+H2SO4(浓)===K2SO4(aq)+2H2O(l)
⑤NaOH(aq)+HCl (aq)===NaCl (aq)+H2O(l); NaOH(aq)+HF(aq)===NaF(aq)+H2O(l)
A. ①③⑤B. ②④⑤C. ②③④D. ①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工业废水含大量的FeSO4,较多的Cu2+和少量的K+。某工厂计划回收金属铜并制取硫酸亚铁,流程如下图,相关分析错误的是( )

A.步骤①加入过量Fe粉后过滤,分别得到固体A和滤液B
B.步骤②所加试剂是稀盐酸
C.蒸发结晶时有大量晶体析出就停止加热
D.取少量步骤①所得溶液B于试管中,先加入盐酸酸化,再加入BaCl2溶液,有白色沉淀生成,表明溶液B中含SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将10mL98%浓硫酸(密度为1.84g/mL)加水稀释至1L,然后向溶液中加入6.5g锌粒。
(1)稀释后硫酸溶液中H+的物质的量浓度是_________________?
(2)标出反应中电子转移方向及数目___________,并计算生成气体在标况下的体积是_____________?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一种节能的氯碱工业新工艺,将电解池与燃料电池相组合,相关流程如下图所示(电极未标出),下列说法错误的是:
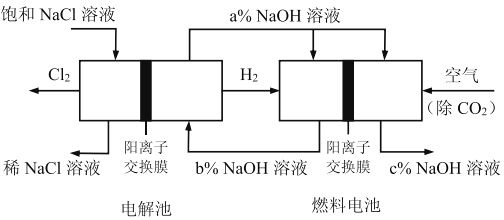
A. 电解池的阴极反应式2H2O+2e-=H2+2OH-
B. 相同条件下,当电解池生成2LCl2,理论上燃料电池应消耗1LO2
C. 电解池中阳离子移动流向阴极池
D. 溶液a、b、c的pH大小顺序为:a>b>c
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以铜银合金(含少量铁)废料为原料回收银和铜的工艺流程如下:

下列说法正确的是
A. 粗铜溶于过量稀硝酸,过滤、低温干燥得纯铜
B. 电解时用粗银作阴极,硝酸银溶液为电解质溶液
C. 用稀硫酸处理渣料时主要发生了氧化还原反应
D. 从滤液B中可以提取绿矾(FeSO4·7H2O)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com