
【题目】下图中A~J均代表无机物或其水溶液,其中B、D、G是单质,B是地壳中含量最高的金属元素,G是气体,J是磁性材料。
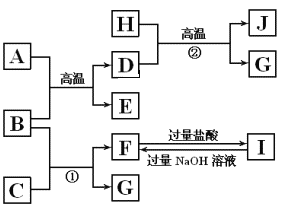
根据图示回答问题:
(1)写出下列物质的化学式:A ______,E______;
(2)反应①的化学方程式是_________________________ ;
反应②的化学方程式是___________________________ ;
(3)J与盐酸反应的化学方程式是______________________ ;
反应后的溶液与足量的D反应的离子方程式是______________________,如何检验最后溶液中的阳离子:______________________________________。
(4)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3与KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为________________________。
【答案】Fe2O3 Al2O3 2Al+NaOH+2H2O=2NaAlO2+3H2↑ 3Fe+4H2O![]() Fe3O4+3H2 Fe3O4+8HCl=FeCl2+FeCl3+4H2O 2Fe3++Fe=3Fe2+ 取少量溶液与试管中滴加硫氰化钾溶液,不变色,再通入氯气变血红色,证明含有二价铁离子 2Fe3+ +3ClO-+10OH- =2FeO42-+3Cl-+5H2O((或2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O)
Fe3O4+3H2 Fe3O4+8HCl=FeCl2+FeCl3+4H2O 2Fe3++Fe=3Fe2+ 取少量溶液与试管中滴加硫氰化钾溶液,不变色,再通入氯气变血红色,证明含有二价铁离子 2Fe3+ +3ClO-+10OH- =2FeO42-+3Cl-+5H2O((或2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O)
【解析】
此题为框图型推断题,解题的突破口有: B地壳中含量最高的金属,为Al;J为磁性材料,故为Fe3O4,②反应条件为高温,该反应为铁和水蒸气的反应G为氢气;B(Al)和C反应生成G(H2)和F,I加入过量NaOH得到F,故C为NaOH,F为NaAlO2,结合A和B的反应条件为高温,可知为铝热反应,D为Fe,E为Al2O3,据此解答。
(1)根据以上分析,A和B在高温下的反应为Al与Fe2O3在高温下发生的铝热反应,生成和Al2O3和Fe,故A的化学式为:Fe2O3,E的化学式为:Al2O3;
故答案为:Fe2O3;Al2O3;
(2) 根据以上分析,B为Al,C为氢氧化钠溶液,反应①是铝和氢氧化钠溶液反应生成偏铝酸钠和氢气,化学方程式是2Al+NaOH+2H2O=2NaAlO2+3H2↑;
反应②是铁在高温下和水蒸汽反应生成四氧化三铁和氢气,化学方程式是3Fe+4H2O![]() Fe3O4+3H2;
Fe3O4+3H2;
故答案为:2Al+NaOH+2H2O=2NaAlO2+3H2↑;3Fe+4H2O![]() Fe3O4+3H2;
Fe3O4+3H2;
(3)J为Fe3O4,Fe3O4与盐酸反应生成氯化铁、氯化亚铁和水,化学方程式是Fe3O4+8HCl=FeCl2+FeCl3+4H2O;反应后的溶液含有Fe3+与足量的Fe反应的离子方程式是2Fe3++Fe=3Fe2+,最后溶液中的阳离子主要是Fe2+,检验的方法是取少量溶液与试管中滴加硫氰化钾溶液,不变色,再通入氯气变血红色,证明含有二价铁离子。
故答案为:Fe3O4+8HCl=FeCl2+FeCl3+4H2O;2Fe3++Fe=3Fe2+;取少量溶液与试管中滴加硫氰化钾溶液,不变色,再通入氯气变血红色,证明含有二价铁离子;
(4)次氯酸钾中氯+1价具有强氧化性,可将+3价的铁氧化成+6价,用FeCl3与KClO在强碱性条件下反应制取K2FeO4,反应的离子方程式为:2Fe3+ +3ClO-+10OH- =2FeO42-+3Cl-+5H2O(或2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O),
故答案为:2Fe3+ +3ClO-+10OH- =2FeO42-+3Cl-+5H2O(或2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O)。


 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是( )
A. 相对分子质量相同、结构不同的化合物一定是互为同分异构体关系
B. 结构对称的烷烃,其一氯代物必定只有一种结构
C. 互为同分异构体的化合物不可能具有相同的结构简式
D. 通式为CnH2n且碳原子数不同的有机物一定互为同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】38.4gCu跟适量的浓HNO3反应,Cu全部反应后共收集到气体22.4L(标准状况),反应中作氧化剂的硝酸与总消耗的HNO3的物质的量比( )
A. 5∶11 B. 6∶11 C. 5∶6 D. 6∶5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法中正确的是( )
A. 常温常压下,2.24 L H2O中含有极性共价键的数目为0.2NA
B. 0.1 mol·L-1NH4Cl溶液中含有NH![]() 的数目小于0.1NA
的数目小于0.1NA
C. 100 mL 12 mol·L-1的浓HNO3与过量Cu反应转移电子的数目为0.6NA
D. 标准状况下,11.2 L由CH4和C2H4组成的混合气体中含有氢原子的数目为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知氨可以与灼热的氧化铜反应得到氮气和金属铜,用示意图中的装置可以实现该反应。

回答下列问题:
(1)A中加入的物质是_______,发生反应的化学方程式是________________________。
(2)B中加入的物质是____________,其作用是_________________。
(3)实验时在C中观察到得现象是_______,发生反应的化学方程式是________________。
(4)实验时在D中观察到得现象是____________________,D中收集到的物质是_____________,检验该物质的方法和现象是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知![]() 与足量的10mol/L硫酸液混合微热,产生下列现象:①有红色金属生成②产生刺激性气味的气体③溶液呈现蓝色。据此判断下列说法正确的是
与足量的10mol/L硫酸液混合微热,产生下列现象:①有红色金属生成②产生刺激性气味的气体③溶液呈现蓝色。据此判断下列说法正确的是
A. 反应中硫酸作氧化剂
B. ![]() 中硫元素被氧化
中硫元素被氧化
C. 刺激性气味的气体是氨气
D. 1mol![]() 完全反应转移0.5mol电子
完全反应转移0.5mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验原理或操作正确的是
A. 用20mL量筒量取15mL酒精,加水5mL,配制质量分数为75%酒精溶液
B. 在200mL某硫酸盐溶液中,含有1.5NA个硫酸根离子,同时含有NA个金属离子,则该硫酸盐的物质的量浓度为2.5mol·L1
C. 实验中需用2.0 mol·L1的Na2CO3溶液950mL,配制时应选用的容量瓶的规格和称取Na2CO3的质量分别为950mL、201.4g
D. 实验室配制500 mL 0.2 mol·L1的硫酸亚铁溶液,其操作是:用天平称15.2g绿矾(FeSO4·7H2O),放入小烧杯中加水溶解,转移到500 mL容量瓶,洗涤、稀释、定容、摇匀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应中通常伴随着能量变化,下列说法中错误的是
A.煤燃烧时将部分化学能转化为热能B.电解水时将部分化学能转化为电能
C.黑火药爆炸时将部分化学能转化为动能D.镁条燃烧时将部分化学能转化为光能
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com