
【题目】某蓄电池反应为NiO2+Fe+2H2O![]() Fe(OH)2+Ni(OH)2。
Fe(OH)2+Ni(OH)2。
(1)该蓄电池充电时,发生还原反应的物质是 (填下列字母),放电时生成Fe(OH)2的质量18 g,则外电路中转移的电子数是 。
A.NiO2 B.Fe C.Fe(OH)2 D.Ni(OH)2
(2)为防止远洋轮船的钢铁船体在海水中发生电化学腐蚀,通常把船体与浸在海水里的Zn块相连,或与该蓄电池这样的直流电源的 极(填“正”或“负”)相连。
(3)以该蓄电池做电源,用右图所示装置,在实验室模拟铝制品表面“钝化”处理的过程中,发现溶液逐渐变浑浊,原因是(用相关的电极反应式和离子方程式表示)。 。

(4)精炼铜时,粗铜应与直流电源的 极(填“正”或“负”)相连,精炼过程中,电解质溶液中c(Fe2+)、c(Zn2+)会逐渐增大而影响进一步电解,甲同学设计如下除杂方案:
![]()
已知:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Zn(OH)2 |
开始沉淀时的pH | 2.3 | 7.5 | 5.6 | 6.2 |
完全沉淀时的pH | 3.9 | 9.7 | 6.4 | 8.0 |
则加入H2O2的目的是 ,乙同学认为应将方案中的pH调节到8,你认为此观点 (填“正确”或“不正确”),理由是 。
【答案】(1)C 0.4NA 或2.408×1023(2)负
(3)Al=Al3++3e- Al3++3HCO3-=Al(OH)3↓+3CO2↑
(4)正 将Fe2+氧化为Fe3+ 不正确 因同时会使Cu2+生成沉淀而除去
【解析】
试题分析:(1)充电时Fe(OH)2得到电子,被还原,发生还原反应,变为Fe。内产生1mol的Fe(OH)2,转移电子2mol,现在产生Fe(OH)2的物质的量为18g÷90g/mol=0.2mol,所以转移电子的物质的量为0.4NA。(2)为防止轮船被腐蚀,应该把轮船的船体与外界电源的负极相连,这样轮船就不会失去电子,从而得到保护。(3)Al作阳极,发生反应:Al-3e-=Al3+;在溶液中发生反应:Al3++3HCO3-=Al(OH)3↓+3CO2↑。因此可看到溶液变浑浊同时冒气泡。(4)精炼铜时,粗铜应与直流电源的正极相连,精铜与直流电源的负极相连,粗铜在的Fe、Zn也逐渐被氧化变为Fe2+、Zn2+,加入H2O2可以把Fe2+氧化为Fe3+,调整溶液的PH至3.9,这时Fe3+完全为Fe(OH)3沉淀,而Cu2+仍然以离子的形式存在于溶液中。乙同学认为应将方案中的pH调节到8,你认为此观点不正确。这是因为PH=8时会使Cu2+生成沉淀而除去。


科目:高中化学 来源: 题型:
【题目】利用下图所示的有机物X可生产S-诱抗素Y。下列说法正确的是

A. 1 mol Y最多能和6 molH2发生加成反应
B. X可以发生氧化、取代、加聚、酯化等反应
C. Y可以与FeCl3溶液发生显色反应,又可使酸性高锰酸钾溶液退色
D. X结构中有2个手性碳原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,浓度均为1.0 mol·L-1的NH3·H2O和NH4Cl混合溶液10 mL,测得其pH为9.3。下列有关叙述正确的是( )
A. 加入适量的NaCl,可使c(NH![]() )=c(Cl-)
)=c(Cl-)
B. 滴加几滴浓氨水,c(NH![]() )减小
)减小
C. 滴加几滴浓盐酸,![]() 的值减小
的值减小
D. 1.0 mol·L-1的NH4Cl溶液中c(NH![]() )比该混合溶液中的大
)比该混合溶液中的大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的铁片和浓硫酸混合加热,充分应后得到溶液X,X中除Fe3+外还可能含有Fe2+.若要确认其中的Fe2+,应选用
A. KSCN溶液和氯水
B. 铁粉和KSCN溶液
C. 浓氨水
D. 酸性KMnO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,将两烧杯中电极用导线相连,四个电极分别为Mg、Al、Pt、C。当闭合开关S后,以下表述正确的是( )
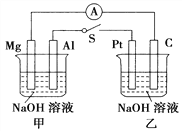
A. 电流表指针不发生偏转
B. Al、Pt两极有H2产生
C. 甲池pH减小,乙池pH不变
D. Mg、C两极生成的气体在一定条件下可以恰好完全反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】药物X、Y和高聚物Z,可以用烃A为主要原料,采用以下路线合成。
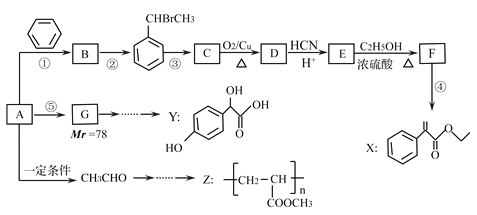
已知:Ⅰ.反应①、反应②的原子利用率均为100%.
Ⅱ.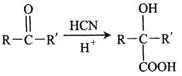 (R或R可以是烃基或氢原子)
(R或R可以是烃基或氢原子)
请回答下列问题:
(1)A的结构简式为____________。
(2)Z中的官能团名称为__________,反应③的条件为___________。
(3)关于药物Y(![]() )的说法正确的是______________。
)的说法正确的是______________。
A.1mol药物Y与足量的钠反应可以生成33.6L氢气。
B.药物Y的分子式为C8H8O4,能使酸性高锰酸钾溶液褪色
C.药物Y中⑥、⑦、⑧三个-OH的酸性由强到弱的顺序是⑧>⑥>⑦
D.1mol药物Y与H2、浓溴水中的Br2反应,最多消耗H2、Br2分别为4mol和2mol
(4)写出反应E→F的化学方程式_________________,F→X的化学方程式______________________。
(5)写出符合下列条件的E的一种同分异构体的结构简式____________。
①遇FeCl3溶液可以发生显色反应,且是苯的对位二元取代物;②能发生银镜反应和水解反应;③核磁共振氢谱有6个峰。
(6)参考上述流程以CH3CHO和CH3OH为起始原料,其它无机试剂任选,设计合成Z的线路。_________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在含有弱电解质的溶液中,往往有多个化学平衡共存。
(1)一定温度下,向1L 0.l mol/L-1 CH3 COOH溶液中加入0.1molCH3COONa固体,溶液中
[c(CH3COO-)·c(H+)]/c(CH3COOH) (填“增大”、“减小”或“不变”);写出表示该混合溶液中所有离子浓度之间的一个等式 。
(2)土壤的pH一般在4-9之间。土壤中Na2CO3含量较高,pH可以高达10.5,试用离子方程式解释土壤呈碱性的原因 ,加入石膏(CaSO4 2H2O)可以使土壤碱性降低,有关反应的化学方程式为
(3)常温下在20ml 0.1mo l·L-1 Na2CO3溶液中逐滴加入0.1mol·L-1 HC1溶液40mL,溶液中含碳元素的各种微粒(CO2)因逸出未画出)物质的量分数随溶液pH变化的情况如图所示。
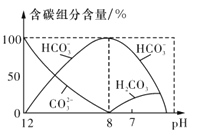
回答下列问题:
①在同一溶液中,H2CO3、HCO3-、CO32- (填“能”或“不能”)大量共存;
②当pH=7时,溶液中含碳元素的主要微粒为 ,溶液中各种离子的物质的量浓度的大小关系
为 ;
③已知在25℃时,CO32-水解反应的平衡常数即水解常数Kh=2×10-4mol·L-1,当溶液中c(HCO3-):c(CO32-)=2:1时,溶液的pH= ;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍氢电池已经成为混合动力汽车的主要电池类型。该电池放电时的总反应为:NiOOH + MH==Ni(OH)2 + M,其中M表示储氢合金,MH表示吸附了氢原子的储氢合金,下列说法正确的是
A. 放电时负极反应为:MH+OH--e-==M+H2O
B. 放电时,每转移1mol电子,有1mol NiOOH被氧化
C. 充电时正极反应为:NiOOH+H2O+e-==Ni(OH)2+OH-
D. 电池电解液可用KOH溶液,充电过程中KOH浓度减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水提溴和海带提碘都需要经过浓缩、氧化、提取三个步骤。有关叙述错误的是
A. 提溴的浓缩液来自于海水晒盐后的卤水 B. 氧化步骤都可以通入氯气来实现
C. 提取溴时利用溴的挥发性 D. 提取碘时利用碘的升华特性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com