
����Ŀ��ú��������úΪԭ�ϣ�������ѧ�ӹ�ʹúת��Ϊ���塢Һ�塢����ȼ���Լ����ֻ�����Ʒ�Ĺ�ҵ���̡�
I����ˮ����ͨ�����ȵ�̿���ɲ���ˮú������ӦΪ��C(s)��H2O(g)![]() CO(g)��H2(g)
CO(g)��H2(g)
��1����ʹ��ѧ��Ӧ���ʼӿ�Ĵ�ʩ��________(�����)��
�����߷�Ӧ�¶�������C�����ʵ������ܱն��������г���CO(g)
II����ҵ����CO����ȼ�ϼ״���һ�������·�����ӦCO��g��+2H2��g��![]() CH3OH��g����
CH3OH��g����
ͼ1 ͼ2
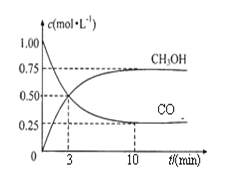
��2��ͼ1�DZ�ʾһ���¶��£������Ϊ2L���ܱ������м���4molH2��һ������CO��CO��CH3OH��g����Ũ����ʱ��仯������ӷ�Ӧ��ʼ��ƽ�⣬��H2Ũ�ȱ仯��ʾƽ����Ӧ����v��H2��=__________________��
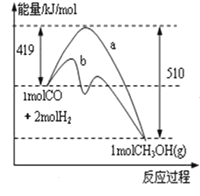
��3��ͼ2��ʾ�÷�Ӧ���й����������ı仯������a��ʾ��ʹ�ô���ʱ��Ӧ�������仯������b��ʾʹ�ô�����������仯������ͼ����ʹ����ӿ컯ѧ��Ӧ���ʵ�ԭ��_______________________________���÷�Ӧ����1molCOʱ��______�������ų���������������__________KJ������
���𰸡��٢� 0.15molL��1min��1 �����뷴Ӧ������γ��м�̬�������˷�Ӧ��� �ų� 91
��������
��1����Ӱ�췴Ӧ���ʵ����ط�����
��2������v=��c/��t���м��㣻
��3�������ӿ컯ѧ��Ӧ���ʵ�ԭ���Ǵ����뷴Ӧ������γ��м�̬�������˷�Ӧ��ܣ����÷�Ӧǰ�����������������Ӧ�������仯��
��1��C(s)��H2O(g)![]() CO(g)��H2(g)
CO(g)��H2(g)
�����߷�Ӧ�¶ȣ����������Ӱٷ�������Ӧ�������ʢ���ȷ��
��CΪ���壬����C�����ʵ�������Ӧ���Ũ�Ȳ��䣬��Ӧ���ʲ��䣬�ʢڴ���
���ܱն��������г���CO(g)������Ũ����������Ӧ��Ũ�ȣ���Ӧ�������ʢ���ȷ��
�ʴ�Ϊ���٢ۡ�
��2����ͼ1��֪��COŨ�ȱ仯��Ϊ1.00mol/L-0.25mol/L=0.75mol/L����t=10min����v��CO��=0.75mol/L��10min=0.075mol/��L��min��������CO��g��+2H2��g��![]() CH3OH��g������ѧ��Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ���v��H2��=2v��CO��=2��0.075mol/��L��min��=0.15 mol/��L��min�����ʴ�Ϊ��0.15 mol/��L��min����
CH3OH��g������ѧ��Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ���v��H2��=2v��CO��=2��0.075mol/��L��min��=0.15 mol/��L��min�����ʴ�Ϊ��0.15 mol/��L��min����
��3�������ӿ컯ѧ��Ӧ���ʵ�ԭ���Ǵ����뷴Ӧ������γ��м�̬�������˷�Ӧ��ܣ���ͼ2��֪���÷�Ӧ�з�Ӧ�����������������������������ʸ÷�ӦΪ���ȷ�Ӧ����Ӧ��Ϊ1molCO��g����2molH2��g����������Ϊ1molCH3OH��g������H=419kJ/mol-510kJ/mol=-91kJ/mol�����Ե���Ӧ����1molCOʱ���ų�91kJ���������ʴ�Ϊ�������뷴Ӧ������γ��м�̬�������˷�Ӧ��ܣ��ų���91��


 ÿ��10���ӿ�����������������ϵ�д�
ÿ��10���ӿ�����������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڽ����˵����ȷ����
A. ��Al(OH)3�����м���NaOH��Һ���������г�������
B. ���ڽ�����磬�ڵ糡�������¿����ڷ�ɢ�����������˶�
C. ���������ķ�����ȥ������Һ�е�NaCl
D. �Ʊ�Fe(OH)3����ʱ��Ҫ������FeCl3��Һ��NaOH��Һ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
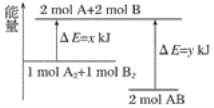
����Ŀ����ѧ��ӦA2��B2===2AB�������仯��ͼ��ʾ��������˵����ȷ���ǣ� ��
A. �÷�Ӧ�����������ķ�Ӧ
B. 1molA��A����1molB��B�������ܷų�xkJ������
C. 2molA��B��������Ҫ����ykJ������
D. 2molAB������������1molA2��1molB2��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶��£���Ӧ2N2O5![]() 4NO2+O2��ʼʱc(N2O5)=0.0408mol��L-1����1 min����c(N2O5)=0.030mol��L-1����÷�Ӧ�ķ�Ӧ����Ϊ
4NO2+O2��ʼʱc(N2O5)=0.0408mol��L-1����1 min����c(N2O5)=0.030mol��L-1����÷�Ӧ�ķ�Ӧ����Ϊ
A. v(N2O5)=1.08��10-4 molL-1s-1 B. v(N2O5)= 1.8��10-1 molL-1min
C. v(O2)=9.0��10-5 molL-1s-1 D. 2 v(NO2)= v(N2O5)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������к��е����ʣ�������Ϊ���ʣ��������ü��ȵķ�����ȥ���ǣ� ��
A.CaCO3��CaO��B.Cu��CuO��
C.Na2CO3��NaHCO3��D.NaHCO3��Na2CO3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���F��һ�����ϣ���ϳ�·����ͼ��ʾ��
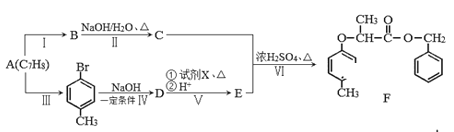
��֪��i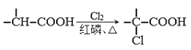
ii
(1)D������Ϊ__________���Լ�X�Ľṹ��ʽΪ___________��������ķ�Ӧ����Ϊ_________��
(2)�����Ӧ�Ļ�ѧ����ʽΪ__________________________________��
(3)��������������(�ٱ�����ֻ������ȡ������������FeCl3��Һ������ɫ��Ӧ�����ܷ���ˮ�ⷴӦ��������Ӧ)��E��ͬ���칹����_______�֣����к˴Ź������������Ϊ6�U2�U2�U1�U1�ķ��ӵĽṹ��ʽΪ___________________________��
(4)����������Ϣ�������![]() Ϊԭ����ȡ
Ϊԭ����ȡ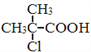 �ĺϳ�·��ͼ_________��(���Լ�һ��Ҫѡ������Һ���������Լ���ѡ)�ϳ�·��ͼʾ�����£�
�ĺϳ�·��ͼ_________��(���Լ�һ��Ҫѡ������Һ���������Լ���ѡ)�ϳ�·��ͼʾ�����£�![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʽΪC4H10O����������Ʒ�Ӧ�ų��������л�����
A. 4�� B. 5�� C. 6�� D. 7��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��пƬ��ͭƬ��ϡ����������ɵ�ԭ���װ�ã�c��d Ϊ�����缫�������йص��жϲ���ȷ��

A. c Ϊ����������������Ӧ
B. ��ع����Ĺ����У�d �缫�ϲ�������
C. ��ع���ʱ����Һ�� SO42���� d �ƶ�
D. ��ع����Ĺ����У���Һ�� SO42��Ũ�Ȼ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ȫ�ӳɺ�����������2��2��3-�������������
A. (CH3)3 C��CH=CH2B. CH2=C(CH2CH3)C (CH3)3
C. HC��CCH(CH3)C(CH3)3D. (CH3)3CC(CH3)=CHCH3
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com