
【题目】在某温度下,NaOH的溶解度为20g,该温度下将80gNaOH投入220g水中,充分搅拌后,静置,测得溶液的密度为1.2g/mL,则该溶液中溶质的物质的量浓度为( )
A. 5.0 mol/L B. 2.0 mol/L C. 0.02mol/L D. 7.5 mol/L
 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案科目:高中化学 来源: 题型:
【题目】“不务正业”的诺贝尔化学奖2017年颁发给三位生物物理科学家,因为他们在开发冷冻电镜的过程中贡献卓越,让我们可以看清生物大分子的模样。可见图像是理解的基础。而在化学学习中,也可以将某些化学知识用图像表示,可以收到直观、简明的效果。下列图象所表示的化学知识中,明显不正确的是
A. 向NaOH溶液中通入CO2
B. 向FeCl3溶液中加入锌粉
C. 向碳酸钠溶液中逐滴加入盐酸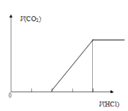
D. 向偏铝酸钠溶液中逐滴加入盐酸溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机玻璃(PMMA)广泛应用于生活。以石油化工产品A为主要原料合成PMMA的一种工艺流程如下(部分产物和条件省略):

(1)B的化学名称为________________。
(2)E的结构简式为________,其核磁共振氢谱显示为________组峰,峰面积之比为________。
(3)由E生成G的反应类型为__________。G中官能团名称为__________。
(4)写出A生成B的化学方程式:_________________________________________________。
(5)T是G的同分异构体,1molT与足量银氨溶液反应最多生成4molAg。T的结构有________种(不含立体结构)。
(6)参照上述流程,以![]() 为原料(其他原料自选),设计合成
为原料(其他原料自选),设计合成![]() 的路线:_______。
的路线:_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上制备相关物质,涉及的反应原理及部分流程较为合理的是
A. 制取镁:海水![]() Mg(OH)2
Mg(OH)2![]() MgO
MgO![]() Mg
Mg
B. 冶炼铝:铝土矿![]() NaAlO2
NaAlO2![]() 无水AlCl3
无水AlCl3![]() Al
Al
C. 制硝酸:N2、H2 ![]() NH3
NH3![]() NO
NO![]() 50%HNO3
50%HNO3 ![]() 浓HNO3
浓HNO3
D. 海带![]() 海带灰
海带灰![]()
![]() I2(aq)
I2(aq)![]() I2
I2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)现有下列4种物质:① NO、②浓H2SO4、③ NaHCO3、④SO2其中,遇空气变红棕色的是______(填序号,下同);能使蔗糖变黑的是______;能使品红溶液褪色的是_________。受热分解产生CO2的是______,写出该反应化学方程式_____________________;
(2)青海昆仑玉被定为十年前北京奥运会奖牌用玉,昆仑玉主要成分是由"透闪石"和"阳起石”组成的纤维状微晶结合体,透闪石(Tremolite)的化学成分为Ca2Mg5Si8O22(OH)2透闪石的化学式写成氧化物的形式为:________________________________;
(3)400 mL某浓度的NaOH溶液与5.6 L Cl2(标准状况)恰好完全反应,计算:生成的NaClO的物质的量_____________;该溶液中NaOH的物质的量浓度__________________;
(4)向1L,1mol/L的氯化铝溶液中加入含氢氧化钠xmol的氢氧化钠溶液,当铝元素以Al(OH)3和AlO2-形式存在时x的取值范围是_________________,当x=3.6时,Al(OH)3的质量为__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列反应的热化学方程式为:
①C(s)+O2(g)=CO2(g)△H1=﹣393.5kJ/mol
②CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l)△H2=﹣870.3kJ/mol
③H2(g)+ ![]() O2(g)=H2O(l)△H3=﹣285.8kJ/mol
O2(g)=H2O(l)△H3=﹣285.8kJ/mol
则反应2C(s)+2H2(g)+O2(g)=CH3COOH(l) 的反应热(焓变)为( )
A.+488.3kJ/mol
B.﹣488.3kJ/mol
C.﹣244.15kJ/mol
D.+244.15kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)向某NaOH溶液中投入一块Al箔,先无明显现象,随后逐渐产生气泡,则产生气泡的离子反应方程式为______。
(2)实验室常用还原性Fe粉与水蒸气反应的实验来研究Fe的还原性,则该反应的化学反应方程式为______
(3)Fe(OH)2制备时,采用的方法是“长滴管、液面下”的实验操作,但在实验时,由于操作不当,依旧会出现白色沉淀、灰绿色沉淀直至最终变为红褐色沉淀,写出白色沉淀最终转化为红褐色沉淀的化学反应方程式为______
(4)实验时制备Al(OH)3时,常用可溶性铝盐(如Al2(SO4)3与氨水反应进行制备。某课外小组在实验时不慎向Al2(SO4)3溶液中加入了过量NaOH溶液,最终并没有制出白色沉淀Al(OH)3,则该小组同学实验时发生的总离子反应方程式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于纯净物、混合物、强电解质、弱电解质和非电解质的正确组合是( )
纯净物 | 混合物 | 强电解质 | 弱电解质 | 非电解质 | |
A | 盐酸 | 醋酸 | 碳酸 | 氨水 | 氯水 |
B | 纯碱 | 碘酒 | 苛性钾 | 冰醋酸 | 干冰 |
C | 石油 | 石灰石 | 硫酸 | 磷酸 | 水 |
D | 烧碱 | 天然气 | 氯化钠 | 碳酸钠 | 蔗糖 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室有一瓶混有氯化钠的氢氧化钠固体试剂,经测定NaOH的质量分数约为82.0%,为了验证其纯度,用浓度为0.2mol/L的盐酸进行滴定,试回答:
(1)托盘天平称量5.0g固体试剂,用蒸馏水溶解于烧杯中,并振荡,然后立即直接转入500mL容量瓶中,恰好至刻度线,配成待测液备用.请改正以上操作中出现的五处错误.① , ② , ③ , ④ , ⑤ .
(2)将标准盐酸装在25.00mL滴定管中,调节液面位置在处,并记下刻度.
(3)取20.00mL待测液,待测定.该项实验操作的主要仪器有 . 用试剂作指示剂时,滴定到溶液颜色由刚好至色时为止.
(4)滴定达终点后,记下盐酸用去20.00mL,计算NaOH的质量分数为 .
(5)试分析滴定偏低误差可能由下列哪些实验操作引起的 .
A.转移待测液至容量瓶时,未洗涤烧杯
B.酸式滴定管用蒸馏水洗涤后,直接装盐酸
C.滴定时,反应容器摇动太激烈,有少量液体溅出
D.滴定到终点时,滴定管尖嘴悬有液滴
E.读数(滴定管)开始时仰视,终点时俯视.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com