
【题目】下列说法正确的是( )
A.依据丁达尔现象可将分散系分为溶液、胶体与浊液
B.用饱和食盐水替代水跟电石反应,可以减缓乙炔的产生速率
C.制备乙酸乙酯时可用热的NaOH溶液收集产物以除去其中的乙酸
D.实验室从海带提取单质碘的方法是:取样![]() 灼烧
灼烧![]() 溶解
溶解![]() 过滤
过滤![]() 萃取
萃取
科目:高中化学 来源: 题型:
【题目】下列实验方法或实验操作不正确的是( )
A.除去乙酸乙酯中的少量乙酸:加入NaOH溶液,充分振荡后分液
B.区别地沟油与矿物油:加入足量NaOH溶液共热,不分层的是地沟油
C.使淀粉水解:先在淀粉中加入20%的硫酸溶液,然后在沸水浴中加热
D.洗去试管上的油污:先用热的纯碱溶液浸泡试管,然后再用清水洗涤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于某酸的酸式盐NaHY的水溶液的下列叙述中,正确的是
A. 该酸式盐的水溶液一定显酸性
B. 在该盐溶液中,离子浓度为:c(Na+)>c(Y2-)>c(HY-)>c(OH-)>c(H+)
C. 若HY-能水解,水解方程式为:HY-+H2O![]() Y2-+H3O+
Y2-+H3O+
D. 若HY-能电离,电离方程式为:HY-+H2O![]() Y2-+H3O+
Y2-+H3O+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家以MoS2为催化剂,在不同电解质溶液中实现常温电催化合成氨,其反应历程与相对能量模拟计算结果如图。下列说法错误的是( )

A. Li2SO4溶液利于MoS2对N2的活化
B. 两种电解质溶液环境下从N2→NH3的焓变不同
C. MoS2(Li2SO4溶液)将反应决速步(*N2→*N2H)的能量降低
D. N2的活化是N≡N键的断裂与N—H键形成的过程
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】南京工业大学某研究团队最近在《Nature Communications》刊文介绍了他们开发的一种新型催化剂——反钙钛矿基非贵金属催化剂,这种价廉的新型催化剂结合了钙钛矿结构的灵活性和过渡金属氮(碳)化合物的高导电性、优异电催化性等优点,理论上来说是一种很有发展潜力的析氧反应电催化剂。回答下列问题:
(1)基态氮原子核外未成对电子数为________,基态碳原子核外电子云有_______个伸展方向。
(2)在周期表中,N、O、F是位于同周期且相邻的三种元素,第一电离能最大的元素和最小的元素组成一种只含极性键的化合物M,M分子的立体构型是_________,中心原子的杂化类型是________。
(3)在周期表中,钡位于第六周期ⅡA族,钛酸钡、钛酸钙的熔点分别为1625℃、1975℃,二者熔点差异的原因为__。
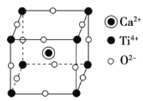
(4)钛酸钙的晶胞如图所示,钛酸钙的化学式为_____________;1个钛离子与________个氧离子等距离且最近,这些氧离子可构成正八面体,钛离子位于该正八面体的体心。已知钛酸钙的晶胞参数为a nm,则该正八面体的边长为________pm。
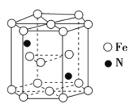
(5)Fe和N可组成一种过渡金属氮化物,其晶胞如图所示,六棱柱底边边长为x cm,高为y cm,NA为阿伏加德罗常数的值,则晶胞的密度为________________g·cm-3(列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知pC=-lgc(B),室温下,某二元酸(H2A)中部分微粒的pC值随溶液pH值变化关系如图所示。下列说法错误的是( )

A.曲线a表示的微粒是H+
B.溶液中水的电离程度:m>n
C.pH=8时,溶液中,c(HA-)>c(H2A)
D.pH=1与pH=3时,H2A的浓度几乎相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人们对苯的认识有一个不断深化的过程。已知分子式为![]() 的甲、乙两种物质的结构简式如图所示。
的甲、乙两种物质的结构简式如图所示。

(1)甲、乙的化学性质的区别为甲能___________________(填字母,下同),而乙能___________________。
A.被酸性![]() 溶液氧化
溶液氧化
B.与溴水发生加成反应
C.与氢气发生加成反应
(2)![]() 甲和
甲和![]() 乙分别与
乙分别与![]() 发生完全加成反应,甲消耗___________
发生完全加成反应,甲消耗___________![]()
![]() ,而乙消耗__________
,而乙消耗__________![]()
![]()
(3)![]() 还可能有另一种结构丙(如图所示),其二氯代物有___________________种。
还可能有另一种结构丙(如图所示),其二氯代物有___________________种。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钙是一种白色固体,微溶于冷水,不溶于乙醇,化学性质与过氧化钠类似。某学习小组设计在碱性环境中利用CaCl2与H2O2反应制取CaO2·8H2O,装置如图所示:
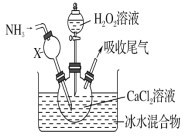
(1)小组同学查阅文献得知:该实验用质量分数为20%的H2O2溶液最为适宜。市售H2O2溶液的质量分数为30%。该小组同学用市售H2O2溶液配制约20%的H2O2溶液的过程中,使用的玻璃仪器除玻璃棒、胶头滴管外,还有_____________。
(2)在冰水浴中进行的原因是_____________________。
(3)实验时,在三颈烧瓶中析出CaO2·8H2O晶体,总反应的离子方程式为________________________。
(4)若CaCl2原料中含有Fe3+杂质,Fe3+催化分解H2O2,会使H2O2的利用率明显降低。反应的机理为:
① Fe3+ + H2O2 = Fe2+ + H+ + HOO·
② H2O2 + X = Y + Z + W(已配平)
③ Fe2+ +·OH = Fe3+ + OH-
④ H+ + OH- = H2O
根据上述机理推导步骤②中的化学方程式为___________________________。
(5)过氧化钙可用于长途运输鱼苗,这体现了过氧化钙具有_____________的性质。
A.与水缓慢反应供氧 B.能吸收鱼苗呼出的CO2气体
C.能使水体酸性增强 D.具有强氧化性,可杀菌灭藻
(6)将所得CaO2·8H2O晶体加热到150~160℃,完全脱水后得到过氧化钙样品。该小组测定过氧化钙样品中CaO2的纯度的方法是:准确称取0.4000g过氧化钙样品,400℃以上加热至完全分解成CaO和O2(设杂质不产生气体),得到33.60mL(已换算为标准状况)气体。则:所得过氧化钙样品中CaO2的纯度为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示。下列叙述正确的是
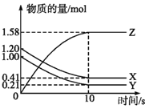
A.反应开始到10 s末时,用Z表示的反应速率为0.158 mol·L-1·s-1
B.反应开始到10 s末时,X的物质的量浓度减少了0.79 mol·L-1
C.反应开始到10 s时,Y的转化率为79.0%
D.反应的化学方程式为X(g)+Y(g)![]() Z(g)
Z(g)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com