
有4种钠的化合物W、X、Y、Z,它们之间存在如下关系:
①W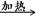 X+H2O+CO2↑
X+H2O+CO2↑
②Z+CO2―→X+O2
③Z+H2O―→Y+O2↑
④X+Ca(OH)2―→Y+CaCO3↓
试回答下列问题:
(1)W、X、Y、Z的化学式分别是:W:________、X:________、Y:________、Z:________。
(2)以上4个化学反应,属于氧化还原反应的是________(填反应序号),反应中氧化剂是________(写化学式),还原剂是________(写化学式)。
(3)若④反应在溶液中进行,写出其离子方程式以及能用该离子方程式表示的另一个化学反应的化学方程式:①离子方程式:__________________________。②化学方程式:_______________________。
(1)NaHCO3 Na2CO3 NaOH Na2O2
(2)②③ Na2O2 Na2O2 (3)Ca2++CO32-=CaCO3↓
Ca(OH)2+K2CO3=2KOH+CaCO3↓(其他合理答案也给分)
解析试题分析:W X+H2O+CO2↑,则W是碳酸氢钠,X是碳酸钠;Z+CO2―→X+O2,则Z是过氧化钠;Z+H2O―→Y+O2↑,则Y是氢氧化钠。
X+H2O+CO2↑,则W是碳酸氢钠,X是碳酸钠;Z+CO2―→X+O2,则Z是过氧化钠;Z+H2O―→Y+O2↑,则Y是氢氧化钠。
(1)W、X、Y、Z的化学式分别是NaHCO3、Na2CO3、NaOH、Na2O2。
(2)凡是有元素化合价升降的反应均是氧化还原反应,据此可知②Na2O2+CO2―→Na2CO3+O2、③Na2O2+H2O―→NaOH+O2↑氧元素的化合价发生变化,属于氧化还原反应,即答案选②③;其中均是过氧化钠中的氧元素发变化,即氧元素化合价部分从-1价升高到0价,部分降低到-2价,属于过氧化钠既是氧化剂,也是还原剂。
(3)碳酸钠和氢氧化钙反应的离子方程式为Ca2++CO32-=CaCO3↓;可溶性碳酸盐也能和氢氧化钙反应生成碳酸钙白色沉淀,例如Ca(OH)2+K2CO3=2KOH+CaCO3↓。
考点:考查钠化合物转化、氧化还原反应的有关判断以及方程式的书写


科目:高中化学 来源: 题型:填空题
无色透明溶液中可能含有下列离子:K+、Al3+、Fe3+、Ba2+、NO3—、SO42—、HCO32—、Cl-,取该溶液进行如下实验:
①用蓝色石蕊试纸检测该溶液,试纸显红色;
②取原溶液少许,加入铜片和稀硫酸共热,产生无色气体,该气体遇空气立即变为红棕色;
③取原溶液少许,加入氨水有白色沉淀生成,继续加入过量氨水,沉淀不消失;
④取原溶液少许,滴入氯化钡溶液产生白色沉淀;
⑤取实验④后的澄清溶液,滴入硝酸银溶液产生白色沉淀,再加入过量的稀硝酸,沉淀不消失。
请回答下列问题:
(1)根据上述实验判断原溶液中上述离子肯定存在的是 ,肯定不存在的是 。
(2)写出与②③两个实验有关的离子方程式:
② , ③ 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
有以下物质:①液氨;②氨水;③盐酸;④醋酸;⑤硫酸钡;⑥银;⑦氯化钠晶体;⑧二氧化碳;⑨醋酸铵;⑩酒精溶液。
(1)属于电解质的是_____________________________________________________________;
(2)能导电的是_________________________________________________________________;
(3)属于强电解质的是___________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
近年来,太湖蓝藻爆发,造成无锡市水质的严重恶化。这些事件再次敲响了我国水危机的警钟。在太湖流域某化工厂排放的污水中,常溶有某些对人体有害的物质,初步认为可能含有Fe3+、Ba2+、K+、OH-、Cl-、 、
、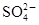 。为了进一步确认,取样进行实验检测:
。为了进一步确认,取样进行实验检测:
①取污水仔细观察,呈无色、透明、均一状态。
②向取样的污水中,滴入稀硫酸,有大量白色沉淀产生,再加稀硝酸,白色沉淀不消失。
③用pH试纸测定污水的pH,试纸显深蓝色。
(1)由此可知,该污水中肯定含有的离子是___________,肯定没有的离子是___________,可能含有的离子是___________。
(2)如何通过实验进一步确定溶液中可能存在的离子__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
离子反应是中学化学中重要的反应类型。回答下列问题:
(1)在发生离子反应的反应物或生成物中,一定存在________ (填序号)。
①单质 ②氧化物 ③电解质 ④盐 ⑤化合物
(2)现有铜、氯化铁溶液、盐酸、硝酸银溶液、氧化铝、二氧化碳、氧气七种物质,两两能发生反应的反应中,属于离子反应的有 种,属于置换反应的有 种。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
写出下列反应的离子反应方程式(全对得10分,有错即为0分)
(1)NaAlO2溶液中加入少量的盐酸
(2)AlCl3溶液中加入过量的NaOH
(3)Al2O3与NaOH水溶液的反应
(4)Fe3O4溶解在稀盐酸中
(5)FeCl2溶液中加入酸化的H2O2溶液
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
某溶液中的溶质由下列中的几种离子构成:Na+、Fe3+、Cu2+、Ba2+、AlO2—、CO32—、SO32—、SO42—。取该溶液进行有关实验,实验步骤及结果如下:
①向溶液中加入过量稀盐酸,得到气体甲和溶液甲;
②向溶液甲中加入过量NH4HCO3溶液,得到白色沉淀乙、气体乙和溶液乙;
③向溶液乙中加入过量Ba(OH) 2溶液,得到白色沉淀丙、气体丙和溶液丙。
④检验气体甲、气体乙、气体丙,都只含有一种成份,而且各不相同。
请回答下列问题:
(1)只根据实验①能得出的结论是 (3分)
(2)沉淀丙中一定含有 (1分),可能含有 (1分)
(3)该溶液中肯定存在的离子有
(4)气体乙分子的结构式为
(5)向溶液甲中加入NH4HCO3溶液至过量,该过程中可能发生反应的离子方程式为 ; ; (根据需要,可不填完,也可补充)
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
I、NaOH、FeCl3是中学化学实验室常用的试剂。
(1)在一定条件下能与NaOH溶液反应的固体单质有________和________(举两例)。
配制一定物质的量浓度的NaOH溶液时,造成实验结果偏低的原因是________。
| A.容量瓶中原有少量蒸馏水 |
| B.洗涤烧杯和玻璃棒的溶液未转入容量瓶中; |
| C.定容时观察液面俯视 |
| D.溶解后未经冷却立即转移至容量瓶内 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
现有含NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂将其转化为相应的沉淀或固体,从而实现Cl-、SO42-、和NO3-的相互分离。相应的实验过程可用下图表示: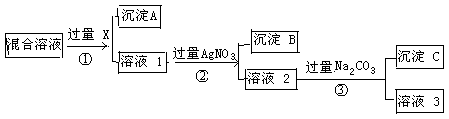
请回答下列问题:⑴写出实验流程中下列物质的化学式
试剂X : 沉淀A:
⑵上述实验流程中加入过量的Na2CO3的目的是 。
⑶按此实验方案得到的溶液3中肯定含有 (填化学式)杂质。
(4)请写出①②中反应的离子方程式①
②
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com