
写出下列反应的离子反应方程式(全对得10分,有错即为0分)
(1)NaAlO2溶液中加入少量的盐酸
(2)AlCl3溶液中加入过量的NaOH
(3)Al2O3与NaOH水溶液的反应
(4)Fe3O4溶解在稀盐酸中
(5)FeCl2溶液中加入酸化的H2O2溶液
(1)AlO2— +H++ H2O = Al(OH)3↓
(2)Al3++4 OH— = AlO2— +2 H2O
(3)Al2O3+2 OH—=" 2" AlO2— + H2O
(4)Fe3O4+8 H+ = Fe2++2 Fe3++4 H2O
(5)2 Fe2++2 H++H2O2 ="2" Fe3++ 2 H2O
解析试题分析:(1)NaAlO2溶液中加入少量的盐酸:AlO2— +H++ H2O = Al(OH)3↓;(2)AlCl3溶液中加入过量的:NaOHAl3++4 OH— = AlO2— +2 H2O ;(3)Al2O3与NaOH水溶液的反应:Al2O3+2 OH—=" 2" AlO2— + H2O;(4)Fe3O4溶解在稀盐酸中:Fe3O4+8 H+ = Fe2++2 Fe3++4 H2O;(5)FeCl2溶液中加入酸化的H2O2溶液:2 Fe2++2 H++H2O2 ="2" Fe3++ 2 H2O。
考点:离子反应方程式的书写


科目:高中化学 来源: 题型:填空题
常见的五种盐A、B、C、D、E,它们的阳离子可能是Na+、NH4+、Cu2+、Ba2+、Al3+、Ag+、Fe3+,阴离子可能是Cl-、NO3-、SO42-、CO32-,已知:
①五种盐均溶于水,水溶液均为无色。
②D的焰色反应呈黄色。
③A的溶液呈中性,B、C、E的溶液呈酸性,D的溶液呈碱性。
④若在这五种盐的溶液中分别加入Ba(NO3)2溶液,只有A、C的溶液不产生沉淀。
⑤若在这五种盐的溶液中,分别加入氨水,E和C的溶液中生成沉淀,继续加氨水,C中沉淀消失。
⑥把A的溶液分别加入到B、C、E的溶液中,均能生成不溶于稀硝酸的沉淀。
请回答下列问题:
(1)五种盐中,一定没有的阳离子是____________;所含阴离子相同的两种盐的化学式是__________________。
(2)D的化学式为__________________,D溶液显碱性的原因是_________________(用离子方程式表示)。
(3)A和C的溶液反应的离子方程式是______________________________________;
E和氨水反应的离子方程式是____________________________________________。
(4)若要检验B中所含的阳离子,正确的实验方法是______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
现有下列物质:①铜②蔗糖③CuO④NaHSO4 ⑤Ba(OH)2⑥氧气⑦盐酸⑧干冰⑨胆矾⑩水
(1)上述物质分类中不属于电解质的有 (填序号),④在水溶液中的电离方程式为 。
(2)碳酸钠俗名纯碱或苏打,在外观上与食盐相似。在一定条件下,上述物质中能用来区分碳酸钠与食盐的物质有 (填序号)。
(3)上述物质中有两种物质在水溶液中发生反应,其离子方程式为:H++OH-=H2O,则该反应的化学方程式为 。
(4)向④ 溶液中缓缓滴加⑤ 溶液至混合溶液刚好呈中性时的离子方程式为:_______。
(5)上述物质中有四种物质在一定条件下相互作用可生成一种新物质—碱式碳酸铜[Cu2(OH)2 CO3],请写出该反应的化学反应方程式________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
全球海水中溴的藏量丰富,约占地球溴总藏量的99%,故溴有“海洋元素”之称,海水中溴含量为65mg/L。其工业提取方法有:
(1)空气吹出纯碱吸收法。方法是将氯气通入到富含溴离子的海水中,使溴置换出来,再用空气将溴吹出,用纯碱溶液吸收,最后用硫酸酸化,即可得到溴单质。该方法涉及到的反应有:①
(写出离子方程式);②Br2+3CO32—=BrO3—+ 5Br—+3CO2↑;③BrO3—+ 5Br—+6H+=3Br2+3H2O。其中反应②中氧化剂是 ;还原剂是 。
(2)空气吹出SO2吸收法。该方法基本同(1),只是将溴吹出后是用SO2来吸收的,使溴转化为氢溴酸,
然后再用氯气氧化氢溴酸即得单质溴。写出溴与二氧化硫的离子反应方程式:_ 。
(3)溶剂萃取法。该法是利用单质溴在水中和溶剂中溶解度的不同的原理来进行的。实验室中萃取用到的实验仪器名称是 。下列可以用于海水中溴的萃取试剂的 。
①乙醇 ②四氯化碳 ③硝酸 ④裂化汽油
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
有4种钠的化合物W、X、Y、Z,它们之间存在如下关系:
①W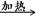 X+H2O+CO2↑
X+H2O+CO2↑
②Z+CO2―→X+O2
③Z+H2O―→Y+O2↑
④X+Ca(OH)2―→Y+CaCO3↓
试回答下列问题:
(1)W、X、Y、Z的化学式分别是:W:________、X:________、Y:________、Z:________。
(2)以上4个化学反应,属于氧化还原反应的是________(填反应序号),反应中氧化剂是________(写化学式),还原剂是________(写化学式)。
(3)若④反应在溶液中进行,写出其离子方程式以及能用该离子方程式表示的另一个化学反应的化学方程式:①离子方程式:__________________________。②化学方程式:_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
某强酸性溶液X中含有Ba2+、Al3+、NH4+、Fe2+、Fe3+、CO32-、SiO32-、SO42-、NO3-中的一种或几种离子。为确定溶液X的成分,进行如下实验: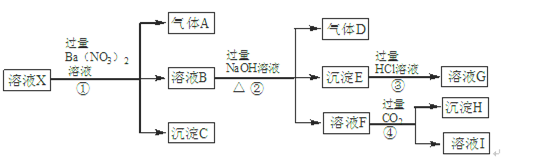
根据以上信息,请回答下列问题:
(1)溶液X中肯定不含有的离子是 ,不能确定是否含有的离子是 ,若要确定是否含有这种离子,最可靠方法是:
。
(2)溶液I中所含溶质有 (填化学式)。
(3)步骤①②③④中,发生符合“强酸制弱酸”反应的步骤是 (填序号)。
(4)步骤①中生成气体A的离子方程式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
含铬化合物有毒,对人畜危害很大。因此含铬废水必须进行处理才能排放。
已知: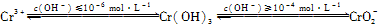
(1)在含+6价铬的废水中加入一定量的硫酸和硫酸亚铁,使+6价铬还原成+3价铬;再调节溶液pH在6~8之间,使Fe3+和Cr3+转化为Fe(OH)3、Cr(OH)3沉淀而除去。
①写出Cr2O72-与FeSO4溶液在酸性条件下反应的离子方程式:________________。
②用离子方程式表示溶液pH不能超过10的原因:____。
(2)将含+6价铬的废水放入电解槽内,用铁作阳极,加入适量的氯化钠进行电解。阳极区生成的Fe2+和Cr2O72-发生反应,生成的Fe3+和Cr3+在阴极区与OH-结合成氢氧化物沉淀而除去。
①写出阴极的电极反应式:________________。
②电解法中加入氯化钠的作用是________________。
(3)铬化学丰富多彩,由于铬光泽度好,常将铬镀在其他金属表面,同铁、镍组成各种性能的不锈钢,CrO3大量地用于电镀工业中。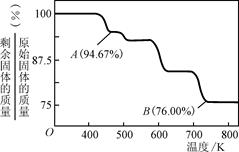
①CrO3具有强氧化性,遇到有机物(如酒精)时,猛烈反应以至着火,若该过程中乙醇被氧化成乙酸,CrO3被还原成绿色的硫酸铬[Cr2(SO4)3]。则该反应的化学方程式为____。
②CrO3的热稳定性较差,加热时逐步分解,其固体残留率随温度的变化如右图所示,则B点时剩余固体的成分是________________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
某强酸性溶液X可能含有Ba2+、A13+、NH4+、Fe2+、Fe3+、CO32-、SO32-、SO42-、C1-、NO3-中的一种或几种,取该溶液进行连续实验,实验过程如下: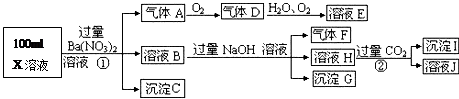
根据以上信息,回答下列问题:
(1)气体F为
(2)上述离子中,溶液X中除H+外还肯定含有的离子是 ,不能确定是否含有的离子是 .
(3)写出生成A的离子方程式:
(4)通常可以利用KClO在碱性条件下氧化G来制备一种新型、高效、多功能水处理剂K2FeO4.请写出制备过程中的离子方程式 .
(5)假设测定A、F、I均为0.1mol,100mL X溶液中n(H+)=0.4mol,且不能确定的离子只有一种。当X溶液中不能确定的离子是 ,则沉淀C的物质的量为
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
按要求完成下列填空
(1)写出下列物质的电离方程式:
Fe2(SO4)3_____________________________________________,
NaHCO3______________________________________________;
(2)写出下列反应的离子方程式:
稀盐酸与碳酸钙反应___________________________________,
氢氧化钡溶液与稀硫酸反应_______________________________;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com