
【题目】元素周期律产生的根本原因就是随着元素原子序数的递增
A. 元素的相对原子质量逐渐增大
B. 核外电子排布呈周期性变化
C. 原子半径呈周期性变化
D. 元素主要化合价呈周期性变化
 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
【题目】中和相同体积、相同pH值的H2SO4、HCl和CH3COOH三种稀溶液,所需相同浓度的NaOH溶液的体积为V1、V2和V3,则( )
A.V1>V2>V3B.V3>V2>V1
C.V3>V1=V2D.V1>V2=V3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于金属性质的叙述正确的是
A.金属一般都容易导电导热,有延展性
B.金属具有较高的硬度和熔点
C.所有金属都是固态
D.金属单质都能与稀H2SO4反应产生H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,将 2 mol SO2 和 1 mol O2 充入2L密闭容器中,在催化剂存在下进行下列反应: 2SO2+ O2 ![]() 2SO3,下列说法中正确的是
2SO3,下列说法中正确的是
A. 达到反应限度时,生成2molSO3
B. 达到反应限度时SO2的消耗速率必定等于O2的生成速率
C. 达到反应限度时SO2、O2、SO3的分子数之比一定为2∶1∶2
D. SO2和SO3物质的量之和一定为 2mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图所示装置测定中和热的实验步骤如下:
①用量筒量取50 mL 0.50 mol·L-1盐酸倒入小烧杯中,测出盐酸温度;
②用另一量筒量取50 mL 0.55 mol·L-1 NaOH溶液,并用同一温度计测出其温度;
③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测得混合液最高温度。回答下列问题:

(1)该图中有两处未画出,它们是______、__________。
(2)为什么所用NaOH溶液要稍过量_________________。
(3)倒入NaOH溶液的正确操作是_______________________。
(4)现将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和1 L 1 mol·L-1的稀盐酸恰好完全反应,其反应热分别为ΔH1、ΔH2、ΔH3,则ΔH1、ΔH2、ΔH3的大小关系为______。
(5)假设盐酸和氢氧化钠溶液的密度都是1 g·cm-3,又知中和反应后生成溶液的比热容c=4.18 J·g-1·℃-1。为了计算中和热,某学生实验记录数据如下:
实验 序号 | 起始温度t1/ ℃ | 终止温度t2/ ℃ | |
盐酸 | 氢氧化钠溶液 | 混合溶液 | |
1 | 20.0 | 20.1 | 23.2 |
2 | 20.2 | 20.4 | 23.4 |
3 | 20.5 | 20.6 | 23.6 |
依据该学生的实验数据计算,该实验测得的中和热ΔH=______(结果保留一位小数)。
(6)____(填“能”或“不能”)用Ba(OH)2溶液和硫酸代替氢氧化钠溶液和盐酸,理由是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素的性质随着原子序数的递增呈周期性变化的原因是
A. 元素的化合价的周期性变化
B. 元素原子的原子半径的周期性变化
C. 元素原子的核外电子排布的周期性变化
D. 元素原子的电子层数的周期性变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关系曲线不能正确反映其对应变化关系的是( )
A. 加热KClO3和MnO2固体混合物
B. 向Ca(OH)2溶液中通入CO2至过量(碳酸钙遇到溶有二氧化碳的水,能生成可溶性碳酸氢钙) 
C. 向一定浓度的NaOH溶液中加水稀释
D. 将等质量的Mg和Al分别与过量等浓度的盐酸反应,则a为Mg,b为Al
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为研究生铁(含少量碳)与浓硫酸的反应情况及产物性质,设计如下实验装置(夹持装置及尾气处理装置未画出)。请回答下列问题:
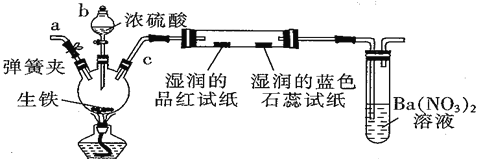
A B C
(1)仪器b 的名称为____________,按照上图装置进行实验,实验过程中,装置B中的现象是湿润的品红试纸__________________,湿润的蓝色石蕊试纸____________ 。若观察到装置C中会出现白色沉淀,原因是_____________________________。
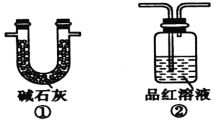

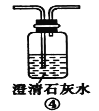
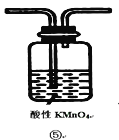
(2)装置A中还会产生能够使得澄清石灰水变浑浊的另一种气体,请写出产生该气体的化学方程式____________________________为了验证该气体,应从下列①~⑤中选出必要的装置连接装置A中出口C处,从左到右的顺序是_____________(填序号),连接好装置,然后打开弹簧夹a,多次鼓入N2,其目的是________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的酸性强弱比较正确的是( )
A. HBrO4<HIO4 B. H2SO4<H3PO4 C. HClO3<HClO D. H2SO4>H2SO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com