
【题目】实验室制备叔丁基苯(![]() )的反应和有关数据如下:
)的反应和有关数据如下:
![]() +ClC(CH3)3
+ClC(CH3)3![]()
![]() +HCl
+HCl
物质 | 相对分子质量 | 密度/gcm-3 | 熔点/℃ | 沸点/℃ | 溶解性 |
AlCl3 | —— | —— | 190 | 易升华 | 遇水极易潮解并产生白色烟雾,微溶于苯 |
苯 | 78 | 0.88 | —— | 80.1 | 难溶于水,易溶于乙醇 |
氯代叔丁烷 | 92.5 | 1.85 | —— | 51.6 | 难溶于水,可溶于苯 |
叔丁基苯 | 134 | 0.87 | —— | 169 | 难溶于水,易溶于苯 |
I.如图是实验室制备无水AlCl3可能需要的装置:
A.  B.
B. 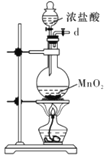 C.
C. 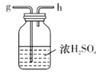 D.
D.  E.
E.  F.
F. 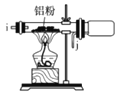
(1)检查B装置气密性的方法是__________。
(2)制备无水AlCl3的装置的合理的连接顺序为________(填小写字母),其中E装置的作用是___________。
(3)实验时应先加热圆底烧瓶再加热硬质玻璃管,其原因是________。
II.如图是实验室制备叔丁基苯的装置(夹持装置略):

在三颈烧瓶中加入50mL的苯和适量的无水AlCl,由恒压漏斗滴加氯代叔丁烷10 mL,一定温度下反应一段时间后,将反应后的混合物洗涤分离,在所得产物中加入少量无水MgSO4固体,静置,过滤,蒸馏得叔丁基苯20 g。
使用恒压漏斗的优点是_________;加入无水MgSO4固体的作用是____________________________________。
(5)洗涤混合物时所用的试剂有如下三种,正确的使用顺序是__________(填序号)
①5%的Na2CO3溶液 ②稀盐酸 ③H2O
(6)本实验中叔丁基苯的产率为______________(保留3位有效数字)
【答案】分液漏斗注入水后,关闭止水夹,打开分液漏斗的活塞使液体流下,一段时间后液体不能继续流下,说明气密性良好 defghijc 防止空气中的水蒸气进入,吸收多余的氯气 若先加热硬质玻璃管,Al先与O2反应,无法制得纯净AlCl3 使液体顺利滴下 干燥 ②①③ 74.6%
【解析】
实验室制备无水AlCl3,需要干燥的氯气与铝在加热条件下反应,题中B用于制备氯气,用D、C装置分别除去HCl、水,用F装置制备氯化铝,避免固体堵塞导管,最后连接E,以吸收空气中的水,且防止氯气污染空气;
Ⅱ.如图是实验室制备叔丁基苯的装置,在三颈烧瓶中加入50 mL的苯和适量的无水AlCl3,由恒压漏斗滴加氯代叔丁烷10mL,恒压漏斗可使液体顺利滴下,产物中加入无水硫酸镁,可起到干燥的作用,反应后混合物中含有氯化铝以及水解生成的氢氧化铝,可加入稀盐酸,然后加入碳酸钠除去盐酸,最后加入水洗涤,以此解答该题。
(1)检查B装置气密性,可利用压强差原理,将分液漏斗注入水后,关闭止水夹,打开分液漏斗的活塞使液体流下,一段时间后液体不能继续流下,说明气密性良好;故答案为:分液漏斗注入水后,关闭止水夹,打开分液漏斗的活塞使液体流下,一段时间后液体不能继续流下,说明气密性良好。
⑵B用于制备氯气,用D、C装置分别除去HCl、水,用F装置制备氯化铝,避免固体堵塞导管,最后连接E,以吸收空气中的水,且防止氯气污染空气,则连接顺序为defghijc;故答案为:defghijc;防止空气中的水蒸气进入,吸收多余的氯气。
(3)实验时应先加热圆底烧瓶再加热硬质玻璃管,原因是若先加热硬质玻璃管,Al先与O2反应,无法制得纯净AlCl3,加热圆底烧瓶,生成的氯气可将装置内的空气排出;故答案为:若先加热硬质玻璃管,Al先与O2反应,无法制得纯净AlCl3。
(4)使用恒压漏斗的优点是使液体顺利滴下,MgSO4固体具有吸水作用,加入无水MgSO4固体可起到干燥的作用;故答案为:使液体顺利滴下;干燥。
(5)反应后混合物中含有氯化铝以及水解生成的氢氧化铝,可加入稀盐酸,然后加入碳酸钠除去盐酸,最后加入水洗涤,则顺序为②①③,故答案为:②①③;
(6)50mL的苯的物质的量为50mL×0.55gmL-1÷78gmol-1=0.35mol,10mL氯代叔丁烷的物质的量为10mL×1.85gmL-1÷ 92.5gmol-1=0.2mol,由方程式可知理论可生成0.2mol叔丁基苯,质量为0.2mol×134gmol-1=26.8g,则产率为20g÷26.8g×100%=74.6%,故答案为:74.6%。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某溶液中只可能含有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 中的若干种离子,且所含有的离子浓度均为
中的若干种离子,且所含有的离子浓度均为![]() 。某同学为确定其成分,进行如图所示实验:
。某同学为确定其成分,进行如图所示实验:
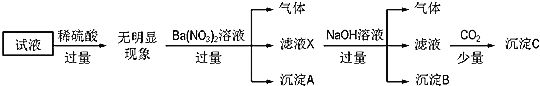
下列说法正确的是( )
A.无法确定原试液中是否含有![]() 、
、![]()
B.滤液X中大量存在的阳离子有![]() 、
、![]() 和
和![]()
C.无法确定沉淀C的成分
D.原溶液中存在的离子为![]() 、
、![]() 、
、![]() 、
、![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的乙醇在氧气不足的情况下燃烧,得到CO、CO2和水的总质量为27.6g,若其中水的质量为10.8g,则CO的质量是( )
A. 1.4gB. 2.2gC. 4.4gD. 在2.2g和4.4g之间
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】本题涉及部分铜及其化合物的相关结构问题的考查,请回答下列问题。
(1)写出基态Cu2+的核外电子排布式:________。Cu的同周期元素中,与铜原子最外层电子数相等的元素原子还有___________(用元素符号表示)。
(2)从原子结构角度分析高温Cu2O比CuO稳定的原因是___________。
(3)[Cu(NH3)2]Ac可用于合成氨工业中的铜洗工序,除去进人合成塔前混合气中的CO(CO能使催化剂中毒)。
①Ac表示CH3COO-,Ac中碳原子的杂化方式为________。
②[Cu(NH3)2]Ac能够结合CO的原因是________。
(4)铜原子与氯原子形成化合物的晶胞如图所示(黑球代表铜原子,白球表示氯原子)。
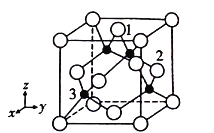
①已知铜和氯的电负性分别为1.9和3.0,则铜与氯形成的化合物属于________填(“离子”或“共价”)化合物。
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图中原子1的坐标为(![]() ,
,![]() ,1),则原子2和3的坐标分别为___________、__________。
,1),则原子2和3的坐标分别为___________、__________。
③已知该晶体的密度为ρg/cm3,阿伏加德罗常数为NA,则该晶体中铜原子和氯原子的最短距离为_____________pm(只写计算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向某Na2CO3、NaHCO3的混合溶液中加入少量的BaCl2,测得溶液中![]() 与
与![]() 的关系如图所示,下列说法正确的是
的关系如图所示,下列说法正确的是
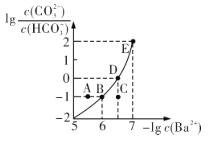
A.该溶液中![]()
B.B、D、E三点对应溶液pH的大小顺序为B>D>E
C.A、B、C三点对应的分散系中,A点的稳定性最差
D.D点对应的溶液中一定存在2c(Ba2+ ) +c(Na+ )+c(H+ )=c(CO32- )+c(OH- )+c(Cl- )
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分别取40mL的0.50mol·L-1盐酸与40mL的0.55mol·L-1NaOH溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热。请回答下列问题:
(1)理论上稀强酸、稀强碱反应生成1mol水时放出57.3kJ的热量,写出表示稀硫酸和稀NaOH溶液反应的中和热的热化学方程式__。
(2)如图所示,A为泡沫塑料板,上面有两个小孔,分别插入温度计和环形玻璃搅拌棒,两个小孔不能开得过大,其原因是__。
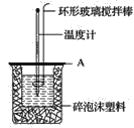
(3)假设盐酸和NaOH溶液的密度都是1g·cm-3,又知中和后生成溶液的比热容c=4.18J·g-1·℃-1。为了计算中和热,实验时还需测量的数据有(填字母)__。
A.反应前盐酸溶液的温度
B.反应前盐酸溶液的质量
C.反应前NaOH溶液的温度
D.反应前NaOH溶液的质量
E.反应后混合溶液的最高温度
F.反应后混合溶液的质量
(4)某学生实验记录数据如下:
实验序号 | 起始温度t1/℃ | 终止温度t2/℃ | |
盐酸 | NaOH | ||
1 | 20.0 | 20.1 | 23.2 |
2 | 20.2 | 20.4 | 23.4 |
3 | 20.5 | 20.6 | 23.6 |
依据该学生的实验数据计算,该实验测得的中和热ΔH=__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应N2O4(g)![]() 2NO2(g)在温度一定时,平衡体系中NO2的体积分数φ(NO2)随压强的变化情况如图所示(实线上任何一点为对应压强下的平衡点),下列说法正确的是( )
2NO2(g)在温度一定时,平衡体系中NO2的体积分数φ(NO2)随压强的变化情况如图所示(实线上任何一点为对应压强下的平衡点),下列说法正确的是( )
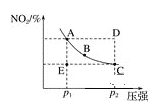
A. A、C两点的正反应速率的关系为A>C
B. A、B、C、D、E各状态中,v(正)<v(逆)的是状态E
C. 使E状态从水平方向到达C状态后,再沿平衡曲线到达A状态,从理论上来讲,可选用的条件是从p1突然加压到p2,再由p2无限缓慢降压至p1
D. 维持p1不变,E→A所需时间为x;维持p2不变,D→C所需时间为y;则x<y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T℃时,体积为0.5L的恒容密闭容器中发生可逆反应:2A(g)+B(g)![]() 2C(g) ΔH=-QkJ·mol-1(Q>0)。保持温度不变,实验测得起始和平衡时的有关数据如表:
2C(g) ΔH=-QkJ·mol-1(Q>0)。保持温度不变,实验测得起始和平衡时的有关数据如表:
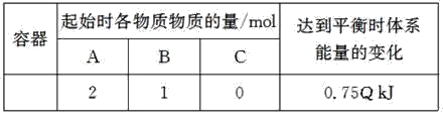
其他条件不变,若容器保持恒容绝热,则达到平衡时C的体积分数____![]() (填“<”、“=”或“>”)。
(填“<”、“=”或“>”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计如图装置制取少量溴苯,请回答下列问题:
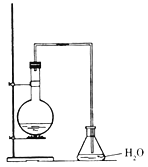
(1)写出实验室制取溴苯的化学方程式:___。
(2)上述反应发生后,在锥形瓶中加入硝酸银溶液观察到的现象是___,这一现象能否说明溴和苯发生了取代反应(填“能”或“不能”)___,理由是___。
(3)反应后得到的溴苯中溶有少量苯、溴、三溴苯、溴化铁和溴化氢等杂质,欲除去上述杂质,得到无水溴苯的合理实验操作步骤可设计为(分液操作已略去):①水洗②碱洗③水洗④干燥⑤蒸馏。则上述操作②碱洗的主要目的是(填序号)___。
A.除三溴苯和溴化氢 B.除溴化铁和三溴苯
C.除溴和溴化氢 D.除苯和溴
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com