
ЁОЬтФПЁПЗжБ№ШЁ40mLЕФ0.50molЁЄL-1бЮЫсгы40mLЕФ0.55molЁЄL-1NaOHШмвКНјаажаКЭЗДгІЁЃЭЈЙ§ВтЖЈЗДгІЙ§ГЬжаЫљЗХГіЕФШШСППЩМЦЫужаКЭШШЁЃЧыЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉРэТлЩЯЯЁЧПЫсЁЂЯЁЧПМюЗДгІЩњГЩ1molЫЎЪБЗХГі57.3kJЕФШШСПЃЌаДГіБэЪОЯЁСђЫсКЭЯЁNaOHШмвКЗДгІЕФжаКЭШШЕФШШЛЏбЇЗНГЬЪН__ЁЃ
ЃЈ2ЃЉШчЭМЫљЪОЃЌAЮЊХнФЫмСЯАхЃЌЩЯУцгаСНИіаЁПзЃЌЗжБ№ВхШыЮТЖШМЦКЭЛЗаЮВЃСЇНСАшАєЃЌСНИіаЁПзВЛФмПЊЕУЙ§ДѓЃЌЦфдвђЪЧ__ЁЃ
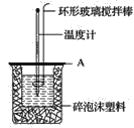
ЃЈ3ЃЉМйЩшбЮЫсКЭNaOHШмвКЕФУмЖШЖМЪЧ1gЁЄcm-3ЃЌгжжЊжаКЭКѓЩњГЩШмвКЕФБШШШШнcЃН4.18JЁЄg-1ЁЄЁц-1ЁЃЮЊСЫМЦЫужаКЭШШЃЌЪЕбщЪБЛЙашВтСПЕФЪ§Онга(ЬюзжФИ)__ЁЃ
AЃЎЗДгІЧАбЮЫсШмвКЕФЮТЖШ
BЃЎЗДгІЧАбЮЫсШмвКЕФжЪСП
CЃЎЗДгІЧАNaOHШмвКЕФЮТЖШ
DЃЎЗДгІЧАNaOHШмвКЕФжЪСП
EЃЎЗДгІКѓЛьКЯШмвКЕФзюИпЮТЖШ
FЃЎЗДгІКѓЛьКЯШмвКЕФжЪСП
ЃЈ4ЃЉФГбЇЩњЪЕбщМЧТМЪ§ОнШчЯТЃК
ЪЕбщађКХ | Ц№ЪМЮТЖШt1/Ёц | жежЙЮТЖШt2/Ёц | |
бЮЫс | NaOH | ||
1 | 20.0 | 20.1 | 23.2 |
2 | 20.2 | 20.4 | 23.4 |
3 | 20.5 | 20.6 | 23.6 |
вРОнИУбЇЩњЕФЪЕбщЪ§ОнМЦЫуЃЌИУЪЕбщВтЕУЕФжаКЭШШІЄHЃН__ЁЃ
ЁОД№АИЁПNaOH(aq)ЃЋ![]() H2SO4(aq)=
H2SO4(aq)=![]() Na2SO4(aq)ЃЋH2O(l) ІЄHЃНЃ57.3kJЁЄmol-1 МѕЩйШШСПЩЂЪЇ ACE Ѓ51.8 kJЁЄmol-1
Na2SO4(aq)ЃЋH2O(l) ІЄHЃНЃ57.3kJЁЄmol-1 МѕЩйШШСПЩЂЪЇ ACE Ѓ51.8 kJЁЄmol-1
ЁОНтЮіЁП
(1)ИљОнЫсМюжаКЭЗДгІЩњГЩ1molвКЬЌЫЎЪБЗХГі57.3kJЕФШШСПЪщаДШШЛЏбЇЗНГЬЪНЃЛ
(2)ИљОнВтЖЈжаКЭШШЙ§ГЬжаБиаыОЁСПМѕЩйШШСПЕФЩЂЪЇЗжЮіЃЛ
(3)ИљОнжаКЭШШМЦЫуЙЋЪНQ=cmЁїTжаЩцМАЕФЮДжЊЪ§ОнНјааХаЖЯЃЛ
(4)ЯШИљОнБэжаВтЖЈЪ§ОнМЦЫуГіЛьКЯвКЗДгІЧАКѓЕФЦНОљЮТЖШВюЃЌдйИљОнQ=cmЁїTМЦЫуГіЗДгІЗХГіЕФШШСПЃЌзюКѓМЦЫуГіжаКЭШШЁЃ
(1)жаКЭШШЪЧжИЫсЁЂМюЕФЯЁШмвКЭъШЋЗДгІЩњГЩ1 molЫЎЪБЕФЗДгІШШЃЌдђБэЪОЯЁСђЫсКЭNaOHЯЁШмвКжаКЭШШЕФШШЛЏбЇЗНГЬЪНжаЫЎЕФМЦСПЪ§ЮЊ1 molЃЌМДЃКNaOH(aq)ЃЋ![]() H2SO4(aq)=
H2SO4(aq)=![]() Na2SO4(aq) ЃЋH2O(l)ЁЁІЄHЃНЃ57.3 kJЁЄmolЃ1ЃЌ
Na2SO4(aq) ЃЋH2O(l)ЁЁІЄHЃНЃ57.3 kJЁЄmolЃ1ЃЌ
ЙЪД№АИЮЊЃКNaOH(aq)ЃЋ![]() H2SO4(aq)=
H2SO4(aq)=![]() Na2SO4(aq) ЃЋH2O(l)ЁЁІЄHЃНЃ57.3 kJЁЄmolЃ1ЃЛ
Na2SO4(aq) ЃЋH2O(l)ЁЁІЄHЃНЃ57.3 kJЁЄmolЃ1ЃЛ
(2)ХнФЫмСЯАхЩЯУцСНИіаЁПзЃЌЗжБ№ВхШыЮТЖШМЦКЭЛЗаЮВЃСЇНСАшАєЃЌШєСНИіаЁПзПЊЕУЙ§ДѓЃЌЛсЕМжТЩЂЪЇНЯЖрЕФШШСПЃЌгАЯьВтЖЈНсЙћЃЌ
ЙЪД№АИЮЊЃКМѕЩйШШСПЩЂЪЇЃЛ
(3)гЩQЃНcmІЄTПЩжЊЃЌВтЖЈжаКЭШШашвЊВтЖЈЕФЪ§ОнЮЊЗДгІЧАбЮЫсШмвКЕФЮТЖШЁЂЗДгІЧАNaOHШмвКЕФЮТЖШКЭЗДгІКѓЛьКЯШмвКЕФзюИпЮТЖШЃЌ
ЙЪД№АИЮЊЃКACEЃЛ
(4)Ек1ДЮЪЕбщбЮЫсКЭNaOHШмвКЦ№ЪМЦНОљЮТЖШЮЊ20.05 ЁцЃЌЗДгІКѓЮТЖШЮЊ23.2 ЁцЃЌЗДгІЧАКѓЮТЖШВюЮЊ3.15 ЁцЃЛЕк2ДЮЪЕбщбЮЫсКЭNaOHШмвКЦ№ЪМЦНОљЮТЖШЮЊ20.3 ЁцЃЌЗДгІЧАКѓЮТЖШВюЮЊ3.1 ЁцЃЛЕк3ДЮЪЕбщбЮЫсКЭNaOHШмвКЦ№ЪМЦНОљЮТЖШЮЊ20.55 ЁцЃЌЗДгІЧАКѓЮТЖШВюЮЊ3.05 ЁцЃЛ40 mLЕФ0.50 molЁЄLЃ1бЮЫсгы40 mLЕФ0.55 molЁЄLЃ1NaOHШмвКЕФжЪСПКЭЮЊmЃН80 mLЁС1 gЁЄcmЃ3ЃН80 gЃЌcЃН4.18 JЁЄgЃ1ЁЄЁцЃ1ЃЌДњШыЙЋЪНQЃНcmІЄTЕУЩњГЩ0.02 molЕФЫЎЗХГіШШСПQЃН4.18 JЁЄgЃ1ЁЄЁцЃ1ЁС80 gЁС![]() Ёж1.037 kJЃЌЩњГЩ1 molЕФЫЎЗХГіШШСПЮЊ1.037 kJЁС
Ёж1.037 kJЃЌЩњГЩ1 molЕФЫЎЗХГіШШСПЮЊ1.037 kJЁС![]() ЁжЃ51.8 kJЁЄmolЃ1ЃЌИУЪЕбщВтЕУЕФжаКЭШШІЄHЃНЃ51.8 kJЁЄmolЃ1ЃЌ
ЁжЃ51.8 kJЁЄmolЃ1ЃЌИУЪЕбщВтЕУЕФжаКЭШШІЄHЃНЃ51.8 kJЁЄmolЃ1ЃЌ
ЙЪД№АИЮЊЃКЃ51.8 kJЁЄmol-1ЁЃ



| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯжгаAЁЂBЁЂCЁЂDЁЂEЁЂFдзгађЪ§вРДЮдіДѓЕФСљжждЊЫиЃЌЫќУЧЮЛгкдЊЫижмЦкБэЕФЧАЫФжмЦкЁЃвбжЊBдЊЫиLВуЕчзгЪ§ЮЊKВуЩЯЕФ2БЖЃЌDЕФдзгКЫЭтДц8жждЫЖЏзДЬЌВЛЭЌЕФЕчзгЃЛEдЊЫигыFдЊЫиДІгкЭЌвЛжмЦкЯрСкЕФзхЃЌЫќУЧЕФдзгађЪ§ЯрВю3ЃЌЧвEдЊЫиЕФЛљЬЌдзгга4ИіЮДГЩЖдЕчзгЁЃЧыЛиД№ЯТСаЮЪЬтЃК
(1)аДГіDдзгЛљЬЌЕФМлВуЕчзгХХВМЭМЃК________ЁЃ
(2)ЯТСаЫЕЗЈДэЮѓЕФЪЧ____________(ЬюађКХ)ЁЃ
A.ЖўбѕЛЏЙшЕФЯрЖдЗжзгжЪСПБШЖўбѕЛЏЬМДѓЃЌЫљвдЗаЕуЃК![]()
B.ЕчИКадЃК![]()
C.![]() гы
гы![]() ЛЅЮЊЕШЕчзгЬхЃЌНсЙЙЯрЫЦЃЌЛЏбЇаджЪЯрЫЦ
ЛЅЮЊЕШЕчзгЬхЃЌНсЙЙЯрЫЦЃЌЛЏбЇаджЪЯрЫЦ
D.ЮШЖЈадЃК![]() ЃЌЪЧвђЮЊЫЎЗжзгМфДцдкЧтМќЕФдЕЙЪ
ЃЌЪЧвђЮЊЫЎЗжзгМфДцдкЧтМќЕФдЕЙЪ
(3)FРызгЪЧШЫЬхФкЖржжУИЕФИЈвђзгЃЌШЫЙЄФЃФтУИЪЧЕБЧАбаОПЕФШШЕуЁЃЯђдЊЫиFЕФСђЫсбЮШмвКжаЭЈШыЙ§СПЕФЦјЬхX(XгЩCЁЂAСНжждЊЫиаЮГЩЕФКЌга10ИіЕчзгЕФЮЂСЃ)ПЩЩњГЩ![]() ЃЌИУРызгЕФНсЙЙЪНЮЊ____________(гУЯрЙидЊЫиЗћКХБэЪО)ЁЃ
ЃЌИУРызгЕФНсЙЙЪНЮЊ____________(гУЯрЙидЊЫиЗћКХБэЪО)ЁЃ
(4)ФГЛЏКЯЮягыF(Ђё)(ЂёБэЪОдЊЫиFЕФЛЏКЯМлЮЊ+1Мл)НсКЯаЮГЩШчЭМЫљЪОЕФРызгЃЌИУРызгжаЬМдзгЕФдгЛЏЗНЪНЪЧ_______ЁЃ
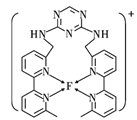
(5)вбжЊ![]() ЪЧжБЯпаЭЗжзгЃЌВЂгаЖдГЦадЃЌЧвЗжзгжаУПИідзгзюЭтВуЖМДяЕН8ЕчзгЮШЖЈНсЙЙЃЌдђ
ЪЧжБЯпаЭЗжзгЃЌВЂгаЖдГЦадЃЌЧвЗжзгжаУПИідзгзюЭтВуЖМДяЕН8ЕчзгЮШЖЈНсЙЙЃЌдђ![]() жаІвМќКЭІаМќЕФИіЪ§БШЮЊ____ЁЃ
жаІвМќКЭІаМќЕФИіЪ§БШЮЊ____ЁЃ
(6)CдЊЫизюИпМлКЌбѕЫсгыСђЫсЫсадЧПЖШЯрНќЃЌдвђЪЧ_______ЁЃ
(7)BЕЅжЪЕФвЛжжЭЌЫивьаЮЬхЕФОЇАћШчЭМЫљЪОЃК
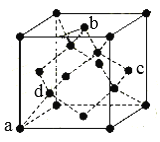
дђвЛИіОЇАћжаЫљКЌBдзгИіЪ§ЮЊ_____ЃЛЦфжадзгзјБъВЮЪ§ЮЊЃК![]() ЃЌ
ЃЌ![]() ЃЌ
ЃЌ![]() ЃЌдђcЕудзгЕФзјБъВЮЪ§ЮЊ______ЁЃ(зјБъЯЕШчЭМ)
ЃЌдђcЕудзгЕФзјБъВЮЪ§ЮЊ______ЁЃ(зјБъЯЕШчЭМ)
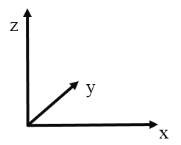
(8)DгыFаЮГЩРызгИіЪ§БШЮЊ1:1ЕФЛЏКЯЮяОЇАћгы![]() РрЫЦЃЌDРызгЕФХфЮЛЪ§ЪЧ________ЃЛЩшИУОЇАћЕФРтГЄЮЊa pmЃЌдђИУОЇЬхЕФУмЖШЮЊ________
РрЫЦЃЌDРызгЕФХфЮЛЪ§ЪЧ________ЃЛЩшИУОЇАћЕФРтГЄЮЊa pmЃЌдђИУОЇЬхЕФУмЖШЮЊ________![]() (гУЯрЙизжФИБэЪОЃЌвбжЊАЂЗќМгЕТТоГЃЪ§ЮЊNA)
(гУЯрЙизжФИБэЪОЃЌвбжЊАЂЗќМгЕТТоГЃЪ§ЮЊNA)
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвбжЊ1molЯТСаЮяжЪЭъШЋШМЩеЩњГЩЮШЖЈЕФВњЮяЪБЗХГіЕФШШСПШчЯТЃК

дђгЩC2H4(g)КЭH2O(l)ЗДгІЩњГЩC2H5OH(l)ЕФІЄHЮЊ(ЁЁЁЁ)
A.-44.2kJЁЄmol-1B.44.2kJЁЄmol-1
C.-330kJЁЄmol-1D.330kJЁЄmol-1
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЪЕбщВтЕУХЈЖШОљЮЊ0.5 mol. L-1ЕФPb(CH3COO)2ШмвКЕФЕМЕчадУїЯдШѕгкPb(NO3)2ШмвКЃЌгжжЊPbSЪЧВЛШмгкЫЎМАЯЁЫсЕФКкЩЋГСЕэЃЌЯТСаРызгЗНГЬЪНЪщаДДэЮѓЕФЪЧ
A.Pb(NO3)2ШмвКгыCH3COONaШмвКЛьКЯЃКPb2+ +2CH3COO-=Pb(CH3COO)2
B.Pb(NO3)2ШмвКгыK2SШмвКЛьКЯЃКPb2++S2-=PbSЁ§
C.Pb(CH3COO)2ШмвКгыK2SШмвКЛьКЯЃКPb(CH3COO)2+S2- =PbSЁ§+ 2CH3COO-
D.Pb(CH3COO)2дкЫЎжаЕчРыЃК Pb(CH3COO)2=Pb2+ +2CH3COO-
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЪЕбщЪвжЦБИЪхЖЁЛљБН(![]() )ЕФЗДгІКЭгаЙиЪ§ОнШчЯТЃК
)ЕФЗДгІКЭгаЙиЪ§ОнШчЯТЃК
![]() +ClC(CH3)3
+ClC(CH3)3![]()
![]() +HCl
+HCl
ЮяжЪ | ЯрЖдЗжзгжЪСП | УмЖШ/gcm-3 | ШлЕу/Ёц | ЗаЕу/Ёц | ШмНтад |
AlCl3 | ЁЊЁЊ | ЁЊЁЊ | 190 | взЩ§ЛЊ | гіЫЎМЋвзГБНтВЂВњЩњАзЩЋбЬЮэЃЌЮЂШмгкБН |
БН | 78 | 0.88 | ЁЊЁЊ | 80.1 | ФбШмгкЫЎЃЌвзШмгкввДМ |
ТШДњЪхЖЁЭщ | 92.5 | 1.85 | ЁЊЁЊ | 51.6 | ФбШмгкЫЎЃЌПЩШмгкБН |
ЪхЖЁЛљБН | 134 | 0.87 | ЁЊЁЊ | 169 | ФбШмгкЫЎЃЌвзШмгкБН |
I.ШчЭМЪЧЪЕбщЪвжЦБИЮоЫЎAlCl3ПЩФмашвЊЕФзАжУЃК
A.  B.
B. 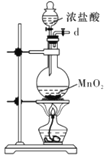 C.
C. 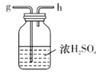 D.
D.  E.
E.  F.
F. 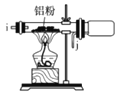
(1)МьВщBзАжУЦјУмадЕФЗНЗЈЪЧ__________ЁЃ
(2)жЦБИЮоЫЎAlCl3ЕФзАжУЕФКЯРэЕФСЌНгЫГађЮЊ________(ЬюаЁаДзжФИ)ЃЌЦфжаEзАжУЕФзїгУЪЧ___________ЁЃ
(3)ЪЕбщЪБгІЯШМгШШдВЕзЩеЦПдйМгШШгВжЪВЃСЇЙмЃЌЦфдвђЪЧ________ЁЃ
II.ШчЭМЪЧЪЕбщЪвжЦБИЪхЖЁЛљБНЕФзАжУ(МаГжзАжУТд)ЃК

дкШ§ОБЩеЦПжаМгШы50mLЕФБНКЭЪЪСПЕФЮоЫЎAlClЃЌгЩКубЙТЉЖЗЕЮМгТШДњЪхЖЁЭщ10 mLЃЌвЛЖЈЮТЖШЯТЗДгІвЛЖЮЪБМфКѓЃЌНЋЗДгІКѓЕФЛьКЯЮяЯДЕгЗжРыЃЌдкЫљЕУВњЮяжаМгШыЩйСПЮоЫЎMgSO4ЙЬЬхЃЌОВжУЃЌЙ§ТЫЃЌеєСѓЕУЪхЖЁЛљБН20 gЁЃ
ЪЙгУКубЙТЉЖЗЕФгХЕуЪЧ_________ЃЛМгШыЮоЫЎMgSO4ЙЬЬхЕФзїгУЪЧ____________________________________ЁЃ
(5)ЯДЕгЛьКЯЮяЪБЫљгУЕФЪдМСгаШчЯТШ§жжЃЌе§ШЗЕФЪЙгУЫГађЪЧ__________(ЬюађКХ)
Ђй5%ЕФNa2CO3ШмвК ЂкЯЁбЮЫс ЂлH2O
(6)БОЪЕбщжаЪхЖЁЛљБНЕФВњТЪЮЊ______________(БЃСє3ЮЛгааЇЪ§зж)
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПNAБэЪОАЂЗќМгЕТТоГЃЪ§ЕФжЕЁЃЯТСаЫЕЗЈВЛе§ШЗЕФЪЧЃЈ ЃЉ
A.ГЃЮТЯТЃЌ18gH2OжаЕчзгЪ§ОљЮЊ10NA
B.БъзМзДПіЯТЃЌ2molSO2КЭ1molO2ГфЗжЗДгІЩњГЩSO2ЕФЪ§ФПЮЊ2NA
C.ГЃЮТЯТЃЌ1L1molЁЄL-1Na2CO3ШмвКжаЃЌвѕРызгЪ§ФПДѓгкNA
D.1molCl2гыFeCl2ШмвКЭъШЋгыЗДгІЃЌзЊвЦЕчзгЕФЪ§ФПЮЊ2NA
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЮЊЗжБ№бщжЄЮТЖШЁЂХЈЖШЁЂДпЛЏМСПХСЃДѓаЁЖдЛЏбЇЗДгІЫйТЪЕФгАЯьЙцТЩЃЌФГЭЌбЇЩшМЦСЫШчЯТ4зщЪЕбщЁЃ

(1)ЩЯБэжаЃЌЗДгІЫйТЪзюПьЕФЪЧ_______ЃЛ
(2)ЪЕбщ3ЁЂ4дЄЦкПЩЕУГіЕФНсТлЪЧ_______ЃЛ
(3)ЩшМЦЪЕбщ2ЁЂ3ЕФФПЕФЪЧ_________ЃЛ
(4)ЩшМЦвЛИіЪЕбщжЄУїдкЦфЫќЬѕМўЯрЭЌЪБЃЌИФБфЮТЖШЖдЙ§бѕЛЏЧтЗжНтЫйТЪЕФгАЯь(аДГіВйзїВНжш)__________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвбжЊЮхжждЊЫиЕФдзгађЪ§ЕФДѓаЁЫГађЮЊCЃОAЃОBЃОDЃОEЃЛAЁЂCЭЌжмЦкЃЌBЁЂCЭЌжїзхЃЌAгыBаЮГЩЕФРызгЛЏКЯЮяA2BжаЫљгаРызгЕФЕчзгЪ§ЯрЭЌЃЌЦфЕчзгзмЪ§ЮЊ30ЃЛDКЭEПЩаЮГЩ4КЫ10ИіЕчзгЗжзгЁЃЪдЛиД№ЯТСаЮЪЬтЃК
(1)аДГіЮхжждЊЫиУћГЦЃКA_______B________C________D_______E______
(2)гУЕчзгЪНБэЪОРызгЛЏКЯЮяA2BЕФаЮГЩЙ§ГЬЃК_____________________
(3)аДГіЯТСаЮяжЪЕФЛЏбЇЪНЁЂЕчзгЪНЛђНсЙЙЪНЃК
ЂйDдЊЫиаЮГЩЕФЕЅжЪЕФНсЙЙЪН___________
ЂкEКЭBаЮГЩЛЏКЯЮяЕФЕчзгЪН___________ЁЂ___________
ЂлAЁЂBЁЂEаЮГЩЕФЛЏКЯЮяЕФЛЏбЇЪНЮЊ________
ЂмDЁЂEаЮГЩЕФЛЏКЯЮяПеМфНсЙЙаЭЮЊ________аЮ_________адЗжзг
ЂнDЁЂCЁЂEаЮГЩЕФЛЏКЯЮяЕФЛЏбЇЪНЮЊ____________
ЂоDЁЂEаЮГЩЕФЛЏКЯЮяЮЊ______ЛЏКЯЮяЃЌ(ЬюЁАРызгЁБЛђЁАЙВМлЁБ)АќКЌЕФЛЏбЇМќЮЊ______________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвЛЖЈЮТЖШЯТНЋCl2ЛКТ§ЭЈШыЫЎжаЁЃЕБЭЈШыЕФCl2ЬхЛ§ЮЊV1ЪБДяЕНБЅКЭЃЌШмвКжаc(H+ЃЉБфЛЏШчЭМжаЧњЯпaЁЃвбжЊCl2ЕФШмНтЖШЫцЮТЖШЩ§ИпЖјбИЫйНЕЕЭЃЌЯТСаа№Ъіжае§ШЗЕФЪЧЃЈ ЃЉ
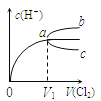
A.НЋБЅКЭТШЫЎМгЫЎЯЁЪЭЃЌШмвКжаc(H+)БфЛЏШчЧњЯпb
B.НЋБЅКЭТШЫЎНЕЕЭЮТЖШЃЌШмвКжаc(H+)БфЛЏШчЧњЯпc
C.дкБЅКЭТШЫЎжаМгШыNaOHЪЙpHЃО7ЃЌЫљЕУШмвКжаДцдкЯТСаЙиЯЕЃКc(Na+)+c(H+)=c(Cl-)+c(OH-)+c(ClO-)
D.дкБЅКЭТШЫЎжаМгШыNaOHЪЙpH=7ЃЌЫљЕУШмвКжаДцдкЯТСаЙиЯЕЃКc(Na+)ЃОc(ClO-)ЃОc(Cl-)ЃОc(HClO)
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com