
ЁОЬтФПЁПвћгУЫЎжЪСПЪЧЙиЯЕШЫРрНЁПЕЕФживЊЮЪЬтЁЃ
(1)Cl2ЪЧзюдчгУгквћгУЫЎЯћЖОЕФЮяжЪЃЌаДГіCl2ШмгкЫЎЗЂЩњЗДгІЕФРызгЗНГЬЪН________________ЁЃ
(2)C1O2ЪЧвЛжжИпаЇЁЂЕЭЖОЕФЯћЖОМСЃЌж№НЅШЁДњCl2ГЩЮЊЩњВњздРДЫЎЕФЯћЖОМСЁЃKClO3гыSO2дкЧПЫсадШмвКжаЗДгІПЩжЦЕУC1O2ЃЌДЫЗДгІЕФРызгЗНГЬЪНЮЊ_________________ЁЃClO2ПЩНЋЗЯЫЎжаЕФMn2+зЊЛЏЮЊMnO2ЖјГ§ШЅЃЌБОЩэЛЙдЮЊCl-ЃЌИУЗДгІЙ§ГЬжабѕЛЏМСгыЛЙдМСЕФЮяжЪЕФСПжЎБШЮЊ___________ЁЃ
(3)ИпЬњЫсМи(K2FeO4)ЪЧвЛжжаТаЭЁЂИпаЇЁЂЖрЙІФмЫЎДІРэМСЃЌБШCl2ЁЂClO2бѕЛЏадИќЧПЃЌЮоЖўДЮЮлШОЕФТЬЩЋЫЎДІРэМСЁЃЙЄвЕЩЯЯШжЦЕУИпЬњЫсФЦЃЌШЛКѓдкЕЭЮТЯТЃЌЯђИпЬњЫсФЦШмвКжаМгШыKOHжСБЅКЭОЭПЩЮіГіИпЬњЫсМиЁЃгЩвдЩЯаХЯЂПЩжЊЃЌЯрЭЌЬѕМўЯТЃЌИпЬњЫсФЦШмНтЖШБШИпЬњЫсМиШмНтЖШ______ (ЬюЁАДѓЁБЛђЁАаЁЁБ)ЁЃИЩЗЈжЦБИИпЬњЫсФЦЕФжївЊЗДгІЮЊ2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2ЁќЃЌИУЗДгІУПЩњГЩ1 molNa2FeO4зЊвЦ____molЕчзгЁЃ
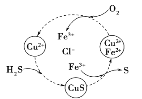
(4)НЋH2SКЭПеЦјЕФЛьКЯЦјЬхЭЈШыFeCl3ЁЂFeCl2ЁЂCuCl2ЕФЛьКЯШмвКжаЗДгІПЩвдЛиЪеSЃЌЦфЮяжЪзЊЛЏШчЭМЫљЪОЁЃдкЭМЪОЕФзЊЛЏжаЃЌЛЏКЯМлВЛБфЕФдЊЫиЪЧ_______ЁЃИУЭМЪОЕФзмЗДгІЮЊ ______ЁЃ
ЁОД№АИЁПCl2+H2OЈTH++ClЉ+HClO 2ClO3Љ+SO2ЈT2ClO2+SO42Љ 2ЃК5 Дѓ 5 HЁЂClЁЂCu 2H2S+O2=2S![]() +2H2O
+2H2O
ЁОНтЮіЁП
ЃЈ1ЃЉТШЦјгыЫЎЗДгІЩњГЩHClЁЂHClOЃЛ
ЃЈ2ЃЉKClO3гыSO2дкЧПЫсадШмвКжаЗДгІПЩжЦЕУC1O2ЃЌПЩжЊSO2БЛбѕЛЏГЩSO42ЉЃЌИУРызгЗДгІЮЊ2ClO3Љ+SO2ЈT2ClO2+SO42ЉЃЛClO2ПЩНЋЗЯЫЎжаЕФMn2+зЊЛЏЮЊMnO2ЖјГ§ШЅЃЌБОЩэЛЙдЮЊCl-ЃЌЦфРызгЗНГЬЪНЮЊ2ClO2+ 5Mn2++6H2O=5MnO2+ 2Cl-+12H+ЃЌПЩжЊИУЗДгІбѕЛЏМСгыЛЙдМСЮяжЪЕФСПжЎБШЃЛ
ЃЈ3ЃЉдкЕЭЮТЯТЃЌИпЬњЫсМиШнвзБфГЩЙЬЬхЮіГіЃЌЫЕУїИпЬњЫсМидкЕЭЮТЯТЕФШмНтЖШБШИпЬњЫсФЦЕФШмНтЖШаЁЃЌЗДгІ2FeSO4+6Na2O2ЈT2 Na2FeO4+2Na2O+2Na2SO4+O2ЁќжаFeдЊЫиЛЏКЯМлЩ§ИпЃЌБЛбѕЛЏЃЌOдЊЫиЛЏКЯМлгЩЉ1МлБфЮЊЉ2МлЁЂ0МлЃЌНсКЯЛЏКЯМлЕФБфЛЏНтД№ИУЬтЃЛ
ЃЈ4ЃЉгЩЭМЪОЗДгІдРэЃЌШмвКРяH2OжаЕФH+ЁЂCl-ЁЂCu2+УЛгаВЮгыбѕЛЏЛЙдЃЌМДHЁЂClЁЂCuШ§жждЊЫиЕФЛЏКЯМлУЛгаБфЛЏЁЃ
ЃЈ1ЃЉТШЦјШмгкЫЎКѓЩњГЩСЫДЮТШЫсКЭбЮЫсЃЌРызгЗДгІЮЊCl2+H2OЈTH++ClЉ+HClOЃЌЙЪД№АИЮЊЃКCl2+H2OЈTH++ClЉ+HClOЃЛ
ЃЈ2ЃЉKClO3гыSO2дкЧПЫсадШмвКжаЗДгІПЩжЦЕУC1O2ЃЌПЩжЊSO2БЛбѕЛЏГЩSO42ЉЃЌИУРызгЗДгІЮЊ2ClO3Љ+SO2ЈT2ClO2+SO42ЉЃЛClO2ПЩНЋЗЯЫЎжаЕФMn2+зЊЛЏЮЊMnO2ЖјГ§ШЅЃЌБОЩэЛЙдЮЊCl-ЃЌЦфРызгЗНГЬЪНЮЊ2ClO2+ 5Mn2++6H2O=5MnO2+ 2Cl-+12H+ЃЌПЩжЊИУЗДгІбѕЛЏМСгыЛЙдМСЮяжЪЕФСПжЎБШn(ClO2)ЃКn(Mn2+)=2ЃК5ЃЛЙЪД№АИЮЊ2ClO3Љ+SO2ЈT2ClO2+SO42ЉЃЛ2ЃК5ЃЛ
ЃЈ3ЃЉдкЕЭЮТЯТЃЌИпЬњЫсМиШнвзБфГЩЙЬЬхЮіГіЃЌЫЕУїЯрЭЌЬѕМўЯТЃЌИпЬњЫсФЦШмНтЖШБШИпЬњЫсМиШмНтЖШДѓЃЌЗДгІ2FeSO4+6Na2O2ЈT2 Na2FeO4+2Na2O+2Na2SO4+O2ЁќжаЃЌУПЩњГЩl mol Na2FeO4ЭЌЪБЩњГЩ0.5molбѕЦјЃЌдђзЊвЦЕчзгЮЊ1molЁСЃЈ6Љ2ЃЉ+0.5molЁС2ЁС[0ЉЃЈЉ1ЃЉ]ЃН5molЃЛЙЪД№АИЮЊЃКДѓЃЛ 5ЃЛ
ЃЈ4ЃЉгЩЭМЪОЗДгІдРэЃЌШмвКРяH2OжаЕФH+ЁЂCl-ЁЂCu2+УЛгаВЮгыбѕЛЏЛЙдЃЌМДHЁЂClЁЂCuШ§жждЊЫиЕФЛЏКЯМлУЛгаБфЛЏЃЌЦфЫќдЊЫиШыOЁЂFeЁЂSЕФЛЏКЯМлОљгаБфЛЏЃЌИУЭМЪОЕФзмЗДгІЮЊ2H2S+O2=2S![]() +2H2OЃЛЙЪД№АИЮЊЃКHЁЂClЁЂCuЃЛ2H2S+O2=2S
+2H2OЃЛЙЪД№АИЮЊЃКHЁЂClЁЂCuЃЛ2H2S+O2=2S![]() +2H2OЁЃ
+2H2OЁЃ


 ПкЫуаЁзДдЊПкЫуЫйЫуЬьЬьСЗЯЕСаД№АИ
ПкЫуаЁзДдЊПкЫуЫйЫуЬьЬьСЗЯЕСаД№АИ ЬьЬьСЗПкЫуЯЕСаД№АИ
ЬьЬьСЗПкЫуЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвЛЖЈЮТЖШЯТЃЌдк2LЕФУмБеШнЦїжаЃЌXЁЂ YЁЂZШ§жжЦјЬхЕФЮяжЪЕФСПЫцЪБМфБфЛЏЕФЧњЯпШчЭМЫљЪОЃК

ЯТСаУшЪіе§ШЗЕФЪЧЃЈ ЃЉ
A. ЗДгІПЊЪМЕН10sЃЌгУZБэЪОЕФЗДгІЫйТЪЮЊ0.158mol/(LЁЄs)Ѓ1
B. ЗДгІПЊЪМЕНl0sЃЌXЕФЮяжЪЕФСПХЈЖШМѕЩйСЫ0.79mol/L
C. ЗДгІПЊЪМЕН10sЪБЃЌYЕФзЊЛЏТЪЮЊ79.0%
D. ЗДгІЕФЛЏбЇЗНГЬЪНЮЊЃКX(g)ЃЋY(g)![]() Z(g)
Z(g)
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁП25ЁцЪБЃЌгУ0ЃЎ10molЁЄLЕФАБЫЎЕЮЖЈl0ЃЎ00mL0ЃЎ05molЁЄL-1H2AШмвКЃЌМгШыАБЫЎЕФЬхЛ§(V)гыШмвКжаlg![]() ЕФЙиЯЕШчЭМЫљЪО(КіТдШмвКЬхЛ§БфЛЏ)ЁЃЯТСаЫЕЗЈВЛе§ШЗЕФЪЧ
ЕФЙиЯЕШчЭМЫљЪО(КіТдШмвКЬхЛ§БфЛЏ)ЁЃЯТСаЫЕЗЈВЛе§ШЗЕФЪЧ
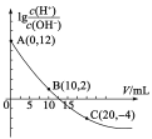
A.AЕуШмвКЕФpHЕШгк1
B.гЩЭМжаЪ§ОнПЩжЊЃЌH2AЮЊШѕЫс
C.BЕуЫЎЕчРыГіЕФH+РызгХЈЖШЮЊ1ЃЎ0ЁС10-6molЁЄL-1
D.CЕуШмвКжа![]()
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯрЖдЗжзгжЪСПЮЊMЕФЦјЬЌЛЏКЯЮяVL (БъзМзДПі)ЃЌШмгкmgЫЎжаЃЌЕУЕНжЪСПЗжЪ§ЮЊwЁЂ ЮяжЪЕФСПХЈЖШЮЊc mol/LЁЂУмЖШЮЊg/mLЕФШмвКЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧ( )
A.ЯрЖдЗжзгжЪСП M=22.4mІи/(1-Іи)V
B.ЮяжЪЕФСПХЈЖШc=Ібv/ЃЈMV+22.4mЃЉ
C.ШмвКЕФжЪСПЗжЪ§Іи=MV/22.4m
D.ШмвКУмЖШІб=cІи/1000ІбІи
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГЛЏбЇПЮЭтаЁзщЫљзіЪЕбщЕФЪОвтЭМШчЭМЫљЪОЃКЭМжаЁАЁњЁББэЪОЦјЬхСїЯђЃЌ MЪЧвЛжжДПОЛЖјИЩдяЕФЦјЬхЃЌYЮЊСэвЛжжЦјЬхЃЌEФкгаКьзиЩЋЦјЬхВњЩњЃЌЪЕбщЫљгУЮяжЪжЛФмгЩЯТСаЮяжЪжабЁШЁЃКNa2CO3ЁЂNa2O2ЁЂNaClЁЂNa2OЁЂCaCl2ЁЂ(NH4)2CO3ЁЂМюЪЏЛвЕШЙЬЬхМАеєСѓЫЎЁЃОнДЫЪЕбщЃЌЭъГЩЯТСаЬюПеЃК

(1)AжаЫљгУзАжУЕФжївЊвЧЦїКЭвЉЦЗЪЧ______________________ЁЃ
(2)BжаЫљбЁЕФИЩдяМСЪЧ________ЃЌЦфзїгУЪЧ______________________________ЁЃ
(3)CжаЗЂЩњЕФжївЊЗДгІЕФЛЏбЇЗНГЬЪНЃК________________________________ЁЃ
(4)жЦШЁYЦјЬхЕФDзАжУЫљгУЕФжївЊвЧЦїЪЧ__________________________ЁЃ
жЦШЁYЦјЬхЕФЛЏбЇЗНГЬЪНЪЧ________________________ЁЃ
(5)FжаЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЮЊ__________________________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПРћгУЩњЮяШМСЯЕчГидРэбаОПЪвЮТЯТАБЕФКЯГЩЃЌЕчГиЙЄзїЪБMV2+/MV+дкЕчМЋгыУИжЎМфДЋЕнЕчзгЃЌЪОвтЭМШчЯТЫљЪОЁЃЯТСаЫЕЗЈДэЮѓЕФЪЧ

A. ЯрБШЯжгаЙЄвЕКЯГЩАБЃЌИУЗНЗЈЬѕМўЮТКЭЃЌЭЌЪБЛЙПЩЬсЙЉЕчФм
B. вѕМЋЧјЃЌдкЧтЛЏУИзїгУЯТЗЂЩњЗДгІH2+2MV2+![]() 2H++2MV+
2H++2MV+
C. е§МЋЧјЃЌЙЬЕЊУИЮЊДпЛЏМСЃЌN2ЗЂЩњЛЙдЗДгІЩњГЩNH3
D. ЕчГиЙЄзїЪБжЪзгЭЈЙ§НЛЛЛФЄгЩИКМЋЧјЯђе§МЋЧјвЦЖЏ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПгаШчЯТЗДгІ(ЮДХфЦН)ЃКBrF3ЃЋH2OЁњBr2ЃЋO2ЃЋHBrO3ЃЋHFЃЌЗДгІКѓВтЕУЩњГЩBr2гыO2Иї1 molЁЃЯТСаХаЖЯДэЮѓЕФЪЧ
A.ЗДгІЙВзЊвЦ6 molЕчзг
B.бѕЛЏМСЮЊBrF3ЃЌЛЙдВњЮяЮЊBr2
C.ХфЦНКѓH2OгыHFЕФЮяжЪЕФСПжЎБШЮЊ5ЁУ9
D.БЛЫЎЛЙдЕФBrF3гыБЛздЩэЛЙдЕФBrF3ЕФЮяжЪЕФСПжЎБШЪЧ1ЁУ2
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСажИЖЈЗДгІЕФРызгЗНГЬЪНе§ШЗЕФЪЧ
A. CaЃЈClOЃЉ2ШмвКжаЭЈШыЩйСПSO2ЃКCa2++2ClO-+SO2+H2O=CaSO4Ё§+H++Cl-+ HClO
B. ЯђFeCl2ШмвКМгШызуСПNaClOШмвКЃК6Fe2++3ClO-+3H2O=2FeЃЈOHЃЉ3Ё§+4Fe3++3Cl-
C. NH4HCO3ШмвККЭЙ§СПЕФNaOHШмвКЛьКЯЃКHCO![]() +OH-===CO
+OH-===CO![]() +H2O
+H2O
D. ЯђFeЃЈNO3ЃЉ3ШмвКжаМгШызуСПЕФHIШмвКЃК2Fe3++2I-= 2Fe2++I2
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯжгаmgФГЦјЬхЃЌЫќгЩЫЋдзгЗжзгЙЙГЩЃЌЫќЕФФІЖћжЪСПЮЊMg/molЃЌШєАЂЗќМгЕТТоГЃЪ§гУNAБэЪОЃЌдђЃК
(1)ИУЦјЬхЫљКЌдзгзмЪ§ЮЊ______ ИіЁЃ
(2)ИУЦјЬхШєШмгк1LЫЎжа(ВЛПМТЧЗДгІ)ЃЌЩшШмвКЕФУмЖШЮЊІбg/cm3ЃЌдђИУШмвКЕФЮяжЪЕФСПХЈЖШЮЊ______ mol/LЁЃ
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com