
【题目】今有原子序数依次增大的A、B、C、D、E、F六种元素。已知A、C、F三原子的最外层共有11个电子,且这三种元素的最高价氧化物的水化物之间,两两皆能反应且均能生成盐和水。D和E各有如下表的电子层结构。
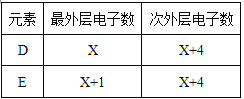
按要求填空:
(1)A的元素符号 ,质子数比中子数少2的B元素的一种核素的符号 ,F的原子结构示意图 。
(2)D和E两者的氢化物稳定性较强的是 (填化学式)。
(3)C单质与A元素的最高价氧化物对应的水化物反应的离子方程式为 。
(4)工业上制取单质D的化学方程式为 。
【答案】(1)Na;![]() ;
; ;
;
(2) PH3;(3) 2Al+2OH-+2H2O=2AlO2-+3H2↑;
(4) SiO2+2C![]() 2CO↑+Si。
2CO↑+Si。
【解析】试题分析:A、B、C、D、E、F为原子序数依次增大的短周期主族元素,A、C、F三种元素原子的最外层共有11个电子,且这三种元素的最高价氧化物的水化物之间两两皆能反应,均生成盐和水,C是Al元素,Al最外层有3个电子,那么A和F的最外层电子数为8,据此得出A应是金属性很强的元素且原子序数小于Al,则A是Na元素,F是Cl元素,B的原子序数大于A而小于C,所以B是Mg元素;D元素原子的最外层电子数比次外层少4个,最外层是8个电子,则其最外层是4个电子,所以D是Si元素;E元素原子次外层电子数比最外层多3个,次外层是8个电子,则最外层是5个电子,所以E是P元素。依据分析可知:A为钠、B为镁、C为铝、D为硅、E为磷、F为氯。
(1)A为Na,B是12号Mg元素,质子数比中子数少2的B元素的一种核素质量数是12+(12+2)=26,该原子的符号表示为![]() ;F为氯,F的原子结构示意图是
;F为氯,F的原子结构示意图是 ;
;
(2)D为硅、E为磷,由于元素的非金属性P>Si,元素的非金属性越强,其氢化物稳定性就越强。所以稳定性:PH3>SiH4;
(3)Al单质与A的最高价氧化物的水化物氢氧化钠溶液发生反应,产生偏铝酸钠和氢气,反应的离子方程式是:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(4)D为硅,在工业上是用焦炭还原SiO2制取Si的,反应的化学方程式是:SiO2+2C![]() 2CO↑+Si。
2CO↑+Si。


科目:高中化学 来源: 题型:
【题目】镍(28Ni)金属羰基化合物[金属元素和一氧化碳(CO)中性分子形成的一类配合物]、金属储氢材料[能可逆的多次吸收、储存和释放氢气(H2)的合金]等领域用途广泛。
(1)Ni原子基态核外电子排布式为_________________。
(2)Ni(CO)4中镍的化合价为_____________,写出与CO互为等电子体的中性分子、带一个单位正电荷的阳离子、带一个单位负电荷的阴离子各一个:__________、_____________、___________。
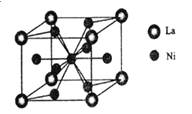
(3)一种储氢合金由镍与镧(La)组成,其晶胞结构如图所示.则该晶体的化学式为_________。
(4)下列反应常用来检验Ni2+,请写出另一产物的化学式__________。
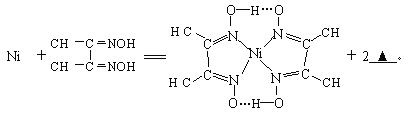
与Ni2+配位的N原子有_________个,该配合物中存在的化学键有__________(填序号)。
A共价键 B离子键 C配位键 D金属键 E氢键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知1 g氢气完全燃烧生成水蒸气时放出热量121 kJ,且氧气中1 mol O==O键完全断裂时吸收热量496 kJ,水蒸气中1 mol H—O键形成时放出热量463 kJ,则氢气中1 mol H—H键断裂时吸收热量为
A. 920 kJ B. 557 kJ C. 436 kJ D. 188 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃料电池是一种将化学反应产生的能量直接转化为电能的装置,你认为下列燃料电池比较适合宇宙飞船上使用的是( )
A.CH4—O2燃料电池
B.C2H5OH—O2燃料电池
C.H2—O2燃料电池
D.CO—O2燃料电池
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 镁带燃烧可以用CO2灭火
B. 单晶硅是重要的半导体材料,常用于制造光导纤维
C. Cl2能使湿润的有色布条褪色,是因为Cl2的氧化性
D. 金属钠可保存在煤油中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于水的离子积常数的叙述中,正确的是( )
A.因为水的离子积常数的表达式是KW=c(H+)·c(OH-),,所以KW随溶液H+和OH-浓度的变化而变化
B.水的离子积常数KW与水的电离平衡常数K电离是同一个物理量
C.水的离子积常数仅仅是温度的函数,随着温度的变化而变化
D.水的离子积常数KW与水的电离平衡常数K电离是两个没有任何关系的物理量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为实验室某浓盐酸试剂瓶标签上的有关信息,试根据标签上的有关数据,回答下列问题(一)(二):(计算结果保留一位小数)

(一).(1)浓盐酸中HCl的物质的量浓度为________mol·L-1。
(2) 量取___ ____mL浓盐酸加水稀释就得到500 mL、0.4mol·L-1的稀盐酸。
(二).取该浓盐酸10g与某MgCl2溶液90g混合,向混合溶液中逐滴加入10%的NaOH溶液,生成的沉淀的质量与加入的NaOH溶液质量关系如下图所示。

回答下列问题
(1)A点溶液的溶质化学式为 。
(2)与MgCl2反应的溶质氢氧化钠的质量为 g。
(3)恰好沉淀完全时,C点所得溶液中溶质的质量分数为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某电池以K2FeO4和Zn为电极材料,KOH溶液为电解质溶液。下列说法正确的是( )
A. Zn为电池的负极
B. 正极反应式为:2FeO42-+ 10H++6e- =Fe2O3+5H2O
C. 该电池放电过程中电解质溶液浓度不变
D. 电池工作时OH- 向负极迁移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应既是氧化还原反应,又是吸热反应的是( )
A.实验室制备氢气
B.灼热的碳与水的反应
C.Ba(OH)2·8H2O与NH4Cl的反应
D.铝粉与氧化铁粉末反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com