
【题目】“二![]() 英”是二苯基1,4二氧六环及其衍生物的通称,其中一种毒性最大的结构是
英”是二苯基1,4二氧六环及其衍生物的通称,其中一种毒性最大的结构是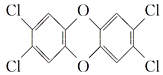 ,关于这种物质的叙述中不正确的是( )
,关于这种物质的叙述中不正确的是( )
A. 该物质不属于芳香族化合物
B. 该物质是一种卤代烃
C. 1 mol该物质最多可与6 mol H2在一定的条件下发生反应
D. 该物质分子中所有原子可能处在同一平面上
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A. 7.8 g Na2S和Na2O2的混合物中含有的阴离子数为NA
B. 17 g H2O2含有0.5NA个非极性共价键
C. 常温下,56 g铁片投入足量浓H2SO4中产生H2分子的个数为NA
D. 标准状况下,22.4LCl2溶于水转移的电子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质有关性质与应用的对应关系不正确的是
选项 | 化学性质 | 实际应用 |
A | ClO2具有强氧化性 | 用于自来水的消毒杀菌 |
B | Na2O2与CO2和H2O均能发生反应 | 用作呼吸面具供氧剂 |
C | 钠的金属性比钾弱 | Na与KCl反应制取单质钾 |
D | FeCl3溶液能与Cu反应 | 用FeCl3溶液蚀刻印刷电路板 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应伴随能量变化,下列说法中错误的是
A.TNT(炸药)爆炸时部分化学能转化为热能
B.电解饱和食盐水时部分化学能转化为电能
C.镁条燃烧时部分化学能转化为光能
D.植物光合作用时部分光能转化为化学能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学知识回答下列问题:
(1)①欲用98%的浓硫酸配制质量分数为20%的稀硫酸,实验中需要用到的仪器除了烧杯、玻璃棒以外,还需要_______________,其中玻璃棒的作用是________________。
②实验室需要0.1 mol·L-1的NaOH溶液450 mL。下列操作使所配NaOH溶液浓度偏高的是__________(填写序号)。
A.定容时俯视刻度线
B.选用的容量瓶内有少量蒸馏水
C.定容摇匀后,液面下降,又加水至刻度线
D.NaOH溶解后,未冷却就立即转移到容量瓶中
(2)焊接钢轨时常用的焊药为氯化铵,其作用是消除焊接处的铁锈。发生的反应体系中共有六种物质:NH4Cl、FeCl3、N2、Fe2O3、Fe和X。根据题意,判断X的化学式是____________,发生氧化反应的物质是___________,若有1mol Fe2O3参加反应,转移电子的物质的量为________mol。
(3)200mL某溶液中有5种离子大量共存,其中4种离子的物质的量如下表:
离子 | H+ | K+ | NO3- | SO42- |
物质的量(mol) | 0.5 | 0.1 | 0.6 | 0.15 |
则另外一种离子是_______(填写代号),该离子的浓度为_________________。
A.Fe2+ B.Cl- C. Al3+ D.ClO-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知化学反应A2(g)+ B2(g) = 2AB(g)的能量变化如图所示,判断下列叙述中正确的是

A.每生成2分子AB吸收bkJ热量
B.断裂1molA—A和1molB—B键,放出akJ能量
C.该反应中反应物的总能量高于生成物的总能量
D.该反应热△H=+(a-b)kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某废液中含有Fe3+、Cu2+、Ba2+、Cl-四种离子,某化学实验小组设计下列方案对废液进行处理,以回收金属并制备氯化钡、氯化铁晶体。

回答下列问题:
(1)写出向废液中加入过量铁粉发生反应的离子方程式______________________。
(2)沉淀A中含有的金属单质是_______________。
(3)下列物质中,可以用作试剂X的是_____________(填写序号)。
A.BaCl2 B.BaCO3 C.NaOH D.Ba(OH)2
(4)向溶液B中通入Cl2的作用是__________________;实验过程中该小组同学用NaCl固体、MnO2和浓硫酸混合加热的办法制得Cl2,写出反应的化学方程式________________;由于Cl2有毒,某同学建议用双氧水替换,请写出向溶液B中加入双氧水后发生反应的离子方程式__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.据报道,日常生活中,将洁厕液与84消毒液混合使用会发生中毒的事故。
(1)84消毒液的主要成分是次氯酸钠,次氯酸钠与空气中CO2反应生成次氯酸,写出次氯酸钠的电子式:__________;若将84消毒液长期露置于空气中,溶液中的主要成分将变为__________(填化学式)。
(2)洁厕灵的主要成分是HCl。洁厕液与84消毒液混合后会发生氧化还原反应,生成有毒的氯气。写出该反应的离子方程式:______________________________。
(3)下列氧化还原反应中,与上述反应类型不同的是________。
A.Na2S2O3+H2SO4===Na2SO4+S↓+SO2↑+H2O B.2FeCl3+Fe===3FeCl2
C.S+2H2SO4(浓)![]() 3SO2↑+2H2O D.KClO3+5KCl+3H2SO4===3K2SO4+3Cl2↑+3H2O
3SO2↑+2H2O D.KClO3+5KCl+3H2SO4===3K2SO4+3Cl2↑+3H2O
II.已知高锰酸钾(硫酸酸化)溶液和草酸(H2C2O4)溶液可以发生氧化还原反应。请回答下列问题:
(1)该反应中的还原剂是________(填化学式)。
(2)写出该反应的离子方程式:____________________________________________。
(3)若生成1molCO2则转移电子_______mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是部分短周期元素的单质及其化合物(或其溶液)的转化关系,已知B、C、D、E是非金属单质,且在常温常压下都是气体,化合物G的焰色反应为黄色,化合物I和J通常状况下呈气态;反应①是化工生产中的一种重要固氮反应。

请回答下列问题:
(1)写出下列物质化学式:A_______C________D________
(2)写出下列物质间反应的化学方程式:
①A+B____________________;②F+CO2________________
③D+E___________________________;④I+J___________________
(3)写出下列反应的离子方程式G+I________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com